LA COMISIÓN EUROPEA,
Visto el Tratado de Funcionamiento de la Unión Europea,
Visto el Reglamento (CE) nº 1069/2009 del Parlamento Europeo y del Consejo, de 21 de octubre de 2009, por el que se establecen las normas sanitarias aplicables a los subproductos animales y los productos derivados no destinados al consumo humano y por el que se deroga el Reglamento (CE) nº 1774/2002 (Reglamento sobre subproductos animales) [1], y, en particular, su artículo 5, apartado 2; su artículo 6, apartado 1, letra b), inciso ii); su artículo 6, apartado 1, párrafo segundo; su artículo 6, apartado 2, párrafo segundo; su artículo 11, apartado 2, letras b) y c); su artículo 11, apartado 2, párrafo segundo; su artículo 15, apartado 1, letras b), d), e), h) e i); su artículo 15, apartado 1, párrafo segundo; su artículo 17, apartado 2; su artículo 18, apartado 3; su artículo 19, apartado 4, letras a), b) y c); su artículo 19, apartado 4, párrafo segundo; su artículo 20, apartados 10 y 11; su artículo 21, apartados 5 y 6; su artículo 22, apartado 3; su artículo 23, apartado 3; su artículo 27, letras a), b), c) y e) a h), y su artículo 27, párrafo segundo; su artículo 31, apartado 2; su artículo 32, apartado 3; su artículo 40; su artículo 41, apartado 3, párrafos primero y tercero; su artículo 42; su artículo 43, apartado 3; su artículo 45, apartado 4; su artículo 47, apartado 2; su artículo 48, apartado 2; su artículo 48, apartado 7, letra a), apartado 8, letra a), y su artículo 48, apartado 8, párrafo segundo,
Vista la Directiva 97/78/CE del Consejo, de 18 de diciembre de 1997, por la que se establecen los principios relativos a la organización de controles veterinarios de los productos que se introduzcan en la Comunidad procedentes de países terceros [2] y, en particular, su artículo 16, apartado 3,
Considerando lo siguiente:
(1) El Reglamento (CE) nº 1069/2009 establece normas en materia de salud animal y salud pública aplicables a los subproductos animales y los productos derivados. Dicho Reglamento determina las circunstancias en las que deben eliminarse los subproductos animales a fin de impedir la propagación de riesgos para la salud pública y animal. Asimismo, dicho Reglamento especifica en qué condiciones pueden emplearse los subproductos animales para la alimentación animal y otros usos diversos, como en cosmética, medicamentos y usos técnicos. Establece igualmente las obligaciones que deben cumplir los operadores en lo que respecta a la manipulación de subproductos animales dentro de establecimientos y plantas sometidos a control oficial.
(2) El Reglamento (CE) nº 1069/2009 dispone que deben adoptarse, mediante medidas de aplicación, normas detalladas para la manipulación de los subproductos animales y productos derivados, como las normas aplicables a la transformación, las condiciones higiénicas y el formato de los documentos que deben acompañar a los envíos de subproductos animales y productos derivados a los efectos de garantizar la trazabilidad.
(3) En el presente Reglamento deben establecerse normas detalladas de uso y eliminación de subproductos animales para alcanzar los objetivos del Reglamento (CE) nº 1069/2009, principalmente el uso sostenible de materiales de origen animal y un elevado nivel de protección de la salud pública y la salud animal en la Unión Europea.
(4) El Reglamento (CE) nº 1069/2009 no se aplica a los cuerpos enteros o partes de animales silvestres que no sean sospechosos de estar infectados o afectados por una enfermedad transmisible a personas o animales, con excepción de los animales acuáticos desembarcados con fines comerciales. Tampoco se aplica a los cuerpos enteros o partes de animales de caza silvestres que no se recojan después de cazados, de conformidad con las buenas prácticas de caza. La eliminación de los subproductos animales procedentes de la caza debe realizarse de modo que se impida la transmisión de riesgos, según corresponda a las prácticas específicas de caza y de conformidad con las buenas prácticas descritas en la profesión de la caza.
(5) El Reglamento (CE) nº 1069/2009 se aplica a los subproductos animales para el preparado de trofeos de caza. El preparado de tales trofeos de caza, así como los preparados de animales y partes de los mismos en los que se usen otros métodos, como la plastinación, deberá realizarse en condiciones que impidan la transmisión de riesgos para la salud humana o animal.
(6) El Reglamento (CE) nº 1069/2009 se aplica a los residuos de cocina procedentes de medios de transporte internacional, como materiales derivados de alimentos servidos a bordo de un avión o de un buque que llegue a la Unión Europea desde un tercer país. Los residuos de cocina entran asimismo dentro del ámbito de dicho Reglamento cuando estén destinados a la alimentación animal, para su transformación de acuerdo con uno de los métodos de transformación autorizados en el presente Reglamento, o a su transformación en biogás o a compostaje. El Reglamento (CE) nº 1069/2009 prohíbe la alimentación de animales de granja, distintos de los animales de peletería, con residuos de cocina. Por lo tanto, de conformidad con el Reglamento (CE) nº 1069/2009, los residuos de cocina pueden ser transformados y usados posteriormente, siempre que el producto derivado no sirva de alimentación a dichos animales.
(7) En aras de la coherencia de la legislación de la Unión, la definición de materias primas para piensos del Reglamento (CE) nº 767/2009 del Parlamento Europeo y del Consejo, de 13 de julio de 2009, sobre la introducción en el mercado y la utilización de los piensos, por el que se modifica el Reglamento (CE) nº 1831/2003 del Parlamento Europeo y del Consejo y se derogan las Directivas 79/373/CEE del Consejo, 80/511/CEE de la Comisión, 82/471/CEE del Consejo, 83/228/CEE del Consejo, 93/74/CEE del Consejo, 93/113/CE del Consejo y 96/25/CE del Consejo y la Decisión 2004/217/CE de la Comisión [3] debe usarse como base para la definición de materias primas para piensos de origen animal en el presente Reglamento.
(8) El Reglamento (CE) nº 1069/2009 prohíbe el envío de subproductos animales y de productos derivados de especies sensibles desde explotaciones, establecimientos, plantas o zonas en los que estén sujetos a restricciones debido a la presencia de una enfermedad transmisible grave. La lista de enfermedades incluidas en los Códigos Sanitarios de los Animales Terrestres y Animales Acuáticos de la Organización Mundial de Sanidad Animal (OIE) debe especificarse como lista de enfermedades transmisibles graves a los efectos de determinar el alcance de esta prohibición, con el objeto de garantizar un nivel elevado de protección de la salud pública y la salud animal en la Unión.
(9) En el presente Reglamento deben establecerse las normas adecuadas para la prevención de riesgos para la salud derivados de la incineración y la coincineración de determinados subproductos animales que no están cubiertos en el alcance de la Directiva 2000/76/CE del Parlamento Europeo y el Consejo, de 4 de diciembre de 2000, relativa a la incineración de residuos [4], teniendo en cuenta las posibles repercusiones sobre el medio ambiente. Los residuos de las actividades de incineración o coincineración de subproductos animales o productos derivados deben reciclarse o eliminarse con arreglo a la legislación medioambiental de la Unión, ya que, en particular, dicha legislación permite el uso del componente fosforoso de cenizas en abonos así como la entrega de las cenizas procedentes de la cremación de animales de compañía a sus propietarios.
(10) Los productos de origen animal o productos alimenticios que los contengan deben eliminarse únicamente en un vertedero, con arreglo a la Directiva 1999/31/CE del Consejo, de 26 de abril de 1999, relativa al vertido de residuos [5], si han sido transformados con arreglo a lo dispuesto en el Reglamento (CE) nº 852/2004 del Parlamento Europeo y del Consejo, de 29 de abril de 2004, relativo a la higiene de los productos alimenticios [6], para limitar los riesgos para la salud.
(11) Debe prohibirse la eliminación de subproductos animales o productos derivados a través de la corriente de aguas residuales, que no está sujeta a los requisitos que garantizarían un control adecuado de los riesgos para la salud pública y la salud animal. Deben adoptarse las medidas apropiadas para evitar riesgos inaceptables de una eliminación accidental de subproductos animales líquidos, como los procedentes de la limpieza de suelos y equipos destinados a la transformación.
(12) La Directiva 2008/98/CE del Parlamento Europeo y del Consejo, de 19 de noviembre de 2008, sobre los residuos y por la que se derogan determinadas Directivas [7] establece ciertas medidas de protección del medio ambiente y de la salud humana. Su artículo 2, apartado 2, letra b), establece que determinadas materias primas quedan excluidas del ámbito de aplicación de la Directiva en la medida en la que ya están cubiertas por otras normativas de la Unión, incluidos los subproductos animales cubiertos por el Reglamento (CE) nº 1774/2002 del Parlamento Europeo y del Consejo, de 3 de octubre de 2002, por el que se establecen las normas sanitarias aplicables a los subproductos animales no destinados al consumo humano [8], excepto los destinados a la incineración, los vertederos o utilizados en una planta de biogás o de compostaje. Dicho Reglamento ha sido derogado y sustituido por el Reglamento (CE) nº 1069/2009 a partir del 4 de marzo de 2011. En aras de la coherencia de la legislación de la Unión, los procesos de transformación en biogás y de compostaje de los subproductos animales y derivados deben cumplir las normas sanitarias establecidas en el presente Reglamento, así como las medidas de protección del medio ambiente estipuladas en la Directiva 2008/98/CE.
(13) La autoridad competente de un Estado miembro debe ser capaz de autorizar parámetros alternativos para la transformación de subproductos animales en biogás o para su compostaje de conformidad con una validación realizada con arreglo a un modelo armonizado. En tal caso, debe ser posible introducir en el mercado los residuos de fermentación y el compost en toda la Unión Europea. Además, la autoridad competente de un Estado miembro debe ser capaz de autorizar ciertos parámetros para subproductos animales específicos que se transformen en biogás o en compost, como los residuos de cocina y sus mezclas con determinados materiales. Al no emitirse dichas autorizaciones con arreglo a un modelo armonizado, los residuos de fermentación y el compost deben comercializarse únicamente en el mercado del Estado miembro en el que se han autorizado los parámetros.
(14) Para evitar la contaminación de los productos alimenticios con agentes patógenos, los establecimientos o plantas de transformación de subproductos animales deben operar en un emplazamiento distinto de los mataderos u otros establecimientos en que se transforman productos alimenticios, en particular conforme al Reglamento (CE) nº 853/2004 del Parlamento Europeo y del Consejo, de 29 de abril de 2004, por el que se establecen normas específicas de higiene de los alimentos de origen animal [9], salvo cuando la transformación de los subproductos animales se desarrolla en condiciones autorizadas por la autoridad competente, con vistas a impedir la transmisión de riesgos para la salud pública y la salud animal en los establecimientos de transformación de alimentos.
(15) El Reglamento (CE) nº 999/2001 del Parlamento Europeo y del Consejo, de 22 de mayo de 2001, por el que se establecen disposiciones para la prevención, el control y la erradicación de determinadas encefalopatías espongiformes transmisibles [10] establece que los Estados miembros deben introducir programas anuales de seguimiento de las encefalopatías espongiformes transmisibles (EET). Los cuerpos de animales usados para la alimentación de ciertas especies, con objeto de fomentar la biodiversidad, deben incluirse en dichos programas de seguimiento en la medida necesaria para garantizar que estos programas ofrezcan información suficiente sobre la prevalencia de las EET en un Estado miembro determinado.
(16) El Reglamento (CE) nº 1069/2009 permite alimentar con determinados materiales de la categoría 1 las especies en peligro o protegidas de aves necrófagas y otras especies que vivan en su hábitat natural, para fomentar la biodiversidad. Dicha alimentación debe ser autorizada en el caso de ciertas especies carnívoras contempladas en la Directiva 92/43/CEE del Consejo, de 21 de mayo de 1992, relativa a la conservación de los hábitats naturales y de la fauna y flora silvestres [11] y en el caso de ciertas especies de aves de presa contempladas en la Directiva 2009/147/CE del Parlamento Europeo y del Consejo, de 30 de noviembre de 2009, relativa a la conservación de las aves silvestres [12], con el fin de tener en cuenta las pautas naturales de alimentación de tales especies.
(17) El Reglamento (CE) nº 1069/2009 introduce un procedimiento para la autorización de métodos alternativos de uso o eliminación de subproductos animales o productos derivados. Dichos métodos pueden ser autorizados por la Comisión previo dictamen de la Autoridad Europea de Seguridad Alimentaria (EFSA). Para facilitar la evaluación de solicitudes por la EFSA, conviene crear un modelo estándar que indique a los solicitantes el tipo de pruebas que deben presentar. De conformidad con los Tratados, debe ser posible presentar solicitudes por métodos alternativos en las lenguas oficiales de la Unión Europea, conforme a lo dispuesto en el Reglamento no 1 del Consejo por el que se fija el régimen lingüístico de la Comunidad Económica Europea [13].
(18) De conformidad con el Reglamento (CE) nº 183/2005 del Parlamento Europeo y del Consejo, de 12 de enero de 2005, por el que se fijan requisitos en materia de higiene de los piensos [14], los explotadores de empresas de piensos distintos de los productores primarios tienen la obligación de almacenar y transportar los piensos bajo ciertas condiciones de higiene. Puesto que dichas condiciones prevén una reducción equivalente de los riesgos, los piensos compuestos derivados de subproductos animales no están sometidos a los requisitos establecidos en el presente Reglamento al respecto del almacenamiento y el transporte.
(19) Para la promoción de la ciencia y la investigación y para garantizar el mejor uso posible de los subproductos animales y productos derivados en el diagnóstico de enfermedades humanas o animales, la autoridad competente debe contar con autorización para imponer condiciones a las muestras de dichos materiales para los propósitos de investigación, educación y diagnóstico. No obstante, tales condiciones no deben imponerse a las muestras de agentes patógenos para las que se contemplan normas especiales en la Directiva 92/118/CEE del Consejo, de 17 de diciembre de 1992, por la que se establecen las condiciones de policía sanitaria y sanitarias aplicables a los intercambios y a las importaciones en la Comunidad de productos no sometidos, con respecto a estas condiciones, a las normativas comunitarias específicas contempladas en el capítulo I del Anexo A de la Directiva 89/662/CEE y, por lo que se refiere a los patógenos, de la Directiva 90/425/CEE [15].
(20) La Directiva 97/78/CE exime de los controles veterinarios en el puesto de inspección fronterizo de entrada en la Unión a los subproductos animales destinados a exposiciones, a condición de que no vayan a ser comercializados, y a los destinados a estudios o análisis concretos. Dicha Directiva permite la adopción de medidas de aplicación de dichas exenciones. Deben establecerse en el presente Reglamento las condiciones adecuadas para la importación de subproductos animales y productos derivados destinados a exposiciones y estudios o análisis concretos, con el fin de garantizar que no se propagan riesgos inaceptables para la salud pública o animal al introducirlos en la Unión. En aras de la coherencia de la legislación de la Unión y a fin de proporcionar seguridad jurídica a los operadores, deben establecerse en el presente Reglamento tales condiciones, así como las medidas de aplicación de la Directiva 97/78/CE.
(21) Los subproductos animales deben manipularse tras su recogida en condiciones adecuadas que garanticen que no se transmiten riesgos inaceptables para la salud pública o animal. Los establecimientos o plantas en los que se efectúan determinadas actividades antes de enviar los subproductos animales para su posterior transformación deben construirse y operar de forma que se prevenga tal transmisión. Entre estos establecimientos o plantas deben figurar los que realizan actividades que conllevan la manipulación de subproductos animales de conformidad con la legislación veterinaria de la Unión, distintas de la manipulación de subproductos animales en la actividad terapéutica de los veterinarios privados.
(22) De conformidad con el Reglamento (CE) nº 1069/2009, los explotadores deben garantizar la trazabilidad de los subproductos animales y los productos derivados en todas las fases de la cadena de fabricación, uso y eliminación, para evitar perturbaciones innecesarias del mercado interior en caso de riesgo para la salud pública o animal. Por ello, la trazabilidad no deben garantizarla exclusivamente los explotadores que generan, recogen o transportan subproductos animales, sino también los que eliminan los subproductos animales o productos derivados por incineración, coincineración o eliminación en vertedero.
(23) Los contenedores y medios de transporte usados para subproductos animales o productos derivados deben mantenerse limpios, para evitar la contaminación. Cuando se dedican al transporte de un material concreto, como un subproducto animal líquido que no entraña riesgos inaceptables para la salud, los explotadores pueden adaptar sus medidas de prevención de la contaminación al riesgo que conlleva realmente dicho material.
(24) Los Estados miembros deben contar con autorización para exigir que los explotadores empleen el sistema veterinario informatizado integrado (Traces) introducido por la Decisión 2004/292/CE de la Comisión, de 30 de marzo de 2004, relativa a la aplicación del sistema Traces y por la que se modifica la Decisión 92/486/CEE [16] ("el sistema TRACES") para confirmar la llegada de las partidas de subproductos animales o productos derivados a su lugar de destino. Como alternativa, debe facilitarse una confirmación de la llegada del envío mediante una cuarta copia del documento comercial, que debe devolverse al productor. Transcurrido el primer año de aplicación del Reglamento, debe evaluarse la experiencia con ambas alternativas.
(25) El Reglamento (CE) nº 853/2004 establece ciertos parámetros para el tratamientos de grasas extraídas, aceite de pescado y ovoproductos que proporcionan un control adecuado de los riesgos para la salud, cuando dichos productos se usan para fines distintos del consumo humano. Estos parámetros deben ser autorizados, por tanto, como alternativas a los tratamientos para subproductos animales definidos en el presente Reglamento.
(26) El calostro y los productos a base de calostro deben proceder de rebaños bovinos indemnes de determinadas enfermedades recogidas en la Directiva 64/432/CEE del Consejo, de 26 de junio de 1964, relativa a problemas de policía sanitaria en materia de intercambios intracomunitarios de animales de las especies bovina y porcina [17].
(27) Procede actualizar las referencias a la Directiva 76/768/CEE del Consejo, de 27 de julio de 1976, relativa a la aproximación de las legislaciones de los Estados Miembros en materia de productos cosméticos [18], a la Directiva 96/22/CE del Consejo, de 29 de abril de 1996, por la que se prohíbe utilizar determinadas sustancias de efecto hormonal y tireostático y sustancias ß-agonistas en la cría de ganado [19], a la Directiva 96/23/CE del Consejo, de 29 de abril de 1996, relativa a las medidas de control aplicables respecto de determinadas sustancias y sus residuos en los animales vivos y sus productos [20], como también procede actualizar las referencias a la Directiva 2009/158/CE del Consejo, de 30 de noviembre de 2009, relativa a las condiciones de policía sanitaria que regulan los intercambios intracomunitarios y las importaciones de aves de corral y de huevos para incubar procedentes de terceros países [21] en las normas sanitarias aplicables al comercio de estiércol sin transformar.
(28) Ciertos materiales importados para la fabricación de alimentos para animales de compañía deben manipularse y utilizarse en condiciones adecuadas a los riesgos que entrañan. En especial, debe preverse su canalización segura hasta el establecimiento o planta de destino, donde se incorporarán a los alimentos para animales de compañía junto con material perteneciente a la categoría 3. Con respecto a los establecimientos o las plantas de destino, la autoridad competente debe contar con autorización para permitir el almacenamiento de materiales importados junto con material de la categoría 3, siempre que se preserve la trazabilidad de los materiales importados.
(29) El Reglamento (CE) nº 1069/2009 alude a determinados productos derivados que pueden ser introducidos en el mercado con arreglo a condiciones establecidas en otra legislación de la Unión. Esa legislación establece asimismo las condiciones para la importación, la recogida y el transporte de subproductos animales y productos derivados para la fabricación de los productos derivados mencionados. No obstante, el Reglamento (CE) nº 1069/2009 es de aplicación cuando la otra legislación de la Unión no establece condiciones relativas a los riesgos para la salud pública y animal que puedan conllevar dichas materias primas. Puesto que tales condiciones no se han establecido al respecto de materiales que se han sometido a ciertas fases de transformación antes de satisfacer las condiciones de introducción en el mercado conforme a dicha legislación de la Unión, deben establecerse en el presente Reglamento. En concreto, deben definirse las condiciones para la importación y manipulación de dichos materiales dentro de la Unión bajo estrictos requisitos de control y documentación, para evitar la transmisión de riesgos sanitarios que puedan entrañar dichos materiales.
(30) En concreto, deben preverse en el presente Reglamento condiciones sanitarias adecuadas para los materiales empleados en la fabricación de medicamentos, con arreglo a la Directiva 2001/83/CE del Parlamento Europeo y del Consejo, de 6 de noviembre de 2001, por la que se establece un código comunitario sobre medicamentos para uso humano [22]; de medicamentos veterinarios, con arreglo a la Directiva 2001/82/CE del Parlamento Europeo y del Consejo, de 6 de noviembre de 2001, por la que se establece un código comunitario sobre medicamentos veterinarios [23]; de productos sanitarios, con arreglo a la Directiva 93/42/CEE del Consejo, de 14 de junio de 1993, relativa a los productos sanitarios [24]; de productos para el diagnóstico in vitro, con arreglo a la Directiva 98/79/CE del Parlamento Europeo y del Consejo, de 27 de octubre de 1998, sobre productos sanitarios para diagnóstico in vitro [25]; de productos sanitarios implantables activos, con arreglo a la Directiva 90/385/CEE del Consejo, de 20 de junio de 1990, relativa a la aproximación de las legislaciones de los Estados miembros sobre los productos sanitarios implantables activos [26]; o de reactivos de laboratorio ("los productos acabados"). Si los riesgos que puedan originarse en dichos materiales se atenúan gracias a la purificación, concentración en el producto o debido a las condiciones de manipulación o eliminación, solo deben aplicarse los requisitos del Reglamento (CE) nº 1069/2009 y del presente Reglamento respecto a la trazabilidad. En tal caso, no deben aplicarse los requisitos relacionados con la separación de los subproductos animales de distintas categorías dentro del establecimiento o fábrica que produce los productos acabados, puesto que el posterior uso de los materiales para otros fines, en concreto su desviación hacia las cadenas de alimentación humana o animal, puede excluirse gracias a la correcta aplicación de las normas por parte del explotador, bajo la responsabilidad de la autoridad competente. Las partidas de dichos materiales que vayan a importarse a la Unión deben someterse a controles veterinarios en los puestos de inspección fronterizos de entrada con arreglo a la Directiva 97/78/CE, a fin de verificar que dichos productos cumplen los requisitos de introducción en el mercado en la Unión.
(31) Ciertas enfermedades a las que son sensibles los équidos son de declaración obligatoria, en virtud de la Directiva 2009/156/CE del Consejo, de 30 de noviembre de 2009, relativa a las condiciones de policía sanitaria que regulan los movimientos de équidos y las importaciones de équidos procedentes de terceros países [27]. Los productos derivados de la sangre de équidos destinados a fines distintos de la alimentación animal, por ejemplo a medicamentos veterinarios, deben proceder de équidos que no presentan signos clínicos de tales enfermedades, a fin de reducir el riesgo de su transmisión.
(32) Debe permitirse la introducción en el mercado de pieles frescas para fines distintos del consumo humano, a condición de que cumplan las condiciones sanitarias para carne fresca definidas con arreglo a la Directiva 2002/99/CE del Consejo, de 16 de diciembre de 2002, por la que se establecen las normas zoosanitarias aplicables a la producción, transformación, distribución e introducción de los productos de origen animal destinados al consumo humano [28], puesto que estas condiciones establecen una disminución apropiada de los riesgos para la salud.
(33) Las normas sanitarias estipuladas en el presente Reglamento para la fabricación e introducción en el mercado de trofeos de caza y otros preparados de animales que eliminan riesgos vienen a añadirse a las normas para la protección de determinadas especies de fauna silvestre establecidas en el Reglamento (CE) nº 338/97 del Consejo, de 9 de diciembre de 1996, relativo a la protección de especies de fauna y flora silvestres mediante el control de su comercio [29], debido al diferente objetivo de dicho Reglamento. Las preparaciones anatómicas de animales o subproductos animales que se han sometido a un proceso como la plastinación que elimina igualmente los riesgos no deben estar sujetos a las restricciones zoosanitarias, para facilitar el uso de dichas preparaciones, en particular, con fines educativos.
(34) Los subproductos de la apicultura que vayan a introducirse en el mercado deben estar indemnes de determinadas enfermedades a las que son sensibles las abejas según lo dispuesto en la Directiva 92/65/CEE del Consejo, de 13 de julio de 1992, por la que se establecen las condiciones de policía sanitaria aplicables a los intercambios y las importaciones en la Comunidad de animales, esperma, óvulos y embriones no sometidos, con respecto a estas condiciones, a las normativas comunitarias específicas a que se refiere la sección I del Anexo A de la Directiva 90/425/CEE [30].
(35) El Parlamento Europeo y el Consejo han instado a la Comisión a definir un punto final en la cadena de fabricación de los productos oleoquímicos, tras el cual no han de someterse a los requisitos del Reglamento (CE) nº 1069/2009. La decisión relativa al punto final debe adoptarse en cuanto se disponga de una evaluación que valore la capacidad del proceso oleoquímico para reducir los riesgos para la salud que puedan estar presentes en grasas animales de cualquier categoría que sean objeto de transformación.
(36) Debe hacerse referencia en el presente Reglamento al Reglamento (UE) nº 206/2010 de la Comisión, de 12 de marzo de 2010, por el que se establecen listas de terceros países, territorios o partes de terceros países o territorios autorizados a introducir en la Unión Europea determinados animales o carne fresca y los requisitos de certificación veterinaria [31], en la medida en que dichos terceros países o territorios deban ser autorizados para importar determinados subproductos animales o productos derivados, puesto que los riesgos que entrañan dichos productos son idénticos a los que pueden proceder de la importación de animales vivos o carne fresca.
(37) Se debería hacer referencia a otras listas de terceros países desde los que ciertos materiales de origen animal pueden ser importados, con el propósito de determinar los terceros países desde los cuales se pueden importar subproductos animales de las respectivas especies, basándose en consideraciones similares relativas a los riesgos sanitarios y para garantizar la coherencia de la legislación de la Unión. Estas listas se han establecido en la Decisión 2004/211/CE de la Comisión, de 6 de enero de 2004, por la que se establece la lista de terceros países y partes de su territorio a partir de los cuales los Estados miembros autorizan la importación de équidos vivos y esperma, óvulos y embriones de la especie equina y por la que se modifican las Decisiones 93/195/CEE y 94/63/CE [32], el Reglamento (UE) nº 605/2010 de la Comisión, de 2 de julio de 2010, por el que se establecen las condiciones sanitarias y zoosanitarias, así como los requisitos de certificación veterinaria, para la introducción en la Unión Europea de leche cruda y productos lácteos destinados al consumo humano [33], la Decisión 2006/766/CE de la Comisión, de 6 de noviembre de 2006, por la que se establecen las listas de terceros países y territorios desde los que se autorizan las importaciones de moluscos bivalvos, equinodermos, tunicados, gasterópodos marinos y productos de la pesca [34], el Reglamento (CE) nº 798/2008 de la Comisión, de 8 de agosto de 2008, por el que se establece una lista de terceros países, territorios, zonas o compartimentos desde los cuales están permitidos la importación en la Comunidad o el tránsito por la misma de aves de corral y productos derivados, junto con los requisitos de certificación veterinaria [35] y el Reglamento (CE) nº 119/2009 de la Comisión, de 9 de febrero de 2009, por el que se establece una lista de terceros países o partes de los mismos para la importación en la Comunidad, o para el tránsito por la misma, de carne de lepóridos silvestres, de determinados mamíferos terrestres silvestres y de conejo de granja y los requisitos de certificación veterinaria [36].
(38) Como los residuos de la industria fotográfica que utiliza determinados subproductos animales, por ejemplo, la columna vertebral de bovinos, no solo entrañan riesgos para la salud pública y la salud animal, sino también riesgos para el medio ambiente, deben eliminarse o exportarse al tercer país de origen de los subproductos animales de conformidad con el Reglamento (CE) nº 1013/2006 del Parlamento Europeo y del Consejo, de 14 de junio de 2006, relativo a los traslados de residuos [37].
(39) Hay que hacer referencia a la lista de puestos de inspección fronterizos establecida en la Decisión 2009/821/CE de la Comisión, de 28 de septiembre de 2009, por la que se establece una lista de puestos de inspección fronterizos autorizados y se disponen determinadas normas sobre las inspecciones efectuadas por los expertos veterinarios de la Comisión, así como las unidades veterinarias en Traces [38], en las normas sobre el tránsito, entre territorios de la Federación Rusa a través de la Unión Europea, de determinados subproductos animales y productos derivados. A los efectos de este tránsito, debe usarse el Documento Veterinario Común de Entrada establecido en el Reglamento (CE) nº 136/2004 de la Comisión, de 22 de enero de 2004, por el que se establecen los procedimientos de control veterinario en los puestos de inspección fronterizos de la Comunidad de los productos importados de terceros países [39].
(40) El presente Reglamento debe disponer que los certificados sanitarios que han de acompañar a los envíos de subproductos animales o productos derivados en el punto de entrada en la Unión en el que se vayan a efectuar los controles veterinarios han de expedirse con arreglo a los principios de certificación equivalentes a los dispuestos en la Directiva 96/93/CE del Consejo de 17 de diciembre de 1996 relativa a la certificación de animales y productos animales [40].
(41) En aras de la coherencia de la legislación de la Unión, deben realizarse controles oficiales en la totalidad de la cadena de subproductos animales y productos derivados de conformidad con las obligaciones generales de controles oficiales dispuestas en el Reglamento (CE) nº 882/2004 del Parlamento Europeo y del Consejo, de 29 de abril de 2004, sobre los controles oficiales efectuados para garantizar la verificación del cumplimiento de la legislación en materia de piensos y alimentos y la normativa sobre salud animal y bienestar de los animales [41].
(42) Por consiguiente, es necesario adoptar medidas de aplicación del Reglamento (CE) nº 1069/2009 en el presente Reglamento.
(43) El Reglamento (CE) nº 1069/2009 deroga el Reglamento (CE) nº 1774/2002 a partir del 4 de marzo de 2011.
(44) A raíz de la adopción del Reglamento (CE) nº 1774/2002, se adoptaron otros actos de aplicación, a saber: el Reglamento (CE) nº 811/2003 sobre la prohibición del reciclado dentro de la misma especie en el caso de los peces, al enterramiento y la incineración de subproductos animales [42], la Decisión 2003/322/CE de la Comisión sobre alimentación de las especies de aves necrófagas con determinados materiales de la categoría 1 [43], la Decisión 2003/324/CE de la Comisión relativa a una excepción a la prohibición de reciclado dentro de la misma especie para los animales de peletería [44], el Reglamento (CE) nº 79/2005 de la Comisión sobre la leche y los productos lácteos [45], el Reglamento (CE) nº 92/2005 de la Comisión sobre métodos de eliminación o utilización de subproductos animales [46], el Reglamento (CE) nº 181/2006 de la Comisión sobre los abonos y las enmiendas del suelo de origen orgánico, con excepción del estiércol [47], el Reglamento (CE) nº 1192/2006 de la Comisión sobre listas de plantas autorizadas [48] y el Reglamento (CE) nº 2007/2006 de la Comisión sobre la importación y el tránsito de determinados productos intermedios derivados de material de la categoría 3 [49].
(45) Asimismo, se han adoptado medidas transitorias proporcionales al riesgo que entrañan algunos usos específicos de subproductos animales, en concreto el Reglamento (CE) nº 878/2004 relativo a la importación y manipulación de determinados materiales de la categoría 1 y de la categoría 2 [50], la Decisión 2004/407/CE con respecto a la importación de gelatina fotográfica [51] y el Reglamento (CE) nº 197/2006 relativo a la manipulación y eliminación de antiguos alimentos [52].
(46) Con el fin de simplificar aún más las normas de la Unión sobre subproductos animales, como había solicitado la Presidencia del Consejo al adoptar el Reglamento (CE) nº 1069/2009, se han revisado dichas medidas transitorias y actos de aplicación. Ahora deben ser derogados y sustituidos, según proceda, por el presente Reglamento, para que exista un marco jurídico coherente en materia de subproductos animales y productos derivados.
(47) El Reglamento (CE) nº 1069/2009 será de aplicación el 4 de marzo de 2011, por lo que es necesario disponer que el presente Reglamento lo sea también a partir de esa fecha. Asimismo, conviene prever un período transitorio, durante el cual se permita a las partes interesadas adaptarse a las nuevas normas dispuestas en el presente Reglamento e introducir en el mercado ciertos productos fabricados con arreglo a las normas sanitarias de la Unión aplicables antes de dicha fecha, y permitir la continuación de las importaciones una vez los requisitos del presente Reglamento sean de aplicación.
(48) La introducción en el mercado y exportación de determinados productos contemplados en el Reglamento (CE) nº 878/2004 debe continuar realizándose de conformidad con las medidas nacionales, ya que los riesgos asociados a las pequeñas cantidades de materiales afectados actualmente permiten su regulación a escala nacional, a la espera de una posible armonización en el futuro. Mientras no se adopten medidas para la recogida y eliminación de ciertas pequeñas cantidades de productos de origen animal del sector minorista, basándose en nuevos datos, la autoridad competente debería continuar pudiendo autorizar la recogida y eliminación de dichos productos por otros medios, a condición de que se garantice una protección equivalente de la salud pública y la salud animal.
(49) Siguiendo el deseo expresado por el Parlamento Europeo al dar su acuerdo al Reglamento (CE) nº 1069/2009 en primera lectura, y tomando en cuenta sus sugerencias más específicas para abordar ciertas cuestiones de carácter técnico, el presente proyecto de Reglamento ha sido presentado a debate a su Comisión de Medio Ambiente, Salud Pública y Seguridad Alimentaria el día 27 de septiembre de 2010.
(50) Las medidas previstas en el presente Reglamento se ajustan al dictamen del Comité Permanente de la Cadena Alimentaria y de Sanidad Animal.
HA ADOPTADO EL PRESENTE REGLAMENTO:
Objeto y ámbito de aplicación
El presente Reglamento establece las medidas de aplicación:
a) de las normas de salud pública y de salud animal aplicables a los subproductos animales y los productos derivados dispuestas en el Reglamento (CE) nº 1069/2009;
b) relativas a determinadas muestras y artículos exentos de los controles veterinarios en los puestos de inspección fronterizos conforme se define en el artículo 16, apartado 1, letras e) y f), de la Directiva 97/78/CE.
Definiciones
A efectos del presente Reglamento, se aplicarán las definiciones recogidas en el anexo I.
Punto final en la cadena de fabricación de ciertos productos derivados
Los siguientes productos derivados podrán introducirse en el mercado, salvo por importación, sin restricciones, a tenor de lo dispuesto en el artículo 5, apartado 2, del Reglamento (CE) nº 1069/2009:
a) el biodiésel que satisfaga los requisitos para la eliminación y el uso de productos derivados establecidos en el punto 2, letra b), de la sección 3 del capítulo IV del anexo IV;
b) los alimentos transformados para animales de compañía que cumplan las condiciones específicas para dichos productos definidas en el punto 7, letra a), del capítulo II del anexo XIII;
c) los accesorios masticables para perros que cumplan las condiciones específicas para dichos productos definidas en el punto 7, letra b), del capítulo II del anexo XIII;
d) las pieles de ungulados que cumplan las condiciones específicas aplicables al punto final de dichos productos definidas en la letra C del capítulo V del anexo XIII;
e) la lana y el pelo que cumplan las condiciones específicas aplicables al punto final de dichos productos definidas en la letra B del capítulo V del anexo XIII;
f) las plumas y el plumón que cumplan las condiciones específicas aplicables al punto final de dichos productos definidas en la letra C del capítulo V del anexo XIII;
g) las pieles de peletería que cumplan las condiciones definidas en el capítulo VIII del anexo XIII.
Enfermedades transmisibles graves
Las enfermedades recogidas por la OIE en el artículo 1.2.3 del Código Sanitario para los Animales Terrestres, edición de 2010, y en el capítulo 1.3 del Código Sanitario para los Animales Acuáticos, edición de 2010, serán consideradas enfermedades transmisibles graves a los efectos de las restricciones generales sobre salud animal, con arreglo a lo dispuesto en el artículo 6, apartado 1, letra b), inciso ii), del Reglamento (CE) nº 1069/2009.
Restricciones del uso de subproductos animales y productos derivados
1. En los Estados miembros a los que hace referencia el capítulo I del anexo II, los operadores cumplirán las condiciones de alimentación de animales de peletería con ciertos materiales derivados de cuerpos o partes de animales de la misma especie establecidas en dicho capítulo.
2. Los operadores respetarán las restricciones relativas a la alimentación de animales de granja con pasto de tierras abonadas con abonos y enmiendas del suelo de origen orgánico establecidas en el capítulo II del anexo II.
Eliminación por incineración y coincineración
1. La autoridad competente garantizará que la incineración y coincineración de subproductos animales y productos derivados solo tendrá lugar:
a) en las plantas de incineración o coincineración que hayan recibido una autorización de explotación de conformidad con la Directiva 2000/76/CE, o
b) en el caso de plantas que no estén obligadas a contar con autorización de conformidad con la Directiva 2000/76/CE, en las plantas de incineración y coincineración que hayan recibido una autorización de la autoridad competente para eliminar por incineración, o para eliminar o recuperar subproductos animales o productos derivados, cuando se trate de residuos, por coincineración, de conformidad con lo dispuesto en el artículo 24, apartado 1, letras b) o c), del Reglamento (CE) nº 1069/2009.
2. La autoridad competente solo autorizará las plantas de incineración y coincineración mencionadas en el punto 1, letra b), de conformidad con el artículo 24, apartado 1, letras b) o c), del Reglamento (CE) nº 1069/2009, si cumplen las condiciones establecidas en el anexo III del presente Reglamento.
3. Los explotadores de plantas de incineración y coincineración cumplirán las condiciones generales en materia de incineración y coincineración establecidas en el capítulo I del anexo III.
4. Los explotadores de las plantas de incineración y coincineración de gran capacidad cumplirán las condiciones que figuran en el capítulo II del anexo III.
5. Los explotadores de las plantas de incineración y coincineración de baja capacidad cumplirán las condiciones que figuran en el capítulo III del anexo III.
Eliminación en vertedero de determinados materiales de las categorías 1 y 3
No obstante lo dispuesto en el artículo 12 y en el artículo 14, letra c), del Reglamento (CE) nº 1069/2009, la autoridad competente podrá autorizar la eliminación de los siguientes materiales de las categorías 1 y 3 en un vertedero autorizado:
a) los alimentos para animales de compañía importados o producidos a partir de materiales importados, de materiales de la categoría 1 a los que hace referencia el artículo 8, letra c), del Reglamento (CE) nº 1069/2009;
b) los materiales de la categoría 3 recogidos en el artículo 10, letras f) y g), del Reglamento (CE) nº 1069/2009, a condición de que:
i) dichos materiales no hayan entrado en contacto con ningún subproducto animal contemplado en los artículos 8 y 9 y en el artículo 10, letras a) a e) y h) a p), de dicho Reglamento;
ii) cuando sean destinados a la eliminación, los materiales:
- contemplados en el artículo 10, letra f), de dicho Reglamento hayan sido transformados con arreglo a lo dispuesto en el artículo 2, apartado 1, letra m), del Reglamento (CE) nº 852/2004, y
- contemplados en el artículo 10, letra g), de dicho Reglamento hayan sido transformados con arreglo a lo dispuesto en el capítulo II del anexo X del presente Reglamento, o de conformidad con las condiciones específicas para alimentos para animales de compañía establecidas en el capítulo II del anexo XIII del presente Reglamento, y
iii) la eliminación de dichos materiales no entrañe riesgo alguno para la salud pública o animal.
Condiciones de las plantas de transformación y otros establecimientos
1. Los explotadores garantizarán que las plantas de transformación y otros establecimientos a su cargo cumplen los siguientes requisitos definidos en el capítulo I del anexo IV:
a) las condiciones generales para la transformación establecidas en la sección 1;
b) las condiciones de tratamiento de aguas residuales establecidas en la sección 2;
c) las condiciones específicas para la transformación de materiales de las categorías 1 y 2 establecidas en la sección 3;
d) las condiciones específicas para la transformación de materiales de la categoría 3 establecidas en la sección 4.
2. La autoridad competente únicamente autorizará plantas de transformación y otros establecimientos que cumplan las condiciones definidas en el capítulo I del anexo IV.
Condiciones de higiene y transformación para plantas de transformación y otros establecimientos
Los explotadores garantizarán que los establecimientos y plantas a su cargo cumplen los siguientes requisitos definidos en el anexo IV:
a) las condiciones de higiene y transformación establecidas en el capítulo II;
b) los métodos estándar de transformación establecidos en el capítulo III, si se utilizan tales métodos en la planta o establecimiento;
c) los métodos alternativos de transformación establecidos en el capítulo IV, si se utilizan tales métodos en la planta o establecimiento.
Condiciones sobre la transformación de subproductos animales y productos derivados en biogás y compost
1. Los explotadores garantizarán que los establecimientos y plantas a su cargo cumplen las condiciones siguientes sobre la transformación de subproductos animales y productos derivados en biogás y compost que se definen en el anexo V:
a) las condiciones aplicables a las plantas de biogás y compostaje definidas en el capítulo I;
b) las condiciones de higiene aplicables a las plantas de biogás y compostaje definidas en el capítulo II;
c) los parámetros de transformación estándar definidos en la sección 1 del capítulo III;
d) las normas sobre residuos de fermentación y compost definidos en la sección 3 del capítulo III.
2. La autoridad competente únicamente autorizará plantas de biogás y compostaje que cumplan las condiciones definidas en el anexo V:
3. La autoridad competente podrá autorizar el uso de parámetros alternativos de transformación para plantas de biogás y compostaje si se cumplen los requisitos definidos en la sección 2 del capítulo III del anexo V.
Normas especiales aplicables a las muestras para diagnóstico e investigación
1. La autoridad competente podrá autorizar el transporte, uso y eliminación de muestras para diagnóstico e investigación en condiciones que garanticen el control de los riesgos para la salud pública y la salud animal.
En particular, la autoridad competente garantizará que los explotadores cumplen los requisitos establecidos en el capítulo I del anexo VI.
2. Los explotadores cumplirán las normas especiales aplicables a las muestras para diagnóstico e investigación definidas en el capítulo I del anexo VI.
3. Los explotadores podrán enviar muestras para diagnóstico e investigación que consistan en los siguientes subproductos animales y productos derivados a otro Estado miembro sin la previa información a la autoridad competente del Estado miembro de origen en virtud del artículo 48, apartado 1, del Reglamento (CE) nº 1069/2009 y sin la previa información a la autoridad competente del Estado miembro de destino por medio del sistema TRACES ni su conformidad de aceptación del envío con arreglo a lo dispuesto en el artículo 48, apartados 1 y 3 de dicho Reglamento:
a) los materiales de las categorías 1 y 2 y la harina de carne y huesos o las grasas animales derivadas de materiales de las categorías 1 y 2;
b) la proteína animal transformada.
Normas especiales relativas a las muestras comerciales y los artículos de exposición
1. La autoridad competente podrá autorizar el transporte, uso y eliminación de muestras comerciales y artículos de exposición en condiciones que garanticen el control de los riesgos para la salud pública y la salud animal.
En particular, la autoridad competente garantizará que los explotadores cumplen las condiciones establecidas en los puntos 2, 3 y 4 de la sección 1 del capítulo I del anexo VI.
2. Los explotadores cumplirán las normas especiales aplicables a las muestras comerciales y artículos de exposición definidas en la sección 2 del capítulo I del anexo VI.
3. Los explotadores podrán enviar muestras comerciales que consistan en los siguientes subproductos animales y productos derivados a otro Estado miembro sin la previa información a la autoridad competente del Estado miembro de origen en virtud del artículo 48, apartado 1, del Reglamento (CE) nº 1069/2009 y sin la previa información a la autoridad competente del Estado miembro de destino por medio del sistema TRACES ni su conformidad de aceptación del envío con arreglo a lo dispuesto en el artículo 48, apartados 1 y 3 de dicho Reglamento:
a) los materiales de las categorías 1 y 2 y la harina de carne y huesos o las grasas animales derivadas de materiales de las categorías 1 y 2;
b) la proteína animal transformada.
Normas especiales de alimentación animal
1. Los explotadores podrán alimentar a los siguientes animales con material de la categoría 2, siempre que proceda de animales que no hayan sido sacrificados ni hayan muerto como consecuencia de la presencia real o sospechada de una enfermedad transmisible al ser humano o a los animales, con arreglo a las condiciones generales establecidas en la sección 1 del capítulo II del anexo VI y cualquier otra condición que pueda establecer la autoridad competente:
a) los animales de zoológico;
b) los animales de peletería;
c) los perros procedentes de perreras o jaurías reconocidas;
d) los perros y gatos en refugios;
e) los gusanos y lombrices para cebos.
2. Los explotadores podrán alimentar a los siguientes animales con material de la categoría 3, con arreglo a las condiciones generales establecidas en la sección 1 del capítulo II del anexo VI y cualquier otra condición que pueda establecer la autoridad competente:
a) los animales de zoológico;
b) los animales de peletería;
c) los perros procedentes de perreras o jaurías reconocidas;
d) los perros y gatos en refugios;
e) los gusanos y lombrices para cebos.
Alimentación de determinadas especies dentro y fuera de comederos de animales y en zoológicos
1. La autoridad competente podrá autorizar el uso de material de la categoría 1 consistente en cuerpos enteros o partes de animales muertos que contengan material especificado de riesgo para la alimentación:
a) en comederos, de animales pertenecientes a especies en peligro o protegidas de aves necrófagas y otras especies que vivan en su hábitat natural, en aras del fomento de la biodiversidad, con arreglo a las condiciones establecidas en la sección 2 del capítulo II del anexo VI;
b) fuera de comederos, si procede sin la previa recogida de los animales muertos, de los animales silvestres a los que hace referencia el punto 1, letra a), del capítulo II del anexo VI, con arreglo a las condiciones establecidas en la sección 3 de dicho capítulo.
2. La autoridad competente podrá autorizar el uso de material de la categoría 1 consistente en cuerpos enteros o partes de animales muertos que contengan material especificado de riesgo y el uso de material derivado de animales de zoológico, para la alimentación de animales de zoológico con arreglo a las condiciones establecidas en la sección 4 del capítulo II del anexo VI.
Normas especiales sobre recogida y eliminación
Si la autoridad competente autoriza la eliminación de subproductos animales de acuerdo con las excepciones previstas en el artículo 19, apartado 1, letras a), b), c) y e), del Reglamento (CE) nº 1069/2009, la eliminación deberá cumplir las siguientes normas especiales definidas en el capítulo III del anexo VI:
a) las normas especiales de eliminación de subproductos animales establecidas en la sección 1;
b) las normas relativas a la incineración y enterramiento de subproductos animales en zonas remotas establecidas en la sección 2;
c) las normas relativas a la incineración y enterramiento de abejas y subproductos de la apicultura establecidas en la sección 3;
Modelo estándar de solicitud de autorización de métodos alternativos
1. Las solicitudes de autorización de un método alternativo de uso o eliminación de subproductos o productos derivados, a las que se hace referencia en el artículo 20, apartado 1, del Reglamento (CE) nº 1069/2009, serán presentadas por los Estados miembros o partes interesadas de conformidad con las condiciones del modelo estándar de solicitud de autorización de métodos alternativos establecido en el anexo VII.
2. Los Estados miembros designarán puntos nacionales de contacto para ofrecer información sobre la autoridad competente responsable de la evaluación de solicitudes de autorización de un método alternativo de uso o eliminación de subproductos animales.
3. La Comisión publicará una lista de puntos nacionales de contacto en su sitio web.
Condiciones relativas a documentos comerciales y certificados sanitarios, identificación, recogida y transporte de subproductos animales y trazabilidad
1. Los explotadores garantizarán que los subproductos animales y productos derivados:
a) cumplen las condiciones para la recogida, el transporte y la identificación establecidas en los capítulos I y II del anexo VIII;
b) van acompañados durante su transporte de documentos comerciales o certificados sanitarios con arreglo a las condiciones establecidas en el capítulo III del anexo VIII.
2. Los explotadores encargados de la expedición, transporte o recepción de subproductos animales o productos derivados llevarán un registro de los envíos y de los respectivos documentos comerciales o certificados sanitarios con arreglo a los requisitos establecidos en el capítulo IV del anexo VIII.
3. Los operadores cumplirán los requisitos sobre el marcado de determinados productos derivados establecidos en el capítulo V del anexo VIII.
Condiciones para la autorización en el mismo emplazamiento de uno o más establecimientos o plantas para la manipulación de subproductos animales
La autoridad competente podrá autorizar la existencia en el mismo emplazamiento de uno o más establecimientos o plantas para la manipulación de subproductos animales, a condición de que se impida la transmisión de riesgos para la salud pública y animal entre los establecimientos o plantas gracias a su diseño y a su modo de manipulación de subproductos animales y productos derivados.
Condiciones sobre determinados establecimientos y plantas autorizados para la manipulación de subproductos animales y productos derivados
Los explotadores garantizarán que los establecimientos y plantas a su cargo que hayan sido autorizados por la autoridad competente cumplan las condiciones establecidas en los capítulos siguientes del anexo IX del presente Reglamento cuando lleven a cabo al menos una de las siguientes actividades contempladas en el artículo 24, apartado 1, del Reglamento (CE) nº 1069/2009:
a) el capítulo I, si fabrican alimentos para animales de compañía recogidos en el artículo 24, apartado 1, letra e) de dicho Reglamento;
b) el capítulo II, si almacenan subproductos animales recogidos en el artículo 24, apartado 1, letra i) de dicho Reglamento, y si manipulan subproductos animales tras su recogida, mediante las siguientes actividades mencionadas en el artículo 24, apartado 1, letra h) de dicho Reglamento:
i) clasificación;
ii) corte;
iii) refrigeración;
iv) congelación;
v) salazón;
vi) conservación por otros procesos;
vii) separación de las pieles o de material especificado de riesgo;
viii) operaciones de manipulación de subproductos animales realizadas de conformidad con las obligaciones de la legislación veterinaria de la Unión;
ix) higienización/pasteurización de los subproductos animales destinados a su transformación en biogás o compostaje previamente a dicha transformación o compostaje en otro establecimiento o planta de conformidad con lo dispuesto en el anexo V del presente Reglamento;
x) cribado;
c) el capítulo III, si almacenan productos derivados para ciertos fines previstos recogidos en el artículo 24, apartado 1, letra j), de dicho Reglamento.
Condiciones sobre determinados establecimientos y plantas autorizados para la manipulación de subproductos animales y productos derivados
1. Los explotadores de plantas o establecimientos registrados u otros explotadores registrados manipularán los subproductos animales y productos derivados con arreglo a las condiciones establecidas en el capítulo IV del anexo IX.
2. Los explotadores registrados que transporten subproductos animales o productos derivados, salvo entre las instalaciones del mismo explotador, cumplirán en concreto las condiciones establecidas en el punto 2 del capítulo IV del anexo IX.
3. Las disposiciones de los apartados 1 y 2 no se aplicarán:
a) a los explotadores autorizados que transporten subproductos animales o productos derivados como actividad auxiliar;
b) a los explotadores que hayan sido registrados para realizar actividades de transporte conforme al Reglamento (CE) nº 183/2005.
4. La autoridad competente podrá eximir a los siguientes explotadores de la notificación obligatoria a la que se refiere el artículo 23, apartado 1, letra a), del Reglamento (CE) nº 1069/2009:
a) los explotadores que manipulen o elaboren trofeos de caza u otros preparados mencionados en el capítulo VI del anexo XIII del presente Reglamento con fines privados o no comerciales;
b) los explotadores que manipulen o eliminen muestras para diagnóstico e investigación con fines educativos.
Tratamiento e introducción en el mercado de subproductos animales y productos derivados para la alimentación de animales de granja, salvo animales de peletería
1. Los explotadores cumplirán las siguientes condiciones aplicables a la introducción en el mercado, salvo importación, de subproductos animales y productos derivados destinados a la alimentación de animales de granja excepto los de peletería, conforme a lo previsto en el artículo 31, apartado 2, del Reglamento (CE) nº 1069/2009, establecidas en el anexo X del presente Reglamento.
a) las condiciones generales para la transformación e introducción en el mercado establecidas en el capítulo I;
b) las condiciones específicas para la transformación de proteína animal y otros productos derivados establecidas en el capítulo II;
c) las condiciones para determinados piensos para peces y cebos de pesca establecidas en el capítulo III.
2. La autoridad competente podrá autorizar la introducción en el mercado, salvo importación, de leche, productos lácteos y productos derivados de la leche catalogados como material de la categoría 3 de acuerdo con el artículo 10, letras e), f) y h), del Reglamento (CE) nº 1069/2009 y que no hayan sido transformados de conformidad con las condiciones generales definidas en la parte I de la sección 4 del capítulo II del anexo X del presente Reglamento, a condición de que dichos materiales cumplan las condiciones de exención aplicables a la introducción en el mercado de leche transformada de conformidad con las normas nacionales establecidas en la parte II de la misma sección.
Introducción en el mercado y uso de abonos y enmiendas del suelo de origen orgánico
1. Los explotadores cumplirán las condiciones relativas a la introducción en el mercado, salvo importación, de abonos y enmiendas del suelo de origen orgánico, así como al uso de tales productos, en particular su aplicación a la tierra, de conformidad con lo dispuesto en el artículo 15, apartado 1, letra i), y el artículo 32, apartado 1, del Reglamento (CE) nº 1069/2009, establecidas en el anexo XI del presente reglamento.
2. La introducción en el mercado, incluida la importación, del guano de aves marinas silvestres no estará sujeta a ninguna condición zoosanitaria.
3. La autoridad competente del Estado miembro en el cual se aplicará a la tierra un abono o enmienda de suelo de origen orgánico producido a partir de harina de huesos y carne derivada de material de la categoría 2 o de proteína animal transformada, autorizará uno o más ingredientes que tendrán que mezclarse con dichos materiales, de conformidad con el artículo 32, apartado 1, letra d), del Reglamento (CE) nº 1069/2009, conforme a los criterios establecidos en el punto 3 de la sección 1 del capítulo II del anexo XI del presente Reglamento.
4. No obstante lo dispuesto en el artículo 48, apartado 1), del Reglamento (CE) nº 1069/2009, las autoridades competentes de un Estado miembro de origen y un Estado miembro de destino que compartan frontera, podrán autorizar el envío de estiércol entre granjas situadas en las regiones fronterizas de los dos Estados miembros cumpliendo las condiciones adecuadas de control de cualquier posible riesgo para la salud pública o animal, como las obligaciones impuestas a los explotadores afectados de mantener los registros adecuados, establecidas en un acuerdo bilateral.
5. Según lo dispuesto en el artículo 30, apartado 1, del Reglamento (CE) nº 1069/2009, la autoridad competente del Estado miembro fomentará, cuando sea necesario, el desarrollo, difusión y uso de guías nacionales de buenas prácticas agrícolas para la aplicación de abonos y enmiendas del suelo de origen orgánico a la tierra.
Productos intermedios
1. Los productos intermedios, importados en la Unión o que transitan por ella, deberán cumplir las condiciones para el control de los riesgos para la salud pública o animal mencionados en el anexo XII del presente Reglamento.
2. Los productos intermedios que hayan sido transportados a un establecimiento o planta descritos en el punto 3 del anexo XII, podrán manipularse sin restricciones adicionales de conformidad con lo dispuesto en el Reglamento (CE) nº 1069/2009 y en el presente, siempre que:
a) el establecimiento o planta disponga de instalaciones adecuadas para la recepción de productos intermedios, que impidan la propagación de enfermedades transmisibles a personas o animales;
b) los productos intermedios no planteen riesgos de transmisión de enfermedades transmisibles a personas o animales, gracias a su purificación o a otros tratamientos a los cuales se hayan sometido los subproductos animales presentes en el producto intermedio, gracias a la concentración de subproductos animales en el producto intermedio o gracias a las medidas de bioseguridad adoptadas en la manipulación de los productos intermedios;
c) el establecimiento o planta lleve registros de la cantidad de materiales recibida, su categoría, si procede, y el establecimiento, planta o explotador a los que ha suministrado sus productos, y
d) los productos intermedios no utilizados u otros materiales sobrantes del establecimiento o plantas, como productos caducados, sean eliminados de conformidad con lo dispuesto en el Reglamento (CE) nº 1069/2009.
3. El explotador o propietario del establecimiento o planta de destino de los productos intermedios o su representante utilizará o expedirá los productos intermedios únicamente para su posterior mezcla, recubrimiento, montaje, embalaje o etiquetado.
Alimentos para animales de compañía y productos derivados
1. Estará prohibido el uso de material de la categoría 1 mencionado en el artículo 8, letras a), b), d) y e), del Reglamento (CE) nº 1069/2009 para la fabricación de productos derivados destinados a ser ingeridos por humanos o animales o a ser aplicados sobre los mismos, distintos de los productos derivados mencionados en los artículos 33 y 36 de dicho Reglamento.
2. Cuando un subproducto animal o un producto derivado pueda emplearse para la alimentación de animales de granja o para otros fines mencionados en el artículo 36, letra a), del Reglamento (CE) nº 1069/2009, se introducirán en el mercado, salvo importación, de conformidad con las condiciones específicas para proteína animal transformada y otros productos derivados definidas en el capítulo II del anexo X del presente Reglamento, siempre que el anexo XIII del presente Reglamento no disponga ninguna condición específica para tales productos.
3. Los explotadores cumplirán las condiciones para la introducción en el mercado, salvo importación, de alimentos para animales de compañía, mencionadas en el artículo 40 del Reglamento (CE) nº 1069/2009 y establecidas en los capítulos I y II del anexo XIII del presente Reglamento.
4. Los explotadores cumplirán las condiciones para la introducción en el mercado, salvo importación, de productos derivados, mencionadas en el artículo 40 del Reglamento (CE) nº 1069/2009 y establecidas en el capítulo I y en los capítulos III a XII del anexo XIII del presente Reglamento.
Importación, tránsito y exportación de subproductos animales y productos derivados
1. La importación a la Unión y el tránsito por la misma de los siguientes subproductos animales estarán prohibidos:
a) el estiércol sin transformar;
b) las plumas, partes de plumas y plumón sin transformar;
c) la cera en forma de panal.
2. La importación a la Unión y el tránsito por la misma de los siguientes subproductos animales no estarán sujetos a requisitos zoosanitarios:
a) la lana y el pelo que hayan sido lavados en fábrica o que hayan sido tratados con otro método que garantice la eliminación de riesgos inaceptables;
b) las pieles que hayan sido secadas a temperatura ambiente de 18 °C durante un período mínimo de dos días con una humedad del 55 %.
3. Los explotadores cumplirán las siguientes condiciones específicas relativas a la importación a la Unión y al tránsito por la misma de determinados subproductos animales y de productos derivados, contempladas en el artículo 41, apartado 3, y en el artículo 42 del Reglamento (CE) nº 1069/2009 y establecidas en el anexo XIV del presente Reglamento.
a) las condiciones específicas para la importación y el tránsito de material de la categoría 3 y productos derivados para usos en la cadena alimentaria animal, distintos de los alimentos para animales de compañía o de piensos para animales de peletería, establecidas en el capítulo I de dicho anexo;
b) las condiciones específicas para la importación y el tránsito de subproductos derivados con fines externos a la cadena alimentaria de animales de granja, establecidas en el capítulo II de dicho anexo.
Introducción en el mercado, importación y exportación de determinados materiales de la categoría 1
La autoridad competente podrá autorizar la introducción en el mercado, incluida la importación y exportación de pieles derivadas de animales que hayan sido sometidos a un tratamiento ilegal, tal como se define en el artículo 1, apartado 2, letra d), de la Directiva 96/22/CE o en el artículo 2, letra b), de la Directiva 96/23/CE, y de intestinos de rumiantes con o sin contenido, y de huesos y productos derivados de huesos que contengan columna vertebral y cráneo, a condición de que se cumplan las siguientes condiciones:
a) dichos materiales no deberán ser materiales de la categoría 1 derivados de los siguientes animales:
i) los animales sospechosos de estar infectados por una EET de acuerdo con el Reglamento (CE) nº 999/2001;
ii) los animales en los que se haya confirmado oficialmente la presencia de una EET;
iii) los animales sacrificados en aplicación de medidas de erradicación de EET;
b) dichos materiales no deberán destinarse a ninguno de los siguientes usos:
i) alimentación animal;
ii) la aplicación a tierras de las que se alimentan animales de granja;
iii) la fabricación de:
- productos cosméticos, tal como se definen en el artículo 1, apartado 1, de la Directiva 76/768/CEE;
- productos sanitarios implantables activos, tal como se definen en el artículo 1, apartado 2, letra c), de la Directiva 90/385/CEE;
- productos sanitarios, tal como se definen en el artículo 1, apartado 2, letra a), de la Directiva 93/42/CEE;
- productos sanitarios para diagnóstico in vitro, tal como se definen en el artículo 1, apartado 2, letra b), de la Directiva 98/79/CE;
- medicamentos veterinarios, tal como se definen en el artículo 1, apartado 2, de la Directiva 2001/82/CE;
- medicamentos, tal como se definen en el artículo 1, apartado 2, de la Directiva 2001/83/CE;
c) los materiales deberán importarse etiquetados y deberán cumplir las condiciones específicas para determinados desplazamientos de subproductos animales definidas en la sección 1 del capítulo IV del anexo XIV del presente documento;
d) los materiales deberán importarse con arreglo a las condiciones de certificación sanitaria establecidas en la legislación nacional.
Importación y tránsito de muestras para investigación y diagnóstico
1. La autoridad competente podrá autorizar la importación y el tránsito de muestras para diagnóstico e investigación, compuestas por productos derivados o subproductos animales, incluidos los que se mencionan en el artículo 25, apartado 1, en condiciones que garanticen el control de los riesgos para la salud pública y animal.
Dichas condiciones incluirán, como mínimo, lo siguiente:
a) la introducción de la partida deberá haber sido autorizada previamente por la autoridad competente del Estado miembro de destino, y
b) la partida deberá remitirse directamente desde el punto de entrada en la Unión al usuario autorizado.
2. Los explotadores presentarán las muestras para diagnóstico e investigación que pretendan importar a través de un Estado miembro distinto del Estado miembro de destino, en un puesto de inspección fronterizo autorizado de la Unión mencionado en el anexo I de la Decisión 2009/81/CE. En el puesto de inspección fronterizo, dichas muestras para diagnóstico e investigación no serán sometidas a controles veterinarios de conformidad con lo dispuesto en el capítulo I de la Directiva 97/78/CE. La autoridad competente del puesto de inspección fronteriza informará a la autoridad competente del Estado miembro de destino al respecto de la introducción de las muestras para diagnóstico e investigación por medio del sistema TRACES.
3. Los explotadores que manipulen muestras para diagnóstico e investigación cumplirán las condiciones especiales de eliminación de muestras para diagnóstico e investigación establecidas en la sección 1 del capítulo III del anexo XIV del presente Reglamento.
Importación y tránsito de muestras comerciales y artículos de exposición
1. La autoridad competente podrá autorizar la importación y el tránsito de muestras comerciales de conformidad con las normas especiales establecidas en el punto 1 de la sección 2 del capítulo III del anexo XIV del presente Reglamento.
2. Los explotadores que manipulen muestras comerciales cumplirán las normas especiales de manipulación y eliminación de muestras comerciales establecidas en los puntos 2 y 3 de la sección 2 del capítulo III del anexo XIV del presente Reglamento.
3. La autoridad competente podrá autorizar la importación y el tránsito de artículos de exposición de conformidad con las normas especiales establecidas en la sección 3 del capítulo III del anexo XIV del presente Reglamento.
4. Los explotadores que manipulen artículos de exposición cumplirán las condiciones de embalaje, manipulación y eliminación de artículos de exposición establecidas en la sección 3 del capítulo III del anexo XIV del presente Reglamento.
Condiciones específicas para el tránsito de determinados subproductos animales entre territorios de la Federación Rusa
1. La autoridad competente autorizará el tránsito a través de la Unión de determinadas partidas de subproductos animales procedentes y destinadas a la Federación Rusa, directamente o a través de un tercer país, por ferrocarril o carretera, entre puestos de inspección fronterizos autorizados de la Unión mencionados en el anexo I de la Decisión 2009/821/CE, siempre que se cumplan las siguientes condiciones:
a) la partida será precintada por los servicios veterinarios de la autoridad competente con un precinto numerado (número de serie) en el puesto de inspección fronterizo de entrada en la Unión;
b) los documentos que acompañen a la partida previstos en el artículo 7 de la Directiva 97/78/CE llevarán en cada página un sello con la inscripción "SOLO PARA TRÁNSITO POR LA UE CON DESTINO A RUSIA", estampado por el veterinario oficial de la autoridad competente responsable del puesto de inspección fronterizo;
c) deberán cumplirse los requisitos procedimentales establecidos en el artículo 11 de la Directiva 97/78/CE;
d) el veterinario oficial del puesto de inspección fronterizo de entrada habrá certificado la partida como aceptable para el tránsito en el documento veterinario común de entrada previsto en el anexo III del Reglamento (CE) nº 136/2004.
2. No se autorizará la descarga o el almacenamiento, a tenor del artículo 12, apartado 4, o del artículo 13 de la Directiva 97/78/CE, de dichas partidas en el territorio de ningún Estado miembro.
3. La autoridad competente realizará periódicamente auditorías para verificar que el número de partidas y las cantidades de los productos que salen del territorio de la Unión corresponden al número y las cantidades introducidas en el mismo.
Listas de establecimientos y plantas de terceros países
Las listas de establecimientos y plantas de terceros países se introducirán en el sistema Traces de conformidad con las especificaciones técnicas publicadas por la Comisión en su sitio web.
Cada lista se actualizará periódicamente.
Modelos de certificados sanitarios y declaraciones para la importación y el tránsito
Las partidas de subproductos animales y productos derivados para la importación a la Unión o el tránsito por la misma irán acompañadas en el punto de entrada en la Unión donde se realicen los controles veterinarios, de certificados sanitarios y declaraciones, conforme a los modelos establecidos en el anexo XV del presente Reglamento, según dispone la Directiva 97/78/CE.
Controles oficiales
1. La autoridad competente adoptará las medidas necesarias para controlar en su integridad la cadena de recogida, transporte, uso y eliminación de subproductos animales y productos derivados, de conformidad con el artículo 4, apartado 2, del Reglamento (CE) nº 1069/2009.
Dichas medidas se llevarán a cabo de conformidad con los principios aplicables a los controles oficiales establecidos en el artículo 3 del Reglamento (CE) nº 882/2004.
2. Los controles oficiales a los que se refiere el apartado 1 incluirán controles sobre el mantenimiento de registros y otros documentos exigidos en aplicación de las normas establecidas en el presente Reglamento.
3. La autoridad competente realizará los siguientes controles oficiales, según lo dispuesto en el artículo 45, apartado 1, del Reglamento (CE) nº 1069/2009, con arreglo a las condiciones establecidas en el anexo XVI del presente Reglamento:
a) controles oficiales en las plantas de transformación dispuestos en el capítulo I;
b) controles oficiales de otras actividades que impliquen la manipulación de subproductos animales, y productos derivados dispuestos en las secciones 1 a 9 del capítulo III.
4. La autoridad competente realizará controles de los precintos aplicados a los envíos de subproductos animales o productos derivados.
Cuando la autoridad competente precinte un envío transportado a un lugar de destino, deberá informar de ello a la autoridad del lugar de destino.
5. La autoridad competente elaborará las listas de establecimientos, plantas y explotadores mencionadas en el artículo 47, apartado 1, del Reglamento (CE) nº 1069/2009 conforme al modelo establecido en el capítulo II del anexo XVI del presente Reglamento.
6. La autoridad competente del Estado miembro de destino adoptará una decisión sobre la solicitud por parte de un explotador en lo que respecta a la aceptación o rechazo de determinados materiales de la categoría 1, de la categoría 2 y harina de huesos y carne o grasa animal derivada de materiales de las categorías 1 y 2, en un plazo de 20 días desde la fecha de recepción de la solicitud, a condición de que se haya presentado en una lengua oficial del Estado miembro en cuestión.
7. Los explotadores enviarán una solicitud para recibir la autorización aludida en el apartado 6 con arreglo al modelo estándar establecido en la sección 10 del capítulo III del anexo XVI del presente Reglamento.
Renovación de la autorización de plantas y establecimientos tras la concesión de una autorización temporal
1. Cuando una planta o establecimiento autorizados para la transformación de material de la categoría 3 recibe posteriormente autorización provisional para la transformación de material de las categorías 1 o 2, de conformidad con el artículo 24, apartado 2, letra b), inciso ii), del Reglamento (CE) nº 1069/2009, tendrá prohibido reiniciar las actividades de la transformación de material de la categoría 3 sin haber obtenido previamente la autorización de la autoridad competente para reiniciar las actividades de transformación de material de la categoría 3 conforme a lo dispuesto en el artículo 44 de dicho Reglamento.
2. Cuando una planta o establecimiento autorizados para la transformación de material de la categoría 2 recibe posteriormente autorización provisional para la transformación de material de la categoría 1, de conformidad con el artículo 24, apartado 2, letra b), inciso ii), del Reglamento (CE) nº 1069/2009, tendrá prohibido reiniciar las actividades de transformación de material de la categoría 2 sin haber obtenido previamente la autorización de la autoridad competente para reiniciar las actividades de transformación de material de la categoría 2 conforme a lo dispuesto en el artículo 44 de dicho Reglamento.
Restricciones sobre la introducción en el mercado de determinados subproductos animales y productos derivados por motivos de salud pública y animal
La autoridad competente no prohibirá ni restringirá la introducción en el mercado de los siguientes subproductos animales y productos derivados por motivos de salud pública o animal distintos de las normas dispuestas en la legislación de la Unión, y en concreto las dispuestas en el Reglamento (CE) nº 1069/2009 y en el presente Reglamento:
a) proteína animal transformada y otros productos derivados contemplados en el capítulo II del anexo X del presente Reglamento;
b) alimentos para animales de compañía y otros productos derivados determinados contemplados en el anexo XIII del presente Reglamento;
c) subproductos animales y productos derivados importados en la Unión o que transitan por ella contemplados en el anexo XIV del presente Reglamento.
Derogación
1. Quedan derogados los siguientes actos:
a) Reglamento (CE) nº 811/2003;
b) Decisión 2003/322/CE;
c) Decisión 2003/324/CE;
d) Reglamento (CE) nº 878/2004;
e) Decisión 2004/407/CE;
f) Reglamento (CE) nº 79/2005;
g) Reglamento (CE) nº 92/2005;
h) Reglamento (CE) nº 181/2006;
i) Reglamento (CE) nº 197/2006;
j) Reglamento (CE) nº 1192/2006;
k) Reglamento (CE) nº 2007/2006.
2. Las referencias a los actos derogados se entenderán hechas al presente Reglamento.
Medidas transitorias
1. Durante un período transitorio que concluirá el 31 de diciembre de 2011, los explotadores podrán introducir en el mercado abonos y enmiendas del suelo de origen orgánico elaborados antes del 4 de marzo de 2011 de conformidad con los Reglamentos (CE) nº 1774/2002 y (CE) nº 181/2006:
a) si han sido elaborados a partir de:
i) harina de carne y huesos derivada de material de la categoría 2;
ii) proteína animal transformada;
b) aunque no se hayan mezclado con otro ingrediente para excluir el uso posterior de la mezcla con fines de alimentación animal.
2. Durante un período transitorio que concluirá el 31 de enero de 2012, las partidas de subproductos animales y productos derivados acompañadas por un certificado sanitario, declaración o documento comercial, cumplimentado y firmado con arreglo al modelo adecuado establecido en el anexo X del Reglamento (CE) nº 1774/2002 seguirán siendo aceptadas para importación a la Unión, a condición de que tales certificados, declaraciones o documentos hayan sido cumplimentados y firmados antes del 30 de noviembre de 2011.
3. Durante un período transitorio que concluirá el 31 de diciembre de 2012 y no obstante lo dispuesto en el artículo 14 del Reglamento (CE) nº 1069/2009, los Estados miembros podrán autorizar la recogida, el transporte y la eliminación de materiales de la categoría 3 consistentes en productos de origen animal, o de productos alimenticios que contengan productos de origen animal, y que ya no estén destinados al consumo humano por motivos comerciales o debido a problemas de fabricación o defectos de embalaje u otros defectos que no entrañen riesgos para la salud pública o la salud animal, conforme a lo estipulado en el artículo 10, letra f), de dicho Reglamento, por otros medios, distintos de la incineración o el enterramiento in situ, conforme a lo dispuesto en el artículo 19, apartado 1, letra d), de dicho Reglamento, con arreglo a las condiciones para eliminación por otros medios establecidas en el capítulo IV del anexo VI del presente Reglamento.
El presente Reglamento entrará en vigor el vigésimo día siguiente al de su publicación en el Diario Oficial de la Unión Europea.
Será aplicable a partir del 4 de marzo de 2011.
El presente Reglamento será obligatorio en todos sus elementos y directamente aplicable en cada Estado miembro.
Hecho en Bruselas, el 25 de febrero de 2011
Por la Comisión
El Presidente
José Manuel Barroso
[1] DO L 300 de 14.11.2009, p. 1.
[2] DO L 24 de 30.1.1998, p. 9.
[3] DO L 229 de 1.9.2009, p. 1.
[4] DO L 332 de 28.12.2000, p. 91.
[5] DO L 182 de 16.7.1999, p. 1.
[6] DO L 139 de 30.4.2004, p. 1.
[7] DO L 312 de 22.11.2008, p. 3.
[8] DO L 273 de 10.10.2002, p. 1.
[9] DO L 139 de 30.4.2004, p. 55.
[10] DO L 147 de 31.5.2001, p. 1.
[11] DO L 206 de 22.7.1992, p. 7.
[12] DO L 20 de 26.1.2010, p. 7.
[13] DO 17 de 6.10.1958, p. 385/58.
[14] DO L 35 de 8.2.2005, p. 1.
[15] DO L 62 de 15.3.1993, p. 49.
[16] DO L 94 de 31.3.2004, p. 63.
[17] DO 121 de 29.7.1964, p. 1977/64.
[18] DO L 262 de 27.9.1976, p. 169.
[19] DO L 125 de 23.5.1996, p. 3.
[20] DO L 125 de 23.5.1996, p. 10.
[21] DO L 343 de 22.12.2009, p. 74.
[22] DO L 311 de 28.11.2001, p. 67.
[23] DO L 311 de 28.11.2001, p. 1.
[24] DO L 169 de 12.7.1993, p. 1.
[25] DO L 331 de 7.12.1998, p. 1.
[26] DO L 189 de 20.7.1990, p. 17.
[27] DO L 192 de 23.7.2010, p. 1.
[28] DO L 18 de 23.1.2003, p. 11.
[29] DO L 61 de 3.3.1997, p. 1.
[30] DO L 268 de 14.9.1992, p. 54.
[31] DO L 73 de 20.3.2010, p. 1.
[32] DO L 73 de 11.3.2004, p. 1.
[33] DO L 175 de 10.7.2010, p. 1.
[34] DO L 320 de 18.11.2006, p. 53.
[35] DO L 226 de 23.8.2008, p. 1.
[36] DO L 39 de 10.2.2009, p. 12.
[37] DO L 190 de 12.7.2006, p. 1.
[38] DO L 296 de 12.11.2009, p. 1.
[39] DO L 21 de 28.1.2004, p. 11.
[40] DO L 13 de 16.1.1997, p. 28.
[41] DO L 191 de 28.5.2004, p. 1.
[42] DO L 117 de 13.5.2003, p. 14.
[43] DO L 117 de 13.5.2003, p. 32.
[44] DO L 117 de 13.5.2003, p. 37.
[45] DO L 16 de 20.1.2005, p. 46.
[46] DO L 19 de 21.1.2005, p. 27.
[47] DO L 29 de 2.2.2006, p. 31.
[48] DO L 215 de 5.8.2006, p. 10.
[49] DO L 379 de 28.12.2006, p. 98.
[50] DO L 162 de 30.4.2004, p. 62.
[51] DO L 208 de 10.6.2004, p. 9.
[52] DO L 32 de 4.2.2006, p. 13.
A efectos del presente Reglamento serán aplicables las siguientes definiciones:
1. "animales de peletería" : animales criados o mantenidos en cautividad para la producción de pieles y no utilizados para el consumo humano;
2. "sangre" : sangre fresca entera;
3. "materias primas para piensos" : materias primas empleadas como ingredientes de piensos, conforme a lo definido en el artículo 3, apartado 2, letra g), del Reglamento (CE) nº 767/2009, cuyo origen es animal, incluidas las proteínas animales transformadas, los hemoderivados, las grasas extraídas, los ovoproductos, el aceite de pescado, los derivados de grasas, el colágeno, la gelatina y las proteínas hidrolizadas, el fosfato dicálcico, el fosfato tricálcico, la leche, los productos lácteos, los productos derivados de la leche, el calostro, los productos a base de calostro y los lodos de centrifugado o de separación;
4. "hemoderivados" : productos derivados de la sangre o las fracciones de la sangre, con exclusión de la harina de sangre; incluyen plasma seco, congelado o líquido, sangre entera desecada y hematíes secos, congelados o líquidos o sus fracciones y mezclas;
5. "proteína animal transformada" : proteínas animales derivadas íntegramente de material de la categoría 3, sometidas a un tratamiento conforme a lo dispuesto en la sección 1 del capítulo II del anexo X (incluidas las harinas de sangre y las harinas de pescado) que las haga aptas para su utilización directa como ingredientes para piensos o cualquier otro uso para piensos, incluidos los alimentos de animales de compañía, o usos en abonos y enmiendas del suelo orgánicos; no obstante, no incluyen los hemoderivados, la leche, los productos lácteos, el calostro, los productos a base de calostro, los lodos de centrifugado o de separación, la gelatina, las proteínas hidrolizadas y el fosfato dicálcico, los huevos y ovoproductos, incluidas las cáscaras de huevo, el fosfato tricálcico y el colágeno;
6. "harina de sangre" : proteína animal transformada derivada del tratamiento térmico de la sangre o partes de sangre de conformidad con lo dispuesto en la sección 1 del capítulo II del anexo X;
7. "harina de pescado" : proteína animal transformada derivada de animales acuáticos, con excepción de los mamíferos marinos;
8. "grasas extraídas" : grasas derivadas de la transformación de:
a) subproductos animales, o
b) productos destinados al consumo humano, que el explotador ha destinado a otros propósitos distintos del consumo humano;
9. "aceite de pescado" : aceite derivado de la transformación de animales acuáticos o aceite derivado de la transformación de pescado para consumo humano, destinado por el explotador a otros propósitos distintos del consumo humano;
10. "subproductos de la apicultura" : miel, cera, jalea real, propóleo o polen no destinados al consumo humano;
11. "colágeno" : productos a base de proteína derivados de pieles, huesos y tendones de animales;
12. "gelatina" : la proteína natural, soluble, gelificante o no, obtenida mediante la hidrólisis parcial de colágeno producido a partir de huesos, pieles, tendones y nervios de animales;
13. "chicharrones" : los residuos proteicos de la fundición de grasas, tras la separación parcial de la grasa y el agua;
14. "proteínas hidrolizadas" : mezclas de polipéptidos, péptidos y aminoácidos obtenidos mediante la hidrólisis de subproductos animales;
15. "agua blanca" : la mezcla de leche, productos lácteos o productos derivados de los mismos con agua que se recoge durante el aclarado de los equipos empleados en la industria láctea, incluidos los contenedores para productos lácteos, antes de su limpieza y desinfección;
16. "alimentos en conserva para animales de compañía" : los sometidos a tratamiento térmico y contenidos en un recipiente herméticamente cerrado;
17. "accesorios masticables para perros" : productos de calidad masticable para animales de compañía, producidos a partir de pieles sin curtir de ungulados o de otro material de origen animal;
18. "subproducto aromatizante" : líquido o producto derivado deshidratado utilizado para realzar el sabor de los alimentos de animales de compañía;
19. "alimentos para animales de compañía" : productos alimenticios para animales de compañía y accesorios masticables para perros, que
a) contengan material de la categoría 3, distinto del material contemplado en el artículo 10, letras n), o) y p), del Reglamento (CE) nº 1069/2009, y
b) puedan contener material importado de la categoría 1 compuesto por los subproductos animales derivados de animales que hayan sido sometidos a un tratamiento ilegal, tal como se define en el artículo 1, apartado 2, letra d), de la Directiva 96/22/CE o el artículo 2, letra b), de la Directiva 96/23/CE;
20. "alimentos transformados para animales de compañía" : alimentos para animales de compañía, distintos de alimentos crudos para animales de compañía, que han sido transformados de conformidad con el punto 3 del capítulo II del anexo XIII;
21. "alimentos crudos para animales de compañía" : alimentos para animales de compañía que contienen determinados materiales de la categoría 3 que no han sido sometidos a ningún proceso de conservación distinto de la refrigeración o la congelación;
22. "residuos de cocina" : residuos alimenticios, incluido el aceite de cocina usado, procedentes de restaurantes, servicios de catering y cocinas, incluidas las cocinas centrales y las cocinas domésticas;
23. "residuos de fermentación" : los residuos resultantes de la transformación de subproductos animales en una planta de biogás;
24. "contenido del tubo digestivo" : el de mamíferos y aves corredoras;
25. "derivados de grasas" : productos derivados de grasas extraídas que, en lo tocante a las de categorías 1 o 2, han sido transformadas de conformidad con el capítulo XI del anexo XIII;
26. "guano" : producto natural recogido de los excrementos de murciélagos o aves marinas silvestres y que no está mineralizado;
27. "harina de carne y huesos" : proteína animal derivada de la transformación de materiales de las categorías 1 o 2 de conformidad con uno de los métodos de transformación definidos en el capítulo III del anexo IV;
28. "pieles tratadas" : productos derivados obtenidos a partir de pieles sin tratar, distintas de los accesorios masticables para perros, que hayan sido:
a) secados;
b) salados en seco o en salmuera durante un período mínimo de catorce días antes de su expedición;
c) salados con sal marina a la que se habrá añadido un 2 % de carbonato sódico, durante un período mínimo de siete días;
d) sometidos a un proceso de desecado durante un período mínimo de 42 días a una temperatura media mínima de 20 °C, o
e) sometidos a un proceso de conservación distinto del curtido;
29. "pieles sin tratar" : todos los tejidos cutáneos y subcutáneos que no han sido sometidos a ningún tratamiento, distinto del corte, refrigeración o congelación;
30. "plumas y partes de plumas sin tratar" : plumas y partes de plumas, distintas de las plumas y partes de plumas que hayan sido tratadas:
a) con una corriente de vapor, o
b) por cualquier otro método que garantice que no queda ningún riesgo inaceptable;
31. "lana sin tratar" : lana, distinta de la que haya sido:
a) lavada en fábrica;
b) obtenida tras un proceso de curtido, o
c) tratada por cualquier otro método que garantice que no queda ningún riesgo inaceptable;
32. "pelo sin tratar" : pelo, distinto del que haya sido:
a) lavado en fábrica;
b) obtenido tras un proceso de curtido, o
c) tratado por cualquier otro método que garantice que no queda ningún riesgo inaceptable;
33. "cerdas sin tratar" : cerdas, distintas de las que hayan sido:
a) lavadas en fábrica;
b) obtenidas tras un proceso de curtido, o
c) tratadas por cualquier otro método que garantice que no queda ningún riesgo inaceptable;
34. "artículo de exposición" : subproductos animales o productos derivados destinados a actividades artísticas o exposiciones;
35. "producto intermedio" : producto derivado
a) destinado a la fabricación de medicamentos, medicamentos veterinarios, productos sanitarios, productos sanitarios implantables activos, productos para el diagnóstico in vitro o reactivos de laboratorio;
b) cuyas fases de diseño, transformación y fabricación se hayan completado lo suficiente como para considerarlo un producto derivado y hacer que el material sea apto directamente o como ingrediente de un producto para tal fin;
c) que, no obstante, requiera alguna manipulación o transformación posterior, como la mezcla, el recubrimiento, el montaje, el embalaje o etiquetado, que lo haga adecuado para su introducción en el mercado o su puesta en servicio, según proceda, como medicamento, medicamento veterinario, producto sanitario, producto sanitario implantable activo, producto para el diagnóstico in vitro o reactivo de laboratorio;
36. "reactivo de laboratorio" : productos envasados, listos para su uso, que contengan subproductos animales o productos derivados y destinados, solos o en combinación con otras sustancias de origen no animal, para un uso específico en laboratorios como reactivo o producto reactivo, calibrador o material de control para detectar, medir, examinar o producir otras sustancias;
37. "productos utilizados para diagnóstico in vitro" : productos envasados, listos para su uso, que contengan un hemoderivado u otro subproducto animal y se empleen, solos o en combinación con otros, como reactivo, producto reactivo, calibrador, kit o cualquier otro sistema, y se destinen a su utilización in vitro para analizar muestras de origen humano o animal, con la finalidad exclusiva o principal de diagnosticar un estado fisiológico o de salud, una enfermedad o una anomalía genética o de determinar la seguridad y la compatibilidad con otros reactivos; no incluye los órganos y la sangre donados;
38. "muestras para diagnóstico e investigación" : subproductos animales o productos derivados destinados a los siguientes propósitos: examen, en el contexto de las actividades de diagnóstico, análisis para el fomento del avance científico y tecnológico, en el contexto de las actividades de educación o de investigación;
39. "muestras comerciales" : todo subproducto animal o producto derivado destinado al estudio o análisis específico con vistas a emprender un proceso de producción o desarrollar alimentos para animales u otros productos derivados, incluidas las pruebas de maquinaria, para su uso en un establecimiento o planta que:
a) produce alimentos o productos para usos distintos de alimentos o piensos, o
b) transforma subproductos animales o productos derivados;
40. "coincineración" : recuperación o eliminación de los subproductos animales o los productos derivados de éstos, cuando se trate de residuos, en una planta de coincineración;
41. "combustión" : proceso que implica la oxidación de combustible con el fin de usar el valor energético de los subproductos animales o productos derivados, si no se trata de residuos;
42. "incineración" : eliminación de los subproductos animales o los productos derivados, si se trata de residuos, en una planta de incineración, conforme a lo definido en el artículo 3, apartado 4 de la Directiva 2000/76/CE;
43. "residuos de incineración y coincineración" : todo residuo definido en el artículo 3, apartado 13, de la Directiva 2000/76/CE, generado en las plantas de incineración o coincineración que transforman subproductos animales o productos derivados;
44. "código de color" : uso sistemático de colores, con arreglo al punto 1, letra c), del capítulo II del anexo VIII, para presentar información, conforme a lo previsto en el presente Reglamento, en la superficie, o parte de ésta, de un envase, contenedor o vehículo, o en una etiqueta o un símbolo que se ponga en los mismos;
45. "actividades intermedias" : actividades distintas del almacenamiento, mencionadas en el artículo 19, letra b);
46. "curtido" : endurecimiento de las pieles mediante agentes curtientes vegetales, sales de cromo u otras sustancias como sales de aluminio, sales férricas, sales silícicas, aldehídos y quininas, u otros agentes endurecedores sintéticos;
47. "taxidermia" : el arte de arreglar, rellenar y montar las pieles de animales para darle una apariencia vital, de tal forma que la piel montada no pueda transmitir ningún riesgo inaceptable para la salud pública y la salud animal;
48. "comercio" : comercio de mercancías entre los Estados miembros, conforme a lo contemplado en el artículo 28 del Tratado de Funcionamiento de la Unión Europea;
49. "métodos de transformación" : los que figuran en los capítulos III y IV del anexo IV;
50. "lote" : unidad de producción fabricada en una misma planta con parámetros de producción uniformes, como el origen de los materiales, o un número de unidades, cuando se fabrican de manera continua en una misma planta y se almacenan juntas como una unidad de envío;
51. "recipiente herméticamente cerrado" : el diseñado para impedir la entrada de microorganismos y destinado a tal fin;
52. "planta de biogás" : planta en la que los subproductos animales o productos derivados de animales son, como mínimo, parte de los materiales sometidos a degradación biológica en condiciones anaerobias;
53. "centros de recogida" : instalaciones distintas de las plantas de transformación en las que se recogen los subproductos animales mencionados en el artículo 18, apartado 1, del Reglamento (CE) nº 1069/2009 con la intención de destinarlos a la alimentación de los animales contemplados en el mismo artículo;
54. "planta de compostaje" : planta en la que los subproductos animales o productos derivados de animales son, como mínimo, parte de los materiales sometidos a degradación biológica en condiciones aerobias;
55. "planta de coincineración" : planta estacionaria o móvil cuyo principal objeto es la generación de energía o la producción de productos materiales conforme a lo definido en el artículo 3, apartado 5, de la Directiva 2000/76/CE;
56. "planta de incineración" : cualquier unidad técnica y equipo móvil o estacionario dedicado al tratamiento térmico de residuos conforme a lo definido en el artículo 3, apartado 4, de la Directiva 2000/76/CE;
57. "fábrica de alimentos para animales de compañía" : instalaciones o locales para la fabricación de alimentos para animales de compañía o subproductos aromatizantes, según lo contemplado en el artículo 24, apartado 1, letra e), del Reglamento (CE) nº 1069/2009;
58. "planta de transformación" : instalaciones o locales para la transformación de subproductos animales, según lo contemplado en el artículo 24, apartado 1, letra a), del Reglamento (CE) nº 1069/2009, en los que los subproductos animales se transforman de conformidad con lo dispuesto en el anexo IV y/o el anexo X.
1. En Estonia, Letonia y Finlandia se puede alimentar a los siguientes animales de peletería con piensos que contengan harina de huesos y carne u otros productos transformados de conformidad con lo dispuesto en el capítulo III del anexo IV derivados de cuerpos o partes de animales de la misma especie:
a) zorros (Vulpes vulpes);
b) perros mapaches (Nyctereutes procynides).
2. En Estonia y Letonia se puede alimentar a los animales de peletería de la especie visón americano (Mustela vison) con piensos que contengan harina de huesos y carne u otros productos transformados de conformidad con los métodos de transformación dispuestos en el capítulo III del anexo IV derivados de cuerpos o partes de animales de la misma especie.
3. La alimentación contemplada en los puntos 1 y 2 anteriores tendrá lugar en las siguientes condiciones:
a) la alimentación solo tendrá lugar en granjas:
i) que hayan sido registradas por la autoridad competente de conformidad con una solicitud acompañada de documentación que demuestre que no hay motivo para sospechar la presencia del agente responsable de la EET en las especies contempladas en la solicitud;
ii) que apliquen un sistema de vigilancia adecuado de las encefalopatías espongiformes transmisibles (EET) en animales de peletería, que incluya el análisis periódico de muestras en un laboratorio para la detección de EET;
iii) que ofrezcan garantías adecuadas de que no podrá entrar en la cadena alimentaria humana o de otros animales distintos de los animales de peletería ningún subproducto animal o harina de huesos y carne u otros productos transformados de conformidad con lo dispuesto en el capítulo III del anexo IV que se derive de dichos animales o de su descendencia;
iv) que no hayan tenido ningún contacto conocido con una explotación en la que se sospeche o se haya confirmado un brote de EET;
v) que el explotador de la granja registrada garantice que:
- las canales de animales de peletería destinadas a alimentar animales de la misma especie son manipuladas y transformadas por separado de las canales no autorizadas a dicho efecto;
- los animales de peletería alimentados con piensos que contengan harina de huesos y carne u otros productos transformados de conformidad con lo dispuesto en el capítulo III del anexo IV derivados de animales de la misma especie se mantienen separados de otros animales que no son alimentados con productos derivados de animales de la misma especie;
- la granja cumple los requisitos definidos en el punto 2 de la sección 1 del capítulo II del anexo VI y el punto 2, letra b), inciso ii), del capítulo II del anexo VIII.
b) el explotador de la granja debe garantizar que los piensos que contengan harina de huesos y carne u otros productos derivados de una especie y destinados a la alimentación de la misma especie:
i) han sido transformados en una planta de transformación autorizada con arreglo al artículo 24, apartado 1, letra a), del Reglamento (CE) nº 1069/2009, exclusivamente mediante los métodos de transformación 1 a 5 o el método de transformación 7 descritos en el capítulo III del anexo IV del presente Reglamento;
ii) han sido producidos a partir de animales sanos sacrificados para la producción de pieles;
c) si se sospecha o se confirma la existencia de cualquier contacto con una explotación en la que se sospeche o se haya confirmado un brote de EET, el explotador de la granja deberá:
i) informar inmediatamente a la autoridad competente;
ii) interrumpir inmediatamente el envío de animales de peletería a cualquier destino sin autorización escrita de la autoridad competente.
Las siguientes condiciones se aplicarán a la alimentación de animales de granja con pasto de tierras abonadas con abonos o enmiendas del suelo de origen orgánico, ya sea por acceso directo de los animales a la tierra o por siega:
a) deberá haberse respetado el período de espera mínimo de 21 días contemplado en el artículo 11, apartado 1, letra c), del Reglamento (CE) nº 1069/2009;
b) solo se han usado abonos y enmiendas del suelo de origen orgánico que cumplen lo dispuesto en el artículo 32, apartados 1 y 2, del Reglamento (CE) nº 1069/2009 y en el capítulo II del anexo XI del presente Reglamento.
No obstante, no se aplicarán tales condiciones, cuando la tierra solo se ha abonado con los siguientes abonos y enmiendas del suelo de origen orgánico:
a) estiércol y guano;
b) contenido del tubo digestivo, leche, productos lácteos, productos derivados de la leche, calostro y productos a base de calostro, que la autoridad competente no considere que entrañan un peligro para la propagación de ninguna enfermedad animal grave.
1. Los explotadores de plantas de incineración y coincineración mencionadas en el artículo 6, apartado 1, letra b), del presente Reglamento garantizarán el cumplimiento de las siguientes condiciones higiénicas en las explotaciones a su cargo:
a) los subproductos animales y productos derivados deberán eliminarse tan pronto como sea posible tras su llegada, de conformidad con las condiciones establecidas por la autoridad competente. Se almacenarán correctamente hasta su eliminación, de conformidad con las condiciones establecidas por la autoridad competente;
b) las plantas deberán contar asimismo con dispositivos apropiados de limpieza y desinfección de contenedores y vehículos, en especial en una zona designada a tal efecto de la que el agua residual se evacúe de conformidad con la legislación de la Unión, a fin de evitar riesgos de contaminación;
c) las plantas deberán estar ubicadas sobre una superficie dura con buen drenaje;
d) las plantas deberán contar con dispositivos apropiados de protección contra las plagas, como insectos, roedores y aves. Para ello, se utilizará un programa de control de plagas documentado;
e) el personal deberá tener acceso a instalaciones adecuadas para la higiene personal, tales como aseos, vestuarios y lavabos, si se necesitan para impedir el riesgo de contaminación;
f) deberán fijarse y documentarse los procedimientos de limpieza para todas las partes de las instalaciones. Deberá disponerse de equipos y agentes de limpieza adecuados.
g) El control de la higiene deberá incluir inspecciones periódicas del entorno y el equipo. Deberán documentarse los programas de inspección y sus resultados y mantenerse durante dos años como mínimo.
2. El operador de la planta de incineración o coincineración deberá tomar todas las precauciones necesarias en lo referente a la recepción de subproductos animales o productos derivados con el fin de prevenir o limitar tanto como sea posible los riesgos directos para la salud humana o animal.
3. Los animales no deberán tener acceso a las plantas, a los subproductos animales y a los productos derivados a la espera de incineración o coincineración o a las cenizas resultantes de la incineración o coincineración de los subproductos animales.
4. Si la planta de incineración o coincineración está situada en una explotación ganadera:
a) deberá haber una separación física total entre el equipo de incineración o coincineración y el ganado, su pienso y sus camas, con vallas en caso necesario;
b) el equipo deberá estar dedicado exclusivamente a las actividades de incineración y no se empleará en ningún otro lugar de la explotación o, en caso contrario, deberá ser limpiado y desinfectado antes de cada uso;
c) el personal que trabaje en la planta deberá cambiarse de ropa y calzado antes de manipular el ganado o los piensos.
5. El almacenamiento de subproductos animales y productos derivados a la espera de su incineración o coincineración y las cenizas deberá efectuarse en contenedores tapados, correctamente identificados y, si procede, estancos.
6. Los subproductos animales no incinerados en su totalidad deberán incinerarse de nuevo o eliminarse por otros medios, distintos de la eliminación en un vertedero autorizado, de conformidad con los artículos 12, 13 y 14, según corresponda, del Reglamento (CE) nº 1069/2009.
Las instalaciones de incineración o coincineración se diseñarán, equiparán, construirán y explotarán de modo que la temperatura de los gases derivados del proceso se eleve, de manera controlada y homogénea, e incluso en las condiciones más desfavorables, hasta 850 °C, durante 2 segundos al menos, o hasta 1100 °C durante 0,2 segundos, medidos cerca de la pared interna de la cámara donde se realiza la incineración o coincineración o en otro punto representativo de ésta autorizado por la autoridad competente.
1. Se reducirán al mínimo la cantidad y la nocividad de los residuos procedentes de la incineración y la coincineración. Dichos residuos deben recogerse, si procede, directamente en la planta o fuera de ella de conformidad con la legislación de la Unión en vigor o eliminarse en un vertedero autorizado.
2. El transporte y el almacenamiento temporal de los residuos secos, incluso de polvo, se realizarán de forma que se evite su dispersión en el medio ambiente, por ejemplo, en contenedores cerrados.
1. Deberán utilizarse técnicas de seguimiento de los parámetros y condiciones relacionadas con el proceso de incineración o coincineración.
2. Los requisitos de medición de temperatura se establecerán en la autorización o en las condiciones anejas a la autorización expedida por la autoridad competente.
3. El funcionamiento de los equipos de seguimiento automatizado de las emisiones a la atmósfera y a las aguas estará sujeto a control y a una prueba anual de supervisión.
4. Los resultados de las mediciones de temperatura se registrarán y presentarán de manera adecuada, para que la autoridad competente pueda comprobar el cumplimiento de las condiciones de explotación autorizadas y de los valores límite de emisión establecidos en el presente Reglamento, con arreglo a los procedimientos que establezca dicha autoridad.
En caso de avería o de condiciones anormales de funcionamiento de una planta de incineración o de coincineración, el explotador de la instalación reducirá o detendrá el funcionamiento de la instalación lo antes posible hasta que éste pueda reanudarse normalmente.
Las plantas de incineración o coincineración que procesen exclusivamente subproductos animales y productos derivados con una capacidad superior a 50 kilogramos por hora (plantas de alta capacidad) y que no estén obligadas a contar con un permiso de explotación de conformidad con la Directiva 2000/76/CE respetarán las siguientes condiciones:
a) Las plantas deberán contar con al menos un quemador auxiliar por cada línea. Este quemador se pondrá en marcha automáticamente cuando la temperatura de los gases de combustión, tras la última inyección de aire de combustión, descienda por debajo 850 °C o 1100 °C, según los casos. Asimismo, deberá utilizarse dicho quemador durante las operaciones de puesta en marcha y parada de la instalación a fin de que la temperatura de 850 °C o 1100 °C, según los casos, se mantenga en todo momento durante estas operaciones mientras haya materiales no incinerados en la cámara donde se efectúa la incineración o coincineración.
b) Cuando los subproductos animales o productos derivados se introducen mediante un proceso continuo en la cámara donde se efectúa la incineración o coincineración, las plantas deberán equiparse con un sistema automático que impida la introducción de subproductos animales o productos derivados durante la puesta en marcha, hasta que se haya alcanzado la temperatura de 850 °C o 1100 °C, según los casos, y siempre que no se mantenga dicha temperatura.
c) El explotador deberá explotar la planta de incineración de modo que obtenga un grado de incineración tal que el contenido de carbono orgánico total de las escorias y cenizas sea inferior al 3 % o su pérdida sea inferior al 5 % del peso seco de la materia. Si es preciso, se emplearán técnicas adecuadas de tratamiento previo.
1. Los emplazamientos de las plantas de alta capacidad, incluidas las zonas de almacenamiento de subproductos animales anejas, se diseñarán de modo que se impida el vertido no autorizado y accidental de sustancias contaminantes al suelo y a las aguas superficiales y subterráneas.
2. Deberá disponerse de capacidad de almacenamiento para la escorrentía de precipitaciones contaminadas procedente del emplazamiento de la instalación o para las aguas contaminadas que provengan de derrames o de operaciones de lucha contra incendios.
El explotador garantizará, si fuera necesario, que dichas aguas puedan someterse a pruebas y tratarse antes de su vertido, cuando sea necesario.
Las plantas de incineración y coincineración que procesen exclusivamente subproductos animales y productos derivados con una capacidad máxima inferior a 50 kilogramos de subproductos animales por hora o por lote (plantas de baja capacidad) y que no estén obligadas a contar con un permiso de explotación de conformidad con la Directiva 2000/76/CE:
a) deberán emplearse únicamente para la eliminación de:
i) animales de compañía muertos según se contempla en el artículo 8, letra a), inciso iii), del Reglamento (CE) nº 1069/2009, o
ii) los materiales de la categoría 1 mencionados en el artículo 8, letras b), e) y f), los materiales de la categoría 2 mencionados en el artículo 9 o los materiales de la categoría 3 mencionados en el artículo 10 de dicho Reglamento;
b) cuando se introducen en la planta de baja capacidad los materiales contemplados en el artículo 8, letra b), del Reglamento (CE) nº 1069/2009, ésta deberá estar equipada con un quemador auxiliar;
c) deberán explotarse de tal forma que los subproductos animales queden reducidos completamente a cenizas.
1. Las plantas de transformación cumplirán como mínimo las condiciones siguientes, para la transformación por esterilización a presión o mediante los métodos de transformación contemplados en el artículo 15, apartado 1, letra b), del Reglamento (CE) nº 1069/2009:
a) las plantas de transformación deberán ubicarse en un emplazamiento distinto al de los mataderos u otros establecimientos autorizados o registrados de conformidad con el Reglamento (CE) nº 852/2004 o el Reglamento (CE) nº 853/2004, salvo que los riesgos para la salud pública y la sanidad animal resultantes de la transformación de subproductos animales que procedan de dichos mataderos o establecimientos queden atenuados mediante el cumplimiento de los siguientes requisitos mínimos:
i) la planta de transformación deberá estar físicamente separada del matadero u otro establecimiento, si procede ubicando la planta de transformación en un edificio completamente independiente del matadero u otro establecimiento;
ii) se instalará y pondrá en funcionamiento en la planta de transformación:
- un sistema transportador de paso obligatorio que una la planta de transformación con el matadero u otro establecimiento,
- entradas, zonas de recepción, equipos y salidas separados para la planta de transformación y el matadero o establecimiento;
iii) deberán adoptarse medidas para impedir la propagación de los riesgos a través de la actividad del personal que trabaja en la planta de transformación y el matadero u otro establecimiento;
iv) las personas no autorizadas y los animales no deberán tener acceso a la planta de transformación.
No obstante lo dispuesto en los incisos i) a iv), en el caso de las plantas de transformación que procesen material de categoría 3, la autoridad competente podrá autorizar otros requisitos, en lugar de los establecidos en dichos incisos, con el fin de reducir los riesgos para la salud pública y la salud animal, incluidos los riesgos derivados de la transformación de material de la categoría 3 procedente de otros establecimientos externos autorizados o registrados con arreglo al Reglamento (CE) nº 852/2004 o al Reglamento (CE) nº 853/2004.
Los Estados miembros informarán a la Comisión y a los demás Estados miembros en el marco del Comité Permanente de la Cadena Alimentaria y de Sanidad Animal contemplado en el artículo 52, apartado 1, del Reglamento (CE) nº 1069/2009, sobre la utilización de esta excepción por parte de sus autoridades competentes.
b) la planta de transformación deberá disponer de un sector "limpio" y otro "sucio", convenientemente separados. El sector sucio deberá contar con un lugar cubierto para recibir los subproductos animales y estar construido de manera que resulte fácil de limpiar y desinfectar. Los suelos estarán construidos de manera que facilite la evacuación de los líquidos;
c) la planta de transformación deberá disponer de instalaciones adecuadas, como servicios, vestuarios y lavabos adecuados para el personal;
d) la planta de transformación deberá disponer de una capacidad de producción de agua caliente y vapor suficientes para la transformación de los subproductos animales;
e) el sector sucio deberá, si procede, disponer de equipo para reducir el tamaño de los subproductos animales y para trasladar los subproductos animales triturados a la unidad de transformación;
f) cuando sea necesario un tratamiento térmico, todas las instalaciones deberán disponer de:
i) equipo de medición para controlar la evolución de la temperatura a lo largo del tiempo y, si fuere necesario para el método de transformación empleado, la presión en los puntos críticos;
ii) dispositivos que registren de forma continua los resultados de estas mediciones de modo que estén accesibles a los efectos de realizar pruebas y controles oficiales;
iii) un sistema de seguridad adecuado para evitar un calentamiento insuficiente;
g) para impedir la recontaminación del producto derivado por la introducción de subproductos animales procedentes del exterior, deberá existir una clara separación entre la parte de la planta reservada a la descarga del material destinado a su transformación y las reservadas a la transformación de ese producto y al almacenamiento del producto derivado.
2. Las plantas de transformación deberán disponer de instalaciones adecuadas para limpiar y desinfectar los contenedores o recipientes en los que se reciban los subproductos animales y los medios de transporte, con excepción de los buques.
3. Deberán proveerse las instalaciones adecuadas para la desinfección de las ruedas y otras partes de los vehículos, si procede, al abandonar el sector sucio de la planta de transformación.
4. Todas las plantas de transformación deberán disponer de un sistema de evacuación de aguas residuales que cumpla los requisitos fijados por la autoridad competente con arreglo a la legislación de la Unión.
5. Las plantas de transformación deberán disponer de su propio laboratorio o recurrir a los servicios de un laboratorio externo. Ese laboratorio deberá disponer del equipo suficiente para realizar los análisis necesarios y estar autorizado por la autoridad competente de conformidad con una evaluación de la capacidad del laboratorio para realizar dichos análisis, estar acreditado conforme a normas internacionalmente reconocidas o someterse a controles periódicos por la autoridad competente, con el fin de evaluar la capacidad del laboratorio para realizar dichos análisis.
6. La planta de transformación deberá disponer de una sala adecuadamente equipada, que pueda cerrarse con llave, para uso exclusivo del servicio de inspección, cuando el volumen de productos tratados requiera la presencia regular o permanente de la autoridad competente, de conformidad con una evaluación de riesgos.
1. Las plantas de transformación que transformen material de la categoría 1, y otros locales en los que se retire material especificado de riesgo, los mataderos y las plantas de transformación que transformen material de la categoría 2 aplicarán un proceso de pretratamiento para la retención y recogida de material animal como paso inicial en el tratamiento de las aguas residuales.
El equipo utilizado en el proceso de pretratamiento dispondrá de sifones de drenaje en las alcantarillas de desagüe o cribas con poros o mallas no superiores a 6 mm a su salida, o sistemas equivalentes que garanticen que las partes sólidas de las aguas residuales que pasen a través de ellos no sean superiores a 6 mm.
2. Las aguas residuales de los locales contemplados en el punto 1 deberán pasar por un proceso de pretratamiento que garantice que han sido filtradas en su totalidad antes de su evacuación de los locales. No se deberá picar, macerar ni aplicar otro tipo de tratamiento o presión que pueda facilitar el paso de materia sólida de origen animal a través del proceso de pretratamiento.
3. Todo material de origen animal retenido en los sistemas de pretratamiento en los locales mencionados en el punto 1 deberá recogerse y transportarse como material de la categoría 1 o de la categoría 2, según proceda, y eliminarse de acuerdo con lo dispuesto en el Reglamento (CE) nº 1069/2009.
4. Las aguas residuales que hayan pasado el proceso de pretratamiento contemplado en el punto 1 y las aguas residuales procedentes de otros locales en los que se manipulen o transformen subproductos animales serán tratadas con arreglo a la legislación de la Unión, sin restricciones en virtud del presente Reglamento.
5. Además de los requisitos dispuestos en el punto 4, la autoridad competente podrá exigir a los explotadores que procedan al tratamiento de las aguas residuales procedentes del sector sucio de las plantas de transformación y de las plantas o establecimientos en los que se lleven a cabo operaciones intermedias con material de las categorías 1 o 2 o en los que se almacene material de las categorías 1 o 2, de conformidad con condiciones que garanticen la reducción de los riesgos derivados de patógenos.
6. No obstante lo establecido en los puntos 1 a 5, se prohibirá la eliminación de subproductos animales, incluidas la sangre y la leche, o productos derivados a través de la corriente de aguas residuales.
Sin embargo, el material de la categoría 3 consistente en lodos de centrifugado o de separación puede eliminarse a través de la corriente de aguas residuales, a condición de que haya sido sometido a uno de los tratamientos para lodos de centrifugado o de separación establecidos en la parte III de la sección 4 del capítulo II del anexo X del presente Reglamento.
La disposición de los locales de transformación del material de la categoría 1 y de la categoría 2 deberá garantizar la total separación del material de la categoría 1 y del material de la categoría 2, desde el momento de la recepción de la materia prima hasta el despacho del producto derivado resultante, salvo que se transforme como material de la categoría 1 una mezcla de material de la categoría 1 y de la categoría 2.
Además de las condiciones generales establecidas en la sección 1, deberán aplicarse las siguientes:
1. Las plantas de transformación de materiales de la categoría 3 no deberán estar ubicadas en el mismo lugar que las plantas de transformación dedicadas a la transformación de materiales de las categorías 1 o 2, salvo que se encuentren en un edificio totalmente separado.
2. No obstante, la autoridad competente podrá autorizar la transformación de materiales de la categoría 3 en un lugar en el que se manipule o transforme material de la categoría 1 o de la categoría 2, siempre que se impida la contaminación cruzada gracias a:
a) la disposición de los locales, en concreto los dispositivos de recepción y mediante la posterior manipulación de las materias primas;
b) la disposición y gestión de los equipos empleados para la transformación, así como la disposición y gestión de líneas de transformación independientes o de procedimientos de limpieza que eviten la propagación de cualquier posible riesgo para la salud pública o la salud animal, y
c) la disposición y la gestión de las zonas dedicadas al almacenamiento provisional de los productos acabados.
3. Las plantas de transformación dedicadas a la transformación de material de la categoría 3 deberán contar con una instalación para comprobar la presencia de cuerpos extraños, como material de envasado o piezas metálicas, en los subproductos animales o productos derivados, cuando dichos materiales de transformación estén destinados a la alimentación de animales. Tales cuerpos extraños deberán ser retirados antes de la transformación o durante la misma.
Además de los requisitos generales de higiene previstos en el artículo 25 del Reglamento (CE) nº 1069/2009, las plantas de transformación contarán con un programa de control de plagas documentado para la aplicación de las disposiciones de protección contra las plagas, como insectos, roedores y aves, mencionadas en el artículo 25, apartado 1, letra c), de dicho Reglamento.
1. Se utilizarán equipos de medición y de registro calibrados con precisión para controlar continuamente las condiciones de transformación. Se llevarán registros en los que consten las fechas de calibrado de los equipos de medición y de registro.
2. El material que no haya sido sometido al tratamiento térmico especificado, como el que se haya descartado antes del proceso o el que se escape de los recipientes, volverá a ponerse en circulación y a someterse al tratamiento térmico, o se recogerá y volverá a transformar o eliminará de conformidad con lo dispuesto en el Reglamento (CE) nº 1069/2009.
Salvo cuando la autoridad competente exija la aplicación de la esterilización a presión (método 1), los materiales de las categorías 1 y 2 se transformarán de conformidad con los métodos de transformación 2, 3, 4 o 5 mencionados en el capítulo III.
1. Entre los puntos críticos de control que determinan el alcance de los tratamientos térmicos aplicados en la transformación figurarán para cada método de transformación, según se especifica en el capítulo III:
a) la dimensión de las partículas de materia prima;
b) la temperatura alcanzada en el tratamiento térmico;
c) la presión, en caso de aplicarse a la materia prima;
d) la duración del tratamiento térmico o, en sistemas continuos, la velocidad de alimentación. Además, se especificarán los parámetros mínimos de transformación para cada punto de control crítico aplicable.
2. En el caso de tratamientos químicos autorizados por la autoridad competente como método de transformación 7 de conformidad con lo dispuesto en la letra G del capítulo III, los puntos críticos de control que determinan el alcance de los tratamientos químicos aplicados incluirán los ajustes del pH conseguidos.
3. Deberán llevarse, y conservarse durante al menos dos años, registros que demuestren que se han aplicado los valores mínimos del proceso para cada punto crítico de control.
4. El material de la categoría 3 se transformará con arreglo a uno de los métodos de transformación 1 a 5 o al método de transformación 7 o, en el caso de material procedente de animales acuáticos, a uno de los métodos de transformación 1 a 7, según se hace referencia en el capítulo III.
A. Método de transformación 1 (esterilización a presión)
Reducción
1. Si la dimensión granulométrica de las partículas de los subproductos animales que deben transformarse es superior a 50 mm, deberá reducirse utilizando el equipo adecuado, calibrándolo de tal manera que la dimensión de las partículas después de la reducción no supere los 50 mm. Deberá controlarse diariamente la eficacia del equipo y llevarse un registro de sus condiciones. Si en los controles se detectase la existencia de partículas mayores de 50 mm, deberá detenerse el proceso y deberán realizarse las reparaciones necesarias antes de reanudarlo.
Tiempo, temperatura y presión
2. Los subproductos animales cuya dimensión granulométrica de partículas no sea superior a 50 mm deberán calentarse a una temperatura interna superior a 133 °C a una presión (absoluta) de al menos 3 bares durante un período mínimo de 20 minutos. La presión debe producirse por la evacuación de todo el aire en la cámara de esterilización y su sustitución por vapor ("vapor saturado"); el método térmico puede aplicarse como proceso único o como una fase de esterilización anterior o posterior al proceso.
3. La transformación podrá llevarse a cabo mediante un sistema continuo o discontinuo.
B. Método de transformación 2
Reducción
1. Si la dimensión granulométrica de las partículas de los subproductos animales que deben transformarse es superior a 150 mm, deberá reducirse utilizando el equipo adecuado, calibrándolo de tal manera que la dimensión de las partículas después de la reducción no supere los 150 mm. Deberá controlarse diariamente la eficacia del equipo y llevarse un registro de sus condiciones. Si en los controles se detectase la existencia de partículas mayores de 150 mm, deberá detenerse el proceso y deberán realizarse las reparaciones necesarias antes de reanudarlo.
Tiempo, temperatura y presión
2. Tras la reducción, los subproductos animales deberán calentarse de modo que garantice una temperatura interna superior a 100 °C durante un período mínimo de 125 minutos, una temperatura interna superior a 110 °C durante un período mínimo de 120 minutos y una temperatura interna superior a 120 °C durante un período mínimo de 50 minutos.
Las temperaturas internas pueden alcanzarse de forma consecutiva o a través de una combinación coincidente de los períodos indicados.
3. La transformación deberá llevarse a cabo mediante un sistema discontinuo.
C. Método de transformación 3
Reducción
1. Si la dimensión granulométrica de las partículas de los subproductos animales que deben transformarse es superior a 30 mm, deberá reducirse utilizando el equipo adecuado, calibrándolo de tal manera que la dimensión de las partículas después de la reducción no supere los 30 mm. Deberá controlarse diariamente la eficacia del equipo y llevarse un registro de sus condiciones. Si en los controles se detectase la existencia de partículas mayores de 30 mm, deberá detenerse el proceso y deberán realizarse las reparaciones necesarias antes de reanudarlo.
Tiempo, temperatura y presión
2. Tras la reducción, los subproductos animales deberán calentarse de modo que garantice una temperatura interna superior a 100 °C durante un período mínimo de 95 minutos, una temperatura interna superior a 110 °C durante un período mínimo de 55 minutos y una temperatura interna superior a 120 °C durante un período mínimo de 13 minutos.
Las temperaturas internas pueden alcanzarse de forma consecutiva o a través de una combinación coincidente de los períodos indicados.
3. La transformación podrá llevarse a cabo mediante un sistema continuo o discontinuo.
D. Método de transformación 4
Reducción
1. Si la dimensión granulométrica de las partículas de los subproductos animales que deben transformarse es superior a 30 mm, deberá reducirse utilizando el equipo adecuado, calibrándolo de tal manera que la dimensión de las partículas después de la reducción no supere los 30 mm. Deberá controlarse diariamente la eficacia del equipo y llevarse un registro de sus condiciones. Si en los controles se detectase la existencia de partículas mayores de 30 mm, deberá detenerse el proceso y deberán realizarse las reparaciones necesarias antes de reanudarlo.
Tiempo, temperatura y presión
2. Tras la reducción, los subproductos animales deberán introducirse en un recipiente con grasa añadida y calentarse de modo que garantice una temperatura interna superior a 100 °C durante un período mínimo de 16 minutos, una temperatura interna superior a 110 °C durante un período mínimo de 13 minutos, una temperatura interna superior a 120 °C durante al menos 8 minutos y una temperatura interna superior a 130 °C durante un período mínimo de 3 minutos.
Las temperaturas internas pueden alcanzarse de forma consecutiva o a través de una combinación coincidente de los períodos indicados.
3. La transformación podrá llevarse a cabo mediante un sistema continuo o discontinuo.
E. Método de transformación 5
Reducción
1. Si la dimensión granulométrica de las partículas de los subproductos animales que deben transformarse es superior a 20 mm, deberá reducirse utilizando el equipo adecuado, calibrándolo de tal manera que la dimensión de las partículas después de la reducción no supere los 20 mm. Deberá controlarse diariamente la eficacia del equipo y llevarse un registro de sus condiciones. Si en los controles se detectase la existencia de partículas mayores de 20 mm, deberá detenerse el proceso y deberán realizarse las reparaciones necesarias antes de reanudarlo.
Tiempo, temperatura y presión
2. Tras la reducción, los subproductos animales deberán calentarse hasta su coagulación y después se procederá a su prensado para separar la grasa y el agua del material proteínico. El material proteínico deberá después ser calentado de modo que garantice una temperatura interna superior a 80 °C durante un período mínimo de 120 minutos y una temperatura interna superior a 100 °C durante un período mínimo de 60 minutos.
Las temperaturas internas pueden alcanzarse de forma consecutiva o a través de una combinación coincidente de los períodos indicados.
3. La transformación podrá llevarse a cabo mediante un sistema continuo o discontinuo.
F. Método de transformación 6 (para subproductos animales de la categoría 3 procedentes de animales acuáticos o invertebrados acuáticos exclusivamente)
Reducción
1. Los subproductos animales deberán reducirse a una dimensión que no será superior a:
a) 50 mm en caso de tratamiento térmico según la letra a) del punto 2, o
b) 30 mm en caso de tratamiento térmico según la letra b) del punto 2.
Después deberán mezclarse con ácido fórmico para reducir y mantener su pH en 4,0 o menos. La mezcla deberá almacenarse durante un mínimo de 24 horas antes de su tratamiento posterior.
Tiempo, temperatura y presión
2. Tras la reducción, la mezcla deberá calentarse a:
a) una temperatura interna de al menos 90 °C durante 60 minutos como mínimo. o
b) una temperatura interna de al menos 70 °C durante 60 minutos como mínimo.
Si se emplea un sistema de flujo continuo, la progresión del producto a través del conversor térmico deberá controlarse mediante dispositivos mecánicos, limitando su desplazamiento de manera que al final de la operación de tratamiento térmico el producto haya sido sometido a un ciclo suficiente tanto de tiempo como de temperatura.
3. La transformación podrá llevarse a cabo mediante un sistema continuo o discontinuo.
G. Método de transformación 7
1. Todo método de transformación autorizado por la autoridad competente una vez el explotador le haya demostrado:
a) la identificación de los peligros relevantes en la materia prima, a la vista de su origen, y de los riesgos a la vista de la calificación sanitaria del Estado miembro o de la zona en la que se pretende emplear el método;
b) la capacidad del método de transformación para reducir dichos peligros a un nivel que no entrañe riesgos significativos para la salud pública o animal;
c) la toma de muestras diaria del producto final a lo largo de un período de 30 días de producción en cumplimiento de las siguientes normas microbiológicas:
i) muestras de material tomadas directamente después del tratamiento:
Clostridium perfringens ausente en 1 g de los productos;
ii) muestras del material tomadas durante el período de almacenamiento o al final del mismo:
Salmonella: ausente en 25 g: n = 5, c = 0, m = 0, M = 0
Enterobacteriaceae: n=5; m=10; M=300 en 1 g
donde:
n = número de muestras del ensayo;
m = valor umbral del número de bacterias; el resultado se considera satisfactorio si el número de bacterias en todas las muestras no es superior a m;
M = valor máximo del número de bacterias; el resultado se considera insatisfactorio si el número de bacterias en una o más muestras es igual o superior a M; y
c = número de muestras cuyo recuento de bacterias puede situarse entre m y M; las muestras siguen considerándose aceptables si el recuento de bacterias de las demás muestras es igual o inferior a m.
2. Deberán registrarse y conservarse los datos sobre los puntos críticos de control con los que cada planta de tratamiento cumple satisfactoriamente las normas microbiológicas de modo que el explotador y la autoridad competente puedan seguir el funcionamiento de la planta de tratamiento. La información que ha de registrarse y controlarse deberá incluir la dimensión granulométrica y, si procede, la temperatura crítica, el tiempo absoluto, el perfil de presión, la frecuencia de recarga de materia prima y el porcentaje de reciclaje de la grasa.
3. No obstante lo dispuesto en el punto 1, la autoridad competente podrá autorizar el uso de métodos de transformación que hayan sido aprobados antes de la fecha de entrada en vigor del presente Reglamento, de conformidad con el capítulo III de anexo V del Reglamento (CE) nº 1774/2002.
4. La autoridad competente suspenderá de forma temporal o permanente la aplicación de los métodos de transformación mencionados en los puntos 1 y 3, en caso de haber obtenido pruebas de variación de algunas de las circunstancias especificadas en el punto 1, letras a) o b).
5. Cuando así lo solicite alguna autoridad competente de otro Estado miembro, la autoridad competente le remitirá la información de que disponga, de conformidad con los puntos 1 y 2, en relación con cualquier método de transformación autorizado.
1. Los materiales resultantes de la transformación de materiales de la categoría 1 y 2, salvo el biodiesel producido de conformidad con la letra D de la sección 2 del presente capítulo, se marcarán de forma permanente con arreglo a los requisitos de marcado de determinados productos derivados dispuestos en el capítulo V del anexo VIII.
2. La autoridad competente de un Estado miembro pondrá los resultados de los controles oficiales a disposición de la autoridad competente de otro Estado miembro previa solicitud, cuando se emplea un método alternativo por primera vez en dicho Estado miembro, a fin de facilitar la introducción del nuevo método alternativo.
A. Proceso de hidrólisis alcalina
1. Materia prima
Para este proceso, podrán utilizarse subproductos animales de todas las categorías.
2. Método de tratamiento
La hidrólisis alcalina se realizará conforme a las siguientes normas de transformación:
a) deberá utilizarse una solución de hidróxido sódico (NaOH) o de hidróxido potásico (KOH) (o una combinación de ambos) en cantidad suficiente para garantizar una equivalencia molar aproximada con respecto al peso, el tipo y la composición de los subproductos animales que deben ser digeridos.
En caso de que los subproductos animales tengan un alto contenido de grasa animal que neutralice la base, la base añadida deberá ajustarse a fin de lograr dicha equivalencia molar;
b) los subproductos animales deberán introducirse en un recipiente de aleación de acero. La cantidad medida de base deberá añadirse en forma sólida o como solución, según lo previsto en el punto 1;
c) el recipiente deberá estar cerrado y los subproductos animales y la mezcla alcalina deberán calentarse a una temperatura interna de al menos 150 °C y a una presión (absoluta) de al menos 4 bares durante un período mínimo de:
i) tres horas sin interrupción;
ii) seis horas sin interrupción en caso de tratamiento de los subproductos animales contemplados en el artículo 8, letra a), incisos i) y ii), del Reglamento (CE) nº 1069/2009.
Sin embargo, los materiales derivados de materiales de la categoría 1 compuestos por animales sacrificados en aplicación de medidas de erradicación de la EET consistentes en rumiantes que no precisen pruebas de diagnóstico de EET o rumiantes sometidos a pruebas de diagnóstico con resultado negativo de conformidad con el artículo 6, apartado 1, del Reglamento (CE) nº 999/2001, se pueden transformar con arreglo al punto 2, letra c), inciso i), de la presente sección, o
iii) una hora sin interrupción en caso de subproductos animales compuestos de materiales procedentes de pescado o de aves de corral;
d) el proceso deberá llevarse a cabo mediante un sistema por lotes, y el material del recipiente deberá mezclarse constantemente para facilitar el proceso de digestión hasta que se disuelven los tejidos y se ablandan los huesos y dientes, y
e) los subproductos animales deberán tratarse de forma que los requisitos relativos al tiempo, la temperatura y la presión se satisfagan simultáneamente.
B. Proceso de hidrólisis a alta presión y alta temperatura
1. Materia prima
Para este proceso, podrán utilizarse materiales de la categoría 2 y 3.
2. Método de tratamiento
La hidrólisis a alta presión y alta temperatura se realizará conforme a las siguientes normas de transformación:
a) los subproductos animales deberán calentarse a una temperatura interna de al menos 180 °C durante un período mínimo de 40 minutos sin interrupción y a una presión (absoluta) de al menos 12 bares, mediante la aplicación indirecta de vapor al reactor biolítico;
b) el proceso deberá llevarse a cabo en un lote, y el material del recipiente deberá mezclarse constantemente, y
c) los subproductos animales deberán tratarse de forma que los requisitos relativos al tiempo, la temperatura y la presión se satisfagan simultáneamente.
C. Producción de biogás por hidrólisis a alta presión
1. Materia prima
Para este proceso, podrán utilizarse subproductos animales de todas las categorías.
2. Método de tratamiento
La producción de biogás por hidrólisis a alta presión se realizará conforme a las siguientes normas de transformación:
a) los subproductos animales deberán transformarse en primer lugar empleando el método de transformación 1 (esterilización por presión) según se dispone en el capítulo III en una planta de transformación autorizada;
b) tras el proceso mencionado en el punto a) anterior, los materiales desgrasados deberán tratarse a una temperatura mínima de 220 °C durante al menos 20 minutos a una presión (absoluta) de al menos 25 bares, calentándolos mediante un procedimiento en dos fases, primero por inyección directa de vapor y luego indirectamente en un intercambiador térmico coaxial;
c) el proceso deberá llevarse a cabo mediante un sistema por lotes o continuo y el material del recipiente deberá mezclarse constantemente;
d) los subproductos animales deberán tratarse de forma que los requisitos relativos al tiempo, la temperatura y la presión se satisfagan simultáneamente;
e) el material resultante deberá mezclarse con agua y fermentarse anaeróbicamente (transformación en biogás) en un reactor de biogás, y
f) en caso de materia prima de la categoría 1, el proceso al completo deberá tener lugar en el mismo emplazamiento y en un sistema cerrado, y el biogás producido durante el proceso deberá quemarse rápidamente en la misma planta a un mínimo de 900 °C y, a continuación, refrigerarse rápidamente ("enfriamiento").
D. Proceso de producción de biodiesel
1. Materia prima
Para este proceso, podrá utilizarse una fracción grasa derivada de subproductos animales de cualquier categoría.
2. Método de tratamiento
La producción de biodiesel se realizará conforme a las siguientes normas de transformación:
a) salvo cuando se use aceite de pescado o grasas extraídas, que hayan sido producidos de conformidad con las secciones VIII o XII del anexo III del Reglamento (CE) nº 853/2004, respectivamente, la fracción grasa derivada de los subproductos animales deberá transformarse en primer lugar utilizando:
i) en el caso de materiales de la categoría 1 o 2, el método de transformación 1 (esterilización por presión) contemplado en el capítulo III, y
ii) en el caso de materiales de la categoría 3, cualquiera de los métodos de transformación 1 a 5 o el método de transformación 7 o, en el caso de material derivado de peces, los métodos de transformación 1 a 7 mencionados en el capítulo III;
b) la grasa transformada deberá someterse entonces a una nueva transformación mediante uno de los métodos siguientes:
i) un proceso por el cual la grasa transformada deberá separarse de la proteína y, en el caso de grasa derivada de rumiantes, las impurezas insolubles deberán eliminarse hasta un nivel que no supere el 0,15 % del peso y, a continuación la grasa transformada, se someterá a esterificación y transesterificación.
No obstante, la esterificación no será necesaria para la grasa transformada derivada de material de la categoría 3. Para la esterificación, el pH deberá reducirse a un valor inferior a 1 añadiendo ácido sulfúrico (H2SO4) o un ácido equivalente, y la mezcla deberá calentarse a 72 °C durante 2 horas como mínimo, mezclándola enérgicamente durante todo este tiempo.
La transesterificación deberá llevarse a cabo elevando el pH hasta un valor en torno a 14 con hidróxido de potasio o una base equivalente, a una temperatura de 35 a 50 °C durante un mínimo de 15 minutos. La transesterificación se realizará dos veces en las condiciones descritas en este punto, utilizando una nueva solución alcalina. A continuación deberán refinarse los productos, incluida su destilación al vacío a 150 °C, que dará como resultado el biodiésel;
ii) un proceso que aplique parámetros equivalentes que hayan sido autorizados por la autoridad competente.
E. Proceso de gasificación Brookes
1. Materia prima
Para este proceso, podrán utilizarse materiales de la categoría 2 y 3.
2. Método de tratamiento
La gasificación Brookes se realizará conforme a las siguientes normas de transformación:
a) la cámara de poscombustión deberá calentarse utilizando gas natural;
b) los subproductos animales deberán introducirse en la cámara primaria del gasificador y deberá cerrarse la puerta. La cámara primaria no deberá disponer de quemadores, por lo que deberá calentarse mediante la transferencia de calor por conducción desde el posquemador, que deberá situarse debajo de ella. El único aire que penetra en la cámara primaria deberá entrar por tres válvulas de admisión situadas en la puerta principal para aumentar la eficacia del proceso;
c) los subproductos animales deberán volatilizarse en hidrocarburos complejos y los gases resultantes deberán pasar a través de una estrecha apertura situada en la parte superior de la pared trasera de la cámara primaria hacia las zonas de mezclado y craqueo, en donde deberán descomponerse en sus elementos constitutivos. Por último, los gases deberán pasar a la cámara del posquemador, donde deberán quemarse con la llama de un quemador de gas natural con exceso de aire;
d) cada unidad de tratamiento deberá contar con dos quemadores y dos ventiladores secundarios como medida de seguridad en caso de fallo del quemador o del ventilador. La cámara secundaria deberá estar diseñada para permitir un tiempo mínimo de residencia de dos segundos a una temperatura de al menos 950 °C en todas las condiciones de combustión;
e) a la salida de la cámara secundaria, los gases de escape deberán pasar a través de un regulador de tiro situado en la base de la chimenea, que los enfríe y diluya con el aire ambiente, manteniendo una presión constante en las cámaras primaria y secundaria;
f) el proceso deberá realizarse durante un ciclo de 24 horas que incluye la carga, el tratamiento, el enfriamiento y la retirada de las cenizas. Al final del ciclo, las cenizas residuales deberán retirarse de la cámara primaria mediante un sistema de aspiración en sacos cerrados, que se sellan posteriormente antes de ser transportados;
g) no deberá permitirse la gasificación de otro material que no sean subproductos animales.
F. Combustión de grasa animal en un proceso de caldera térmica
1. Materia prima
Para este proceso, podrá utilizarse una fracción grasa derivada de subproductos animales de cualquier categoría.
2. Método de tratamiento
La combustión de grasa animal en una caldera térmica se realizará de conformidad con las siguientes normas de transformación:
a) salvo cuando se use aceite de pescado o grasas extraídas, que hayan sido producidos de conformidad con las secciones VIII o XII del anexo III del Reglamento (CE) nº 853/2004, respectivamente, la fracción grasa derivada de los subproductos animales deberá transformarse en primer lugar utilizando:
i) en el caso de fracción grasa de materiales de las categorías 1 y 2 destinada a su combustión en otra planta,
- para la fracción grasa resultante de la transformación de rumiantes sometidos a pruebas de diagnóstico con resultado negativo de conformidad con el artículo 6, apartado 1, del Reglamento (CE) nº 999/2001 y de la transformación de animales distintos de rumiantes que precisen pruebas de diagnóstico de EET, cualquiera de los métodos de transformación 1 a 5 mencionados en el capítulo III del presente anexo;
- para la fracción grasa resultante de la transformación de otros rumiantes, el método de transformación 1 mencionado en el capítulo III, y
ii) en el caso de materiales de las categorías 1 y 2 destinados a la combustión dentro de la misma planta y en el caso de materiales de la categoría 3, cualquiera de los métodos de transformación 1 a 5 o el método de transformación 7; en el caso de materiales derivados de peces, los métodos de transformación 1 a 7 mencionados en el capítulo III;
b) la fracción grasa deberá separarse de la proteína y en el caso de grasa de origen de rumiantes destinada a su combustión en otra planta, deberán eliminarse las impurezas insolubles hasta un nivel que no supere el 0,15 % del peso;
c) tras el proceso mencionado en las letras a) y b), la grasa deberá:
i) vaporizarse en una caldera generadora de vapor y quemarse a una temperatura mínima de 1100 °C durante al menos 0,2 segundos, o
ii) transformarse aplicando parámetros equivalentes que hayan sido autorizados por la autoridad competente;
d) no deberá permitirse la combustión de otro material de origen animal que no sea grasa animal;
e) la combustión de la grasa derivada de material de las categorías 1 y 2 deberá efectuarse en la misma instalación en la que se extraiga la grasa, con el fin de utilizar la energía generada para los procesos de extracción. No obstante, la autoridad competente podrá autorizar el traslado de esa grasa a otras instalaciones para su combustión, siempre que:
i) la planta de destino esté autorizada para la combustión;
ii) la transformación de alimentos o piensos en los mismos locales de una planta autorizada se efectúa en estrictas condiciones de separación;
f) la combustión deberá realizarse de conformidad con la legislación de la Unión relacionada con la protección del medio ambiente, en particular, con referencia a las normas previstas en dicha legislación respecto a las mejores técnicas disponibles para el control y seguimiento de emisiones.
G. Proceso de producción termomecánica de biocombustible
1. Materia prima
Para este proceso, podrán utilizarse estiércoles y contenido del tubo digestivo y materiales de la categoría 3.
2. Método de tratamiento
La producción termomecánica de biocombustible se realizará conforme a las siguientes normas de transformación:
a) los subproductos animales deberán introducirse en un convertidor y, posteriormente, tratarse a una temperatura de 80 °C durante ocho horas. Durante este período, el material deberá reducirse constantemente de tamaño mediante un equipo adecuado de abrasión mecánica;
b) el material deberá tratarse posteriormente a una temperatura de 100 °C durante al menos dos horas;
c) el tamaño de las partículas del material resultante no debe superar los 20 mm;
d) los subproductos animales deberán tratarse de forma que los requisitos relativos al tiempo, la temperatura y la presión establecidos en las letras a) y b) se satisfagan simultáneamente;
e) durante el tratamiento térmico del material, el agua evaporada deberá extraerse constantemente del espacio por encima del biocombustible y pasarse a través de un condensador de acero inoxidable. El vapor condensado deberá mantenerse a una temperatura de al menos 70 °C durante al menos una hora antes de verterse como agua residual;
f) tras el tratamiento térmico del material, el biocombustible resultante procedente del convertidor deberá verterse y transportarse automáticamente mediante una cinta transportadora totalmente cubierta y cerrada para su incineración o coincineración en la misma instalación;
g) el proceso deberá llevarse a cabo por lotes.
1. Los productos derivados de la transformación de
a) materiales de la categoría 1 deberán:
i) eliminarse de conformidad con lo establecido en el artículo 12, letras a) o b), del Reglamento (CE) nº 1069/2009;
ii) eliminarse por enterramiento en un vertedero autorizado;
iii) transformarse en biogás, a condición de que los residuos de la digestión sean eliminados de conformidad con los apartados i) o ii), o
iv) transformarse nuevamente en derivados de grasas para usos diferentes a la alimentación animal.
b) materiales de las categorías 2 o 3 deberán:
i) eliminarse de conformidad con lo establecido en el punto 1, letra a), inciso i) o ii), con o sin procesamiento previo conforme a lo dispuesto en el artículo 12, letras a) y b), del Reglamento (CE) nº 1069/2009;
ii) transformarse nuevamente en derivados de grasas para usos diferentes a la alimentación animal;
iii) emplearse como abono o enmienda de suelo de origen orgánico, o
iv) transformarse en compost o biogás.
2. Los materiales resultantes de la transformación de conformidad con:
a) el proceso de hidrólisis alcalina definido en la letra A de la sección 2, podrán transformarse en una planta de biogás y quemarse rápidamente a un mínimo de 900 °C y, a continuación, refrigerarse rápidamente ("enfriamiento"); cuando se haya empleado como materia prima el material mencionado en el artículo 8, letras a) y b), del Reglamento (CE) nº 1069/2009, la transformación en biogás tendrá lugar en el mismo emplazamiento en el que se realiza la transformación y en un sistema cerrado;
b) el proceso de producción de biodiésel, podrán:
i) en el caso de biodiésel y de residuos de la destilación del biodiésel, emplearse como combustible sin restricciones con arreglo al presente Reglamento (punto final);
ii) en el caso de sulfato de potasio, emplearse para la producción de productos derivados para su aplicación a la tierra;
iii) en el caso de glicerina:
- derivada de material de las categorías 1 o 2 que haya sido transformada con arreglo al método de transformación 1 definido en el capítulo III, transformarse en biogás;
- derivada de material de la categoría 3, emplearse para la alimentación de animales.
3. Todos los residuos resultantes de la transformación de subproductos animales de conformidad con la presente sección, como lodos, sedimentos de filtros, cenizas y residuos de fermentación, se eliminarán conforme a lo dispuesto en el Reglamento (CE) nº 1069/2009 y en el presente Reglamento.
1. Las plantas de biogás estarán equipadas con una unidad de pasteurización/higienización de paso obligatorio para los subproductos animales o productos derivados introducidos con una dimensión granulométrica máxima antes de entrar en la unidad de 12 mm, con:
a) instalaciones para controlar que se alcanza la temperatura de 70 °C durante una hora;
b) dispositivos que registren de forma continua los resultados de las mediciones de control contempladas en la letra a), y
c) un sistema adecuado para evitar un calentamiento insuficiente.
2. No obstante lo dispuesto en el punto 1, no será obligatoria una unidad de pasteurización/higienización para las plantas de biogás que solo transformen:
a) material de la categoría 2 que haya sido transformado con arreglo al método de transformación 1 definido en el capítulo III del anexo IV;
b) material de la categoría 3 que haya sido transformado con arreglo a uno de los métodos de transformación 1 a 5 o al método de transformación 7 o, en el caso de material procedente de animales acuáticos, a uno de los métodos de transformación 1 a 7, conforme a lo dispuesto en el capítulo III del anexo IV;
c) material de la categoría 3 que haya sido sometido a pasteurización/higienización en otra planta autorizada;
d) subproductos animales que pueden ser utilizados como materia prima sin transformación con arreglo al artículo 13, letra e), inciso ii), del Reglamento (CE) nº 1069/2009 y al presente Reglamento;
e) subproductos animales que han sido sometidos al proceso de hidrólisis alcalina definido en la letra A de la sección 2 del capítulo IV del anexo IV;
f) los siguientes subproductos animales, si lo autoriza la autoridad competente:
i) los subproductos animales mencionados en el artículo 10, letra f), del Reglamento (CE) nº 1069/2009, que hayan sido transformados conforme a lo definido en el artículo 2, apartado 1, letra m), del Reglamento (CE) nº 852/2004 en el momento en el que se destinan a fines distintos del consumo humano;
ii) los subproductos animales a que se refiere el artículo 10, letra g), del Reglamento (CEE) nº 1069/2009, o
iii) subproductos animales que se transformen en biogás, donde los residuos de la digestión son sometidos posteriormente a compostaje o transformados o eliminados de conformidad con el presente Reglamento.
3. Si la planta de biogás se encuentra cerca o dentro de las instalaciones en las que se mantienen animales de granja y no usa exclusivamente estiércol, leche o calostro procedente de dichos animales, la planta estará ubicada a cierta distancia de la zona en la que se mantienen animales de ese tipo.
Esa distancia se determinará de forma que se garantice que no existe ningún riesgo inaceptable de transmisión de enfermedades transmisibles a personas o animales desde la planta de biogás.
En todo caso, deberá haber una separación física total entre la planta de biogás y los animales, su pienso y sus camas, con vallas en caso necesario.
4. Cada planta de biogás deberá disponer de su propio laboratorio o recurrir a un laboratorio externo. El laboratorio deberá estar equipado para realizar los análisis necesarios y estar autorizado por la autoridad competente, acreditado conforme a las normas internacionalmente reconocidas o someterse a controles periódicos por parte de la autoridad competente.
1. Toda planta de compostaje estará equipada con un área cerrada o un reactor de compostaje cerrado de paso obligatorio para los subproductos animales o productos derivados introducidos en la planta, con:
a) instalaciones para comprobar la evolución de la temperatura a lo largo del tiempo;
b) dispositivos que registren, de forma continua cuando proceda, los resultados de las mediciones de control contempladas en el apartado a);
c) un sistema de seguridad adecuado para evitar un calentamiento insuficiente.
2. No obstante lo dispuesto en el apartado 1, podrán autorizarse otros sistemas de compostaje a condición de que:
a) se manejen de manera que todo el material del sistema alcance los parámetros de tiempo y temperatura exigidos, si es necesario mediante una supervisión continua de los parámetros, o
b) transformen exclusivamente materiales mencionados en el punto 2 de la sección 1, y
c) cumplan todos los demás requisitos pertinentes del presente Reglamento.
3. Si la planta de compostaje se encuentra cerca o dentro de las instalaciones en las que se mantienen animales de granja y no usa exclusivamente estiércol, leche o calostro procedente de dichos animales, la planta de compostaje estará ubicada a cierta distancia de la zona en la que se mantienen animales.
Esa distancia se determinará de forma que se garantice que no existe ningún riesgo inaceptable de transmisión de enfermedades transmisibles a personas o animales desde la planta de compostaje.
En todo caso, deberá haber una separación física total entre la planta de compostaje y los animales, su pienso y sus camas, con vallas en caso necesario.
4. Cada planta de compostaje deberá disponer de su propio laboratorio o recurrir a un laboratorio externo. El laboratorio deberá estar equipado para realizar los análisis necesarios y estar autorizado por la autoridad competente, acreditado conforme a las normas internacionalmente reconocidas o someterse a controles periódicos por parte de la autoridad competente.
1. Los subproductos animales deberán transformarse lo antes posible tras su llegada a la planta de biogás o de compostaje. Deberán almacenarse adecuadamente hasta su transformación.
2. Los contenedores, recipientes y vehículos utilizados para el transporte de material no tratado deberán limpiarse y desinfectarse en una zona designada a tal efecto.
Dicha zona estará situada o diseñada con el fin de prevenir el riesgo de contaminación de los productos transformados.
3. Se tomarán sistemáticamente medidas preventivas contra pájaros, roedores, insectos y otros parásitos.
Para ello, se aplicará un programa de control de plagas documentado.
4. Deberán fijarse y documentarse los procedimientos de limpieza para todas las zonas de las instalaciones. Deberá disponerse de equipos y agentes de limpieza adecuados.
5. El control de la higiene deberá incluir inspecciones periódicas del entorno y el equipo. Deberán documentarse los programas de inspección y sus resultados.
6. Las instalaciones y el equipo deberán mantenerse en buen estado de conservación; el equipo de medición deberá calibrarse periódicamente.
7. Los residuos de fermentación y el compost deberán manipularse y almacenarse en la planta de biogás o de compostaje mediante procedimientos que excluyan su recontaminación.
1. El material de la categoría 3 utilizado como materia prima en una planta de biogás equipada con una unidad de pasteurización/higienización deberá cumplir las siguientes condiciones mínimas:
a) dimensión granulométrica máxima antes de entrar en la unidad: 12 mm;
b) temperatura mínima de todo el material en la unidad: 70 °C; y
c) permanencia mínima en la unidad sin interrupción: 60 minutos.
Sin embargo, la leche, los productos lácteos, los productos derivados de la leche, los calostros y productos a base de calostro de la categoría 3 podrán utilizarse sin pasteurización/higienización como materia prima en una planta de biogás si la autoridad competente considera que no plantean un riesgo de propagación de ninguna enfermedad transmisible grave para personas o animales.
Los requisitos mínimos definidos en las letras b) y c) del presente párrafo se aplicarán igualmente al material de la categoría 2 que se introduce en la planta de biogás sin transformación previa con arreglo al artículo 13, letra e), inciso ii), del Reglamento (CE) nº 1069/2009.
2. El material de la categoría 3 utilizado como materia prima en las plantas de compostaje deberá cumplir las siguientes condiciones mínimas:
a) dimensión granulométrica máxima antes de entrar en el reactor de compostaje: 12 mm;
b) temperatura mínima de todo el material en el reactor: 70 °C; y
c) permanencia mínima sin interrupción: 60 minutos.
Los requisitos mínimos definidos en las letras b) y c) del presente párrafo se aplicarán igualmente al material de la categoría 2 que se compostan sin transformación previa con arreglo al artículo 13, letra e), inciso ii), del Reglamento (CE) nº 1069/2009.
1. La autoridad competente podrá autorizar el uso de parámetros distintos de los definidos en el punto 1 de la sección 1 del capítulo 1 y distintos de los parámetros estándar de transformación, a condición de que el interesado que solicite su uso demuestre que garantizan una atenuación adecuada de los riesgos biológicos. La demostración incluirá una validación, que se llevará a cabo conforme a los siguientes requisitos:
a) identificación y análisis de los riesgos, incluido el impacto del material aportado, basándose en una descripción completa de las condiciones y parámetros de transformación;
b) una determinación del riesgo que evalúe cómo se alcanzan en la práctica, en situaciones normales y atípicas, las condiciones de transformación específicas contempladas en la letra a);
c) validación del proceso previsto, midiendo la reducción de la viabilidad/infecciosidad de:
i) los organismos indicadores endógenos durante el proceso, cuando el indicador:
- está constantemente presente en la materia prima, en altos niveles,
- no es menos termorresistente a los aspectos letales del proceso de transformación, pero tampoco más significativamente resistente que los patógenos para los que se usa como control;
- es relativamente fácil de cuantificar, identificar y confirmar, o
ii) un organismo o virus de ensayo caracterizado, durante la exposición, introducido en la materia prima en un organismo de control adecuado;
d) la validación del proceso previsto contemplado en la letra c) debe demostrar que el proceso consigue la reducción global del riesgo siguiente:
i) por lo que se refiere a los procesos térmicos y químicos, mediante:
- una reducción de 5 log10 de Enterococcus faecalis o Salmonella Senftenberg (775W, H2S negativa);
- una reducción del título de infecciosidad de virus termorresistentes como los parvovirus de al menos 3 log10, cuando se identifiquen como un peligro pertinente, y
ii) por lo que se refiere a los procesos químicos:
- una reducción de parásitos resistentes como los huevos de Ascaris sp. de al menos el 99,9 % (3 log10) de fases viables;
e) concepción de un programa completo de control que incluya procedimientos para controlar el funcionamiento de los procesos contemplados en la letra c);
f) medidas que garanticen la vigilancia y supervisión continuas de los parámetros pertinentes del proceso fijados en el programa de control durante el funcionamiento de la planta.
Deberán recogerse y conservarse datos de los parámetros pertinentes del proceso utilizados en las plantas de biogás o de compostaje, así como otros puntos críticos de control, de forma que el propietario, el encargado o su representante y la autoridad competente puedan controlar el funcionamiento de la planta.
El explotador deberá facilitar a la autoridad competente los registros cuando los solicite. La información relativa a un proceso autorizado en virtud de este párrafo deberá entregarse a la Comisión previa solicitud.
2. No obstante lo dispuesto en el punto 1, a la espera de la adopción de las normas indicadas en el artículo 15, apartado 2, letra a), inciso ii), del Reglamento (CE) nº 1069/2009, la autoridad competente podrá autorizar el uso de otros requisitos especiales distintos de los establecidos en el presente capítulo, a condición de que garanticen un efecto equivalente respecto a la reducción de patógenos, para:
a) residuos de cocina empleados como único subproducto animal en la planta de biogás o de compostaje, y
b) mezclas de residuos de cocina con los siguientes materiales:
i) estiércol
ii) contenido del tubo digestivo separado del tubo digestivo;
iii) leche;
iv) productos lácteos;
v) productos derivados de la leche;
vi) calostro;
vii) productos a base de calostro;
viii) los huevos,
ix) ovoproductos;
x) subproductos animales contemplados en el artículo 10, letra f), del Reglamento (CE) nº 1069/2009, que se han transformado con arreglo a lo dispuesto en el artículo 2, apartado 1, letra m), del Reglamento (CE) nº 852/2004.
3. Cuando los materiales mencionados en el punto 2, letra b), o los productos derivados mencionados en el artículo 10, letra g), del Reglamento (CE) nº 1069/2009, son la única materia prima de origen animal sometida a tratamiento en la planta de biogás o de compostaje, la autoridad competente podrá autorizar el uso de otros requisitos específicos distintos de los contemplados en el presente capítulo, a condición de que:
a) no considere que dichos materiales puedan plantear un riesgo de propagación de ninguna enfermedad transmisible grave a personas o animales;
b) considere que los residuos de fermentación o compost son material sin transformar y obligue a los explotadores a manipularlos con arreglo a lo dispuesto en el Reglamento (CE) nº 1069/2009 y en el presente Reglamento.
4. Los explotadores podrán comercializar residuos de fermentación y el compost que se hayan obtenido de conformidad con los parámetros autorizados por la autoridad competente:
a) de acuerdo con el punto 1;
b) de acuerdo con los puntos 2 y 3, solamente dentro de las fronteras del Estado miembro en el que se han autorizado tales parámetros.
1. a) Las muestras representativas de los residuos de fermentación o de compost tomadas durante o inmediatamente después de su transformación en la planta de biogás o de su compostaje en la planta de compostaje para controlar el proceso deberán cumplir las normas siguientes:
Escherichia coli: n = 5, c = 1, m = 1000, M = 5000 en 1 g;
o
Enterococcaceae: n = 5, c = 1, m = 1000, M = 5000 en 1 g;
y
b) las muestras representativas de los residuos de fermentación o de compost tomadas durante el almacenamiento o en el momento de la salida del almacén deberán cumplir las normas siguientes:
Salmonella: ausente en 25 g: n = 5; c = 0; m = 0; M = 0
cuando en el caso de las letras a) o b):
n = número de muestras del ensayo;
m = valor umbral del número de bacterias; el resultado se considera satisfactorio si el número de bacterias en todas las muestras no es superior a m;
M = valor máximo del número de bacterias; el resultado se considera insatisfactorio si el número de bacterias en una o más muestras es igual o superior a M; y
c = número de muestras cuyo recuento de bacterias puede situarse entre m y M; la muestra sigue considerándose aceptable si el recuento de bacterias de las demás muestras es igual o inferior a m;
2. Los residuos de fermentación y el compost que no cumplan las condiciones establecidas en esta sección serán sometidos de nuevo a transformación o compostaje, y en caso de presencia de Salmonella serán tratados o eliminados conforme a las instrucciones de la autoridad competente.
1. Los explotadores garantizarán que los envíos de muestras para diagnóstico e investigación van acompañados de un documento comercial que debe indicar:
a) la descripción del material y la especie animal de origen;
b) la categoría del material;
c) la cantidad de material;
d) el lugar de origen y el lugar de envío del material;
e) el nombre y la dirección del expedidor;
f) el nombre y la dirección del destinatario y/o usuario.
2. Los usuarios que manipulen muestras para diagnóstico e investigación adoptarán todas las medidas necesarias para impedir la propagación de enfermedades transmisibles a personas o animales durante la manipulación de los materiales bajo su control, en particular por medio de la aplicación de buenas prácticas de laboratorio.
3. Estará prohibido todo uso posterior de las muestras para diagnóstico e investigación para fines distintos de los indicados en el punto 38 del anexo I.
4. Salvo cuando se conserven por motivos de referencia, las muestras para diagnóstico e investigación y cualquier producto derivado del uso de dichas muestras se eliminarán:
a) como residuo mediante incineración o coincineración;
b) en caso de los subproductos animales o productos derivados mencionados en el artículo 8, letra a), inciso iv), el artículo 8, letras c) y d), y en los artículos 9 y 10, del Reglamento (CE) nº 1069/2009 que formen parte de cultivos celulares, equipos de laboratorio o muestras de laboratorio, por medio de un tratamiento cuyas condiciones sean equivalentes, como mínimo, al método validado para autoclaves de vapor [1] y posterior eliminación como residuo o aguas residuales de conformidad con la legislación relevante de la Unión;
c) por esterilización a presión y posterior eliminación o uso de conformidad con lo dispuesto en los artículos 12, 13 y 14, del Reglamento (CE) nº 1069/2009.
5. Los usuarios que manipulen muestras para diagnóstico e investigación llevarán un registro de los envíos de dichas muestras.
Dicho registro incluirá la información contemplada en el punto 1, así como la fecha y el método de eliminación de las muestras y de todo producto derivado.
6. No obstante lo dispuesto en los puntos 1, 4 y 5, la autoridad competente podrá aceptar la manipulación y eliminación de muestras para diagnóstico e investigación con fines educativos en otras condiciones que garanticen que no surgen riesgos inaceptables para la salud pública y animal.
1. Las muestras comerciales y objetos de exposición podrán transportarse, usarse y eliminarse únicamente conforme a lo dispuesto en los puntos 1 a 4 y 6 de la sección 1.
2. Salvo cuando las muestras comerciales se conserven con fines de referencia, y tras haber realizado los estudios o análisis específicos, serán:
a) devueltas al Estado miembro de origen;
b) enviadas a otro Estado miembro o tercer país, siempre que el envío sea previamente autorizado por la autoridad competente del Estado miembro o tercer país de destino, o
c) eliminadas o empleadas de conformidad con lo establecido en los artículos 12, 13 y 14 del Reglamento (CE) nº 1069/2009.
3. Una vez concluida la exposición o actividad artística, los artículos de exposición serán devueltos al Estado miembro de origen, enviados o eliminados, conforme a lo dispuesto en el punto 2.
Los materiales de las categorías 2 y 3 a los que hace referencia el artículo 18, apartado 1, del Reglamento (CE) nº 1069/2009 pueden utilizarse como alimento para los animales contemplados en el apartado 1, letras a), d), f), g) y h) del mismo artículo, a condición del cumplimiento de las siguientes condiciones mínimas, además de cualquier condición establecida por la autoridad competente de conformidad con el artículo 18, apartado 1, del Reglamento:
1. Los subproductos animales serán transportados hasta los usuarios o hasta los centros de recogida con arreglo a las secciones 1 y 3 del capítulo I del anexo VIII.
2. La autoridad competente procederá al registro de los centros de recogida siempre que:
a) cumplan las condiciones para plantas que realizan operaciones intermedias definidas en el capítulo II del anexo IX, y
b) dispongan de las instalaciones adecuadas para la destrucción de material no utilizado, o envíen ese material a una planta de transformación autorizada o a una planta de incineración o coincineración autorizada conforme a lo dispuesto en el presente Reglamento.
3. Los Estados miembros podrán autorizar que una planta de transformación de material de la categoría 2 sea utilizada como centro de recogida.
4. Los explotadores de centros de recogida que suministren a usuarios finales materiales distintos de los subproductos animales procedentes de animales acuáticos y de animales invertebrados acuáticos, deben garantizar que dichos materiales han sido sometidos a uno de los tratamientos siguientes:
a) desnaturalización con una solución de un agente colorante; la solución deberá tener una concentración tal que la coloración sea claramente visible en el material tratado y no desaparezca al congelar o refrigerar el material, y toda la superficie de todos los trozos de material deberá haber sido cubierta por la solución, bien por inmersión del material en la solución, bien por pulverización o cualquier otro modo de aplicación de la solución,
b) esterilización por cocción mediante agua o vapor a presión hasta que todos los trozos de material estén totalmente cocidos, o
c) cualquier otro tratamiento o manipulación autorizado por la autoridad competente responsable del explotador.
1. La autoridad competente podrá autorizar el uso de material de la categoría 1 contemplado en el artículo 18, apartado 2, letra b), del Reglamento (CE) nº 1069/2009 para la alimentación de las siguientes especies protegidas y en peligro, en comederos bajo las siguientes condiciones:
a) el material deberá servir de alimentación a:
i) alguna de las siguientes especies de aves necrófagas en los siguientes Estados miembros:
|
Estado miembro |
Especie animal |
|
Bulgaria |
quebrantahuesos (Gypaetus barbatus) buitre negro (Aegypius monachus) alimoche (Neophron percnopterus) buitre leonado (Gyps fulvus) águila real (Aquila chrysaetos) águila imperial (Aquila heliaca) pigargo europeo (Haliaeetus albicilla) milano negro (Milvus migrans) milano real (Milvus milvus) |
|
Grecia |
quebrantahuesos (Gypaetus barbatus) buitre negro (Aegypius monachus) alimoche (Neophron percnopterus) buitre leonado (Gyps fulvus) águila real (Aquila chrysaetos) águila imperial (Aquila heliaca) pigargo europeo (Haliaeetus albicilla) milano negro (Milvus migrans) |
|
España |
quebrantahuesos (Gypaetus barbatus) buitre negro (Aegypius monachus) alimoche (Neophron percnopterus) buitre leonado (Gyps fulvus) águila real (Aquila chrysaetos) águila imperial ibérica (Aquila adalberti) milano negro (Milvus migrans) milano real (Milvus milvus) |
|
Francia |
quebrantahuesos (Gypaetus barbatus) buitre negro (Aegypius monachus) alimoche (Neophron percnopterus) buitre leonado (Gyps fulvus) águila real (Aquila chrysaetos) pigargo europeo (Haliaeetus albicilla) milano negro (Milvus migrans) milano real (Milvus milvus) |
|
Italia |
quebrantahuesos (Gypaetus barbatus) buitre negro (Aegypius monachus) alimoche (Neophron percnopterus) buitre leonado (Gyps fulvus) águila real (Aquila chrysaetos) milano negro (Milvus migrans) milano real (Milvus milvus) |
|
Chipre |
buitre negro (Aegypius monachus) buitre leonado (Gyps fulvus) |
|
Portugal |
buitre negro (Aegypius monachus) alimoche (Neophron percnopterus) buitre leonado (Gyps fulvus) águila real (Aquila chrysaetos) |
|
Eslovaquia |
águila real (Aquila chrysaetos) águila imperial (Aquila heliaca) pigargo europeo (Haliaeetus albicilla) milano negro (Milvus migrans) milano real (Milvus milvus) |
ii) alguna de las especies del orden Carnivora que figuran en el anexo II de la Directiva 92/43/CEE, en zonas de conservación especial creadas con arreglo a dicha Directiva, o
iii) alguna de las especies de de los órdenes Falconiformes o Strigiformes que figuran en el anexo I de la Directiva 2009/147/CE, en zonas de protección especial creadas con arreglo a dicha Directiva;
b) la autoridad competente ha concedido autorización al explotador responsable del comedero;
La autoridad competente concederá dicha autorización a condición de que:
i) la alimentación no se utilice como una forma alternativa de eliminar material especificado de riesgo o de rumiantes muertos que lo contengan que supongan un riesgo de EET;
ii) apliquen un sistema de vigilancia adecuado de las EET con arreglo a lo dispuesto en el Reglamento (CE) nº 999/2001, que incluya el análisis periódico de muestras en un laboratorio para la detección de EET;
c) la autoridad competente deberá velar por su coordinación con cualquier otra autoridad competente responsable de la supervisión de los requisitos estipulados en la autorización;
d) La autoridad competente tendrá la seguridad, de conformidad con una evaluación de la situación específica de las especies en cuestión y sus hábitats, de que se mejorará la situación de conservación de la especie.
e) la autorización concedida por la autoridad competente deberá:
i) referirse a las especies objetivo y nombrarlas;
ii) describir detalladamente la ubicación del comedero en la zona geográfica donde tendrá lugar la alimentación, y
iii) suspenderse inmediatamente si:
- se sospecha o confirma una relación con la propagación de EET, hasta que pueda descartarse el riesgo, o
- no se cumple alguna de las disposiciones del presente Reglamento;
f) el operador responsable de la alimentación deberá:
i) acondicionar una zona para la alimentación cerrada cuyo acceso esté limitado a los animales de la especie que se desea conservar, si fuera necesario por medio de vallas y otros medios adecuados a las pautas de alimentación natural de esas especies;
ii) garantizar que los cuerpos elegibles de bovinos y un 4 % como mínimo de los cuerpos elegibles de ovinos y caprinos que se vayan a utilizar como alimento obtengan un resultado negativo en pruebas previas del programa de seguimiento de las EET realizadas con arreglo al anexo III del Reglamento (CE) nº 999/2001 y, si procede, con arreglo a una Decisión adoptada de conformidad con el artículo 6, apartado 1, letra b), párrafo segundo, de dicho Reglamento, y
iii) llevar un registro, como mínimo, del número, la naturaleza, el peso estimado y el origen de los cadáveres de animales utilizados como alimento, la fecha de la alimentación, el lugar donde ésta tuvo lugar y, si procede, el resultado de las pruebas de detección de EET.
2. Los Estados miembros que soliciten a la Comisión su inclusión en la lista mencionada en la letra a) del punto 1 deberán presentar:
a) una justificación detallada para la ampliación de la lista a determinadas especies de aves necrófagas en dicho Estado miembro, exponiendo los motivos por los cuales es necesario alimentar dichas aves con materiales de la categoría 1 en lugar de hacerlo con materiales de las categorías 2 y 3;
b) una explicación de las medidas que se adoptarán para garantizar el cumplimiento de lo dispuesto en el punto 1.
La autoridad competente podrá autorizar el uso de materiales de la categoría 1 consistentes en cuerpos enteros o partes de animales muertos que contengan material especificado de riesgo fuera de los comederos, sin la previa recogida de los animales muertos cuando proceda, para la alimentación de los animales silvestres mencionados en el punto 1, letra a), de la sección 2, en las siguientes condiciones:
1. La autoridad competente tendrá la seguridad de conformidad con una evaluación de la situación específica de las especies en cuestión y sus hábitats, de que se mejorará la situación de conservación de la especie.
2. En la autorización, la autoridad competente deberá identificar explotaciones o rebaños dentro de una zona de alimentación geográficamente definida y bajo las siguientes condiciones:
a) la zona de alimentación no deberá extenderse a zonas en las que haya ganadería intensiva;
b) los animales de granja en explotaciones o rebaños dentro de la zona de alimentación deberán hallarse bajo la vigilancia periódica de un veterinario oficial respecto de la prevalencia de las EET y de enfermedades transmisibles a personas o animales;
c) la alimentación deberá suspenderse inmediatamente si:
i) se sospecha o confirma una relación con la propagación de EET en una explotación o rebaño, hasta que pueda descartarse el riesgo;
ii) se sospecha o confirma un brote de una enfermedad grave transmisible a personas o animales en una explotación o rebaño, hasta que pueda descartarse el riesgo, o
iii) no se cumple alguna de las disposiciones del presente Reglamento;
d) la autoridad competente deberá especificar en la autorización:
i) las medidas adoptadas para evitar la transmisión de EET y de enfermedades transmisibles de animales muertos a personas o animales, como medidas específicas sobre pautas de alimentación de las especies que se desea conservar, restricciones estacionales de alimentación, restricciones de circulación de animales de granja y otras medidas destinadas a controlar los riesgos de transmisión de una enfermedad transmisible a personas o animales, como medidas relacionadas con las especies presentes en la zona de alimentación para cuya alimentación no se utilizan los subproductos animales;
ii) las responsabilidades de las personas o entidades dentro de la zona de alimentación que colaboran con la alimentación o son responsables de los animales de granja, en relación con las medidas mencionadas en el inciso i) anterior;
iii) las condiciones para la imposición de sanciones mencionadas en el artículo 53 del Reglamento (CE) nº 1069/2009 aplicables a las infracciones de las medidas contempladas en el inciso i) por las personas o entidades mencionadas en el inciso ii) de la presente letra d);
e) en caso de que la alimentación se lleve a cabo sin la previa recogida de los animales muertos, deberá realizarse una estimación de la tasa probable de mortalidad de los animales de granja dentro de la zona de alimentación y de las necesidades probables de alimentación de los animales silvestres, de conformidad con la determinación de los riesgos posibles de transmisión de enfermedades.
La autoridad competente podrá autorizar el uso de materiales de la categoría 1 consistentes en cuerpos enteros o partes de animales muertos que contengan material especificado de riesgo y el uso de materiales derivados de animales de zoológico, para la alimentación de animales de zoológico en las siguientes condiciones:
a) la autoridad competente deberá haber concedido autorización al explotador responsable de la alimentación. La autoridad competente concederá dicha autorización a condición de que:
i) la alimentación no se utilice como una forma alternativa de eliminar material especificado de riesgo o de rumiantes muertos que lo contengan que supongan un riesgo de EET;
ii) cuando se usen materiales de la categoría 1 consistentes en cuerpos enteros o partes de animales muertos que contengan material especificado de riesgo procedentes de bovinos, se aplique un sistema de vigilancia adecuado de las EET con arreglo a lo dispuesto en el Reglamento (CE) nº 999/2001, que incluya el análisis periódico de muestras en un laboratorio para la detección de EET;
b) la autorización concedida por la autoridad competente deberá suspenderse inmediatamente en caso de que:
i) se sospeche o confirme una relación con la propagación de EET, hasta que pueda descartarse el riesgo, o
ii) no se cumpla alguna de las disposiciones del presente Reglamento;
c) el operador responsable de la alimentación deberá:
i) almacenar el material que prevé emplear para la alimentación y llevar a cabo dicha alimentación en una zona cerrada y vallada para garantizar que no tenga acceso a dicho material ningún otro animal carnívoro distinto de los animales de zoológico para cuya alimentación se ha concedido la autorización;
ii) garantizar que los rumiantes que se vayan a utilizar como alimento se someten a un programa de seguimiento de las EET llevado a cabo con arreglo al anexo III del Reglamento (CE) nº 999/2001 y, de ser aplicable, con arreglo a una Decisión adoptada de conformidad con el artículo 6, apartado 1, letra b), párrafo segundo del citado Reglamento, y
iii) llevar un registro, como mínimo, del número, la naturaleza, el peso estimado y el origen de los cuerpos de los animales utilizados como alimento, el resultado de las pruebas de detección de EET y la fecha de la alimentación.
1. Cuando la autoridad competente autorice la eliminación de los subproductos animales in situ con arreglo a lo dispuesto en el artículo 19, apartado 1, letras a), b), c) y e), del Reglamento (CE) nº 1069/2009, la eliminación se podrá efectuar:
a) mediante incineración o enterramiento en los establecimientos en que se hayan originado;
b) en un vertedero autorizado, o
c) mediante incineración o enterramiento en un lugar que permita minimizar el riesgo para la salud pública o animal y el medio ambiente, a condición de que el lugar se encuentre a una distancia suficiente que permita a la autoridad competente gestionar la prevención del riesgo para la salud pública y animal y el medio ambiente.
2. La incineración de subproductos animales en los lugares mencionados en el artículo 19, apartado 1, letras b), c) y e), del Reglamento (CE) nº 1069/2009 debe realizarse de forma que se garantice su incineración:
a) en una pira construida adecuadamente y que los subproductos animales quedan reducidos a ceniza;
b) de manera que no entrañe un riesgo para la salud humana;
c) sin utilizar procedimientos o métodos que puedan dañar el medio ambiente, en concreto mediante riesgos para el agua, el aire, el suelo, las plantas y los animales, o por el ruido o los olores;
d) en condiciones que garanticen la eliminación de las cenizas resultantes por enterramiento en un vertedero autorizado.
3. El enterramiento de subproductos animales en los lugares recogidos en el artículo 19, apartado 1, letras a), b), c) y e), del Reglamento (CE) nº 1069/2009 debe realizarse de forma que se garantice su enterramiento:
a) de tal manera que los animales carnívoros u omnívoros no puedan acceder a ellos;
b) en un vertedero autorizado o en otro emplazamiento sin poner en peligro la salud humana y utilizando procedimientos o métodos que no dañen el medio ambiente, en concreto mediante riesgos para el agua, el aire, el suelo, las plantas y los animales, o por el ruido o los olores.
4. En el caso de eliminación con arreglo a lo dispuesto en el artículo 19, apartado 1, letras a), b), c) y e), del Reglamento (CE) nº 1069/2009, el traslado de los subproductos animales desde el lugar de origen hasta el lugar de eliminación debe realizarse de forma que:
a) se transporten en contenedores o vehículos seguros y estancos;
b) su carga y descarga sea supervisada por la propia autoridad competente, si procede;
c) se desinfecten las ruedas del vehículo antes de abandonar el lugar de origen;
d) los contenedores y vehículos utilizados para su transporte se limpien y desinfecten adecuadamente tras la descarga de los subproductos, y
e) los vehículos dispongan de escolta adecuada, controles de estanqueidad y dispongan de doble cubierta, si procede.
El porcentaje máximo mencionado en el artículo 19, apartado 2, del Reglamento (CE) nº 1069/2009 no superará los siguientes:
a) 10 % de la población bovina del Estado miembro en cuestión;
b) 25 % de la población ovina y caprina del Estado miembro en cuestión;
c) 10 % de la población porcina del Estado miembro en cuestión, y
d) un porcentaje de la población de otra especie determinado por la autoridad competente, de conformidad con una evaluación de los riesgos para la salud pública y la salud animal que se generan con la eliminación de animales de dicha especie por medio de incineración o enterramiento in situ.
La autoridad competente podrá autorizar la eliminación de abejas y subproductos apícolas mediante incineración o enterramiento in situ, a tenor de lo dispuesto en el artículo 19, apartado1, letra f), del Reglamento (CE) nº 1069/2009, a condición de que se adopten las medidas necesarias para que ello no suponga un riesgo para la salud humana o animal y el medio ambiente.
No obstante lo dispuesto en el artículo 14 del Reglamento (CE) nº 1069/2009, los Estados miembros podrán autorizar la recogida, transporte y eliminación de materiales de la categoría 3 contemplados en el artículo 10, letra f), de dicho Reglamento por otros medios distintos de la incineración o enterramiento in situ, a condición de que:
a) los materiales procedentes de un establecimiento o planta no superen un volumen de 20 kg por semana, independientemente de la especie de origen de los materiales;
b) los materiales se recojan, transporten y eliminen por medios que eviten la transmisión de riesgos inaceptables para la salud pública y la salud animal;
c) la autoridad competente realice controles periódicos, incluidos controles de los registros llevados por los explotadores en los establecimientos o plantas en los que se recogen los materiales, a fin de garantizar el cumplimiento de las disposiciones de la presente sección.
Los Estados miembros podrán optar por incrementar el volumen indicado en el apartado a) hasta un máximo de 50 kg por semana, tras presentar una justificación pormenorizada a la Comisión y a los restantes Estados miembros en el marco del Comité Permanente de la Cadena Alimentaria y de Sanidad Animal contemplado en el artículo 52, apartado 1, del Reglamento (CE) nº 1069/2009, donde se indique la naturaleza de las actividades para las cuales se incrementa el volumen, la especie de origen de los subproductos animales en cuestión, así como una explicación de los motivos por los cuales es necesario incrementar el volumen, considerando el sistema de manipulación y eliminación de subproductos animales y productos derivados en su territorio, según se contempla en el artículo 4, apartado 4, de dicho Reglamento.
[1] CEN TC/102 – Esterilizadores para uso médico – EN 285:2006 + A2:2009 – Esterilización. Esterilizadores de vapor. Esterilizadores grandes. Referencia publicada en el DO C 293 de 2.12.2009, p. 39.
1. Las solicitudes de autorización de un método alternativo de uso o eliminación de subproductos o productos derivados, a las que se hace referencia en el artículo 20 del Reglamento (CE) nº 1069/2009 (solicitudes) serán presentadas en una de las lenguas oficiales de la Unión Europea en virtud de lo dispuesto en el artículo 1 del Reglamento no 1 de 1958.
2. Las partes interesadas que presenten tal solicitud en una lengua distinta del inglés validarán la traducción oficial de su solicitud, facilitada por EFSA, antes de la evaluación.
El período mencionado en el artículo 20, apartado 5, del Reglamento (CE) nº 1069/2009 no comenzará hasta que la parte interesada haya validado la traducción oficial de la solicitud.
1. Las solicitudes contendrán toda la información necesaria sobre los siguientes aspectos, de forma que EFSA pueda valorar la seguridad de la propuesta de método alternativo:
a) las categorías de los subproductos animales que se pretenden someter al método alternativo, con referencia a las categorías mencionadas en los artículos 8, 9 y 10, del Reglamento (CE) nº 1069/2009;
b) la identificación y caracterización de los materiales de riesgo conforme a los siguientes principios:
Los materiales con un riesgo significativo deberán ser identificados de forma independiente. Deberá determinarse la probabilidad de exposición de personas o animales en condiciones de funcionamiento normales, anormales y de emergencia para cada material. En caso de exposición significativa, deberá evaluarse el posible riesgo;
c) la reducción de riesgos de agentes conforme a los siguientes principios:
La reducción del riesgo para la salud pública y la salud animal que puede lograrse con el proceso deberá estimarse mediante mediciones directas.
Si no hay mediciones directas disponibles, podrán usarse modelos o extrapolación de otros procesos. Deberá cuantificarse el peligro identificado (como Salmonella) tanto en el material (sin procesar) aportado como en el material resultante, con el objeto de demostrar la reducción efectiva del riesgo. A los efectos del presente capítulo, material resultante incluye cualquier producto final resultante del proceso y otros productos derivados del mismo.
Las estimaciones deberán ir acompañadas de pruebas: en el caso de las mediciones, información sobre la metodología empleada (sensibilidad y fiabilidad de los métodos empleados), naturaleza de las muestras analizadas y pruebas de la representatividad de las muestras (muestras reales relevantes, número de pruebas realizadas).
Si se utilizan sustitutos para la medición de priones, deberá aportarse una explicación de su relevancia. Será necesario facilitar una evaluación de la validez con las incertidumbres implicadas;
d) la contención de riesgos conforme a los siguientes principios:
Deberá analizarse la eficacia probable de las medidas técnicas empleadas para garantizar la contención de riesgos.
Dicho análisis deberá reflejar las condiciones de funcionamiento normales, anormales y de emergencia, incluida la interrupción del proceso.
Deberán especificarse los procedimientos de vigilancia y control que demuestren la contención.
Si no puede lograrse una contención plena, será necesaria una evaluación de todo posible riesgo;
e) la identificación de procesos interdependientes conforme a los siguientes principios:
Deberán evaluarse los posibles impactos indirectos que puedan afectar a la capacidad de reducción del riesgo de un proceso concreto.
Los impactos indirectos pueden provenir del transporte, el almacenamiento y la eliminación segura de los productos finales resultantes de un proceso o los subproductos derivados del mismo;
f) el uso final previsto de los productos finales y otros productos derivados conforme a los siguientes principios:
Deberá especificarse el uso final previsto de los productos finales y otros productos derivados obtenidos en un proceso.
Los riesgos probables involucrados que puedan afectar a la salud de personas y animales deberán calcularse a partir de la reducción estimada del riesgo con arreglo a lo dispuesto en el apartado c)
2. Las solicitudes deberán presentarse con documentos justificativos, en concreto un diagrama de flujo que muestre el funcionamiento del proceso, las pruebas mencionadas en el punto 1, letra c), así como otras pruebas que respalden las explicaciones aportadas conforme a lo dispuesto en el punto 1.
3. Las solicitudes incluirán una dirección de contacto de la parte interesada, con mención del nombre y dirección completa, números de teléfono, fax y/o dirección de correo electrónico de la persona de contacto individual responsable o representante de la parte interesada.
1. Los subproductos animales y productos derivados deberán recogerse y transportarse en envases nuevos sellados o vehículos o contenedores a prueba de fugas desde el punto de partida de la cadena de fabricación definido en el artículo 4, apartado 1, del Reglamento (CE) nº 1069/2009.
2. Los vehículos y contenedores reutilizables, así como todos los elementos reutilizables del equipo o de los instrumentos que entren en contacto con subproductos animales o productos derivados, distintos de los productos derivados comercializados con arreglo al Reglamento (CE) nº 767/2009, almacenados y transportados con arreglo al anexo II del Reglamento (CE) nº 183/2005, deberán mantenerse limpios.
En particular, salvo cuando se dediquen al transporte de un determinado subproducto animal o producto derivado y con el propósito de evitar la contaminación cruzada, deberán:
a) limpiarse y secarse antes de usarlos, y
b) limpiarse, lavarse y/o desinfectarse después de cada uso siempre que sea necesario para evitar la contaminación cruzada.
3. Los contenedores reutilizables deberán dedicarse al transporte de un determinado subproducto animal o producto derivado siempre que sea necesario para evitar la contaminación cruzada.
No obstante, podrán utilizarse contenedores reutilizables a condición de que la autoridad competente haya autorizado dicho uso:
a) para el transporte de diferentes subproductos animales o productos derivados a condición de que sean limpiados y desinfectados entre los distintos usos para evitar la contaminación cruzada;
b) para el transporte de subproductos animales o productos derivados mencionados en el artículo 10, letra f), del Reglamento (CE) nº 1069/2009, después de su uso para el transporte de productos destinados al consumo humano, en condiciones que impidan la contaminación cruzada.
4. El material de embalaje debe eliminarse, por incineración o por otro medio, con arreglo a la legislación de la Unión.
1. El transporte de subproductos animales destinados a la elaboración de piensos o alimentos crudos para animales de compañía debe efectuarse a una temperatura apropiada, en el caso de los subproductos animales derivados de la carne y productos de la carne destinados a fines distintos del consumo humano a una temperatura máxima de 7 °C, salvo cuando se utilizan para la alimentación de animales de conformidad con el capítulo I del anexo II, para evitar cualquier riesgo para la salud pública o animal.
2. El material sin transformar de la categoría 3 que se destine a la elaboración de piensos o alimentos para animales domésticos deberá almacenarse y transportarse refrigerado, congelado o ensilado, excepto en el caso de que:
a) se transforme en un plazo de 24 horas desde su recogida o desde el final del almacenamiento refrigerado o congelado, si el transporte posterior tiene lugar en un medio de transporte en el que se mantiene la temperatura de almacenamiento;
b) la leche, los productos lácteos o los productos derivados de la leche que no han sido sometidos a ninguno de los tratamientos mencionados en la parte I de la sección 4 del capítulo II del anexo X, se transporten en contenedores refrigerados y aislados, salvo cuando los riesgos se pueden reducir por otros medios, debido a las características del material.
3. Los vehículos destinados al transporte refrigerado deberán estar diseñados de tal manera que pueda mantenerse la temperatura requerida durante toda la duración del transporte y permitan el control de la temperatura.
La sección 1 no se aplicará a la recogida y transporte de material de la categoría 3 consistente en leche, productos a base de leche y productos derivados de la leche realizados por explotadores de establecimientos de transformación de leche que han sido autorizados con arreglo al artículo 4 del Reglamento (CE) nº 853/2004, cuando reciban productos que han entregado previamente y que les son devueltos, en especial por sus clientes.
Como excepción a lo dispuesto en la sección 1, la autoridad competente podrá aceptar la recogida y el transporte de estiércol entre dos puntos situados en la misma granja o entre explotadores de granjas y usuarios en el mismo Estado miembro en otras condiciones que aseguren la prevención de riesgos inaceptables para la salud pública y animal.
1. Deberán adoptarse todas las medidas necesarias para garantizar que:
a) los envíos de subproductos animales y productos derivados son identificables y se mantienen de forma separada e identificable durante la recogida en el lugar de origen y durante su transporte;
b) las sustancias de marcado para la identificación de los subproductos animales o productos derivados de una categoría específica se usan exclusivamente para la categoría en la que se exige su utilización con arreglo al presente Reglamento, o se establece o dispone con arreglo al punto 4;
c) las partidas de subproductos animales y productos derivados se envían desde un Estado miembro a otro en envases, contenedores o vehículos marcados prominentemente y de forma indeleble con códigos de colores, al menos durante el período de transporte, para presentar información, conforme a lo previsto en el presente Reglamento, en la superficie, o parte de ésta, de un envase, contenedor o vehículo, o en una etiqueta o un símbolo que se fije en los mismos de la siguiente forma:
i) para materiales de la categoría 1, el color negro;
ii) para materiales de la categoría 2 (excepto el estiércol y contenido del tubo digestivo), el color amarillo;
iii) para materiales de la categoría 3, el color verde con un alto contenido de azul para garantizar que se distingue claramente de los demás colores;
iv) para partidas importadas, el color mencionado para el material correspondiente en los incisos i), ii) y iii), desde el momento en el que la partida haya cruzado el puesto de inspección fronterizo de primer punto de entrada en la Unión.
2. Durante el transporte y almacenamiento, una etiqueta fijada al envase, contenedor o vehículo deberá:
a) indicar claramente la categoría de los subproductos animales o productos derivados, y
b) mostrar las siguientes palabras de forma visible y legible en el envase, contenedor o vehículo, según corresponda:
i) para materiales de la categoría 3, las palabras "no apto para el consumo humano";
ii) para materiales de la categoría 2 (distintos del estiércol y el contenido del tubo digestivo) y los productos derivados de material de la categoría 2, las palabras "no apto para el consumo animal"; no obstante, cuando los materiales de la categoría 2 se destinen a la alimentación de animales contemplados en el artículo 18, apartado 1, del Reglamento (CE) nº 1069/2009, en las condiciones establecidas en dicho artículo, en la etiqueta se hará constar, en su lugar "apto para la alimentación de …", que se completará con el nombre de la especie animal a cuya alimentación se destinen los materiales;
iii) para materiales de la categoría 1 y los productos derivados de material de la categoría 1 destinados a
- la eliminación, las palabras "solo para eliminación";
- la elaboración de alimentos para animales de compañía, las palabras "solo para fabricación de alimentos para animales de compañía";
- a la fabricación de productos derivados contemplados en el artículo 36 del Reglamento (CE) nº 1069/2009, las palabras "solo para fabricación de productos derivados. No apto para el consumo humano o animal ni para la aplicación a la tierra";
iv) para leche, productos lácteos, productos derivados de la leche, calostro y productos a base de calostro, las palabras "no apto para el consumo humano";
v) para gelatina producida a partir de material de la categoría 3, las palabras "gelatina apta para el consumo animal";
vi) para colágeno producido a partir de material de la categoría 3, las palabras "colágeno apto para el consumo animal";
vii) para alimentos crudos para animales de compañía, las palabras "solo como alimentos para animales de compañía";
viii) para pescado y productos derivados de pescado destinados a la alimentación de peces, tratados y envasados antes de su distribución, el nombre y dirección del establecimiento de origen de elaboración del pienso, marcado de forma clara y legible, y
- para harina de pescado derivada de peces silvestres, con la mención "solo contiene harina de pescado derivada de peces silvestres – puede usarse para la alimentación de peces de piscifactoría de todas las especies";
- para harina de pescado derivada de peces de piscifactoría, con la mención "solo contiene harina de pescado derivada de peces de piscifactoría de la especie […] – puede usarse únicamente para la alimentación de peces de piscifactoría de otra especie";
- para harina de pescado derivada de peces silvestres y de peces de piscifactoría, con la mención "contiene harina de pescado derivada de peces silvestres y peces de piscifactoría de la especie […] – puede usarse únicamente para la alimentación de peces de piscifactoría de otra especie";
ix) para hemoderivados de équidos con fines distintos de la alimentación animal, las palabras "sangre y hemoderivados de équidos. No apto para el consumo humano";
x) para cuernos, pezuñas y otros materiales para la fabricación de abonos y enmiendas del suelo de origen orgánico mencionadas en la sección 12 del capítulo II del anexo XIV, las palabras "no apto para el consumo humano o animal";
xi) para abonos y enmiendas del suelo de origen orgánico, las palabras "abonos o enmiendas del suelo de origen orgánico – no está permitido el pasto de animales de granja o el uso de los cultivos como hierba de pasto durante un mínimo de 21 días tras su aplicación";
xii) para materiales empleados para la alimentación de animales conforme a la sección 1 del capítulo II del anexo VI, el nombre y la dirección del centro de recogida, y las palabras "no apto para el consumo humano";
xiii) para el estiércol y el contenido del tubo digestivo, la palabra "estiércol";
xiv) para productos intermedios, en el envase exterior, las palabras "solo para medicamentos/medicamentos veterinarios/productos sanitarios/productos sanitarios implantables activos/productos para el diagnóstico in vitro/reactivos de laboratorio";
xv) para muestras para diagnóstico e investigación, las palabras "para fines de investigación y diagnóstico", en lugar del texto de etiqueta definido en la letra a);
xvi) para muestras comerciales, las palabras "muestras comerciales no aptas para el consumo humano", en lugar del texto de etiqueta definido en la letra a);
xvii) para artículos de exposición, las palabras "artículos de exposición no aptos para el consumo humano", en lugar del texto de etiqueta definido en la letra a).
c) Sin embargo, la etiqueta mencionada en el apartado b), inciso xi), no será obligatoria para los siguientes abonos y enmiendas del suelo de origen orgánico:
i) en envases destinados a la venta directa con un peso máximo de 50 kg para uso del consumidor final, o
ii) en grandes sacos con un peso máximo de 1000 kg, a condición de que:
- hayan sido autorizados previamente por la autoridad competente del Estado miembro donde se prevé aplicar a la tierra el abono o enmienda de suelo de origen orgánico;
- se indique sobre los envases o sacos que no están destinados a la aplicación a tierras a las que tengan acceso animales de granja.
3. Los Estados miembros podrán establecer sistemas o normas para el código de colores de los envases, los contenedores o los vehículos utilizados para el transporte de subproductos animales y productos derivados de su territorio y que permanecen en éste, a condición de que dichos sistemas o normas no provoquen confusión con el sistema de código de colores contemplado en el punto 1, letra c).
4. Los Estados miembros podrán establecer sistemas o normas para el marcado de los subproductos animales originarios de su territorio y que permanecen en éste, a condición de que dichos sistemas o normas no entren en conflicto con los requisitos de marcado establecidos para los productos derivados en el capítulo V del presente anexo.
5. No obstante lo dispuesto en los puntos 3 y 4, los Estados miembros podrán utilizar los sistemas o normas mencionados en dichos puntos para los subproductos animales originarios de su territorio pero que no están destinados a permanecer en él si el Estado miembro o tercer país de destino ha comunicado su acuerdo.
6. No obstante:
a) los puntos 1 y 2 del presente capítulo no se aplicarán a la identificación de material de la categoría 3 compuesto por leche, productos lácteos y productos derivados de la leche efectuada por explotadores de establecimientos de transformación de leche que hayan sido autorizados con arreglo al artículo 4 del Reglamento (CE) nº 853/2004, cuando reciban productos que han entregado previamente y que les son devueltos, en especial por sus clientes;
b) la autoridad competente podrá aceptar la identificación de estiércol transportado entre dos puntos situados en la misma explotación o entre explotaciones y los usuarios ubicados dentro del mismo Estado miembro por otros medios, como excepción a lo dispuesto en los puntos 1 y 2;
c) los piensos compuestos contemplados en el artículo 3, apartado 2, letra h), del Reglamento (CE) nº 767/2009 que se han fabricado a partir de subproductos animales o a partir de productos derivados y que están envasados y se comercializan como piensos conforme al artículo 4 del Reglamento (CE) nº 767/2009 no tienen que estar identificados con arreglo al punto 1 y no tienen que estar etiquetados con arreglo al punto 2.
1. Durante el transporte, los subproductos animales y los productos derivados deberán ir acompañados de un documento comercial con arreglo al modelo establecido en el presente capítulo o, cuando el presente Reglamento así lo requiera, de un certificado sanitario.
No obstante, dicho documento o certificado no será necesario, a condición de que:
a) los productos derivados de material de la categoría 3 y los abonos y enmiendas del suelo de origen orgánico se suministren a usuarios finales distintos de explotadores comerciales dentro del mismo Estado miembro por parte de comercios de venta al por menor;
b) la leche, los productos lácteos y los productos derivados de la leche que sean materiales de la categoría 3 se recojan y devuelvan a los explotadores de explotaciones de transformación de leche que hayan sido autorizadas de conformidad con el artículo 4 del Reglamento (CE) nº 853/2004, si dichos explotadores reciben productos, en particular de sus clientes, entregados previamente por ellos;
c) los piensos compuestos contemplados en el artículo 3, apartado 2, letra h), del Reglamento (CE) nº 767/2009 que se han fabricado a partir de subproductos animales o a partir de productos derivados, se comercialicen envasados y etiquetados conforme al artículo 4 del Reglamento (CE) nº 767/2009.
2. El documento comercial deberá presentarse al menos por triplicado (el original y dos copias); el original deberá acompañar al envío hasta su destino final. El consignatario deberá conservarlo. Una de las copias será para el productor y la otra permanecerá en poder del transportista.
Los Estados miembros podrán exigir una confirmación de la llegada del envío a través del sistema Traces o mediante una cuarta copia del documento comercial remitido por el receptor al productor como confirmación de la llegada del envío.
3. Los certificados sanitarios deberán expedirse y firmarse por la autoridad competente.
4. Todos los subproductos animales y productos derivados irán acompañados desde el punto de partida de la cadena de fabricación de un documento comercial con arreglo al modelo del punto 6, en virtud de lo establecido en el artículo 4, apartado 1, del Reglamento (CE) nº 1069/2009, durante el transporte en la Unión.
Sin embargo, además de la autorización de transmisión de información mediante un sistema alternativo, según se especifica en el artículo 21, apartado 3, párrafo segundo, del Reglamento (CE) nº 1069/2009, la autoridad competente podrá autorizar que dichos subproductos animales y productos derivados transportados dentro de su territorio vayan acompañados de:
a) un documento comercial diferente, en formato electrónico o en papel, a condición de que dicho documento comercial contenga la información contemplada en la letra f) de las Notas que se recogen en el punto 6, del presente capítulo;
b) un documento comercial en el que se exprese la cantidad de materiales en peso o en volumen de material o en cantidad de envases;
5. Los registros y documentos comerciales relacionados o certificados sanitarios se conservarán durante un período mínimo de dos años para su eventual presentación a las autoridades competentes.
6. Modelo de documento comercial
Notas
a) Los documentos comerciales se elaborarán según el modelo que figura en el presente capítulo.
Cada documento contendrá, siguiendo la numeración del modelo, los certificados requeridos para el transporte de subproductos animales y productos derivados.
b) El documento comercial estará redactado en una de las lenguas oficiales del Estado miembro de origen y de destino, según proceda.
También podrá estar redactado en otras lenguas oficiales de la Unión si va acompañado de una traducción oficial o previo acuerdo de las autoridades competentes del Estado miembro de destino.
c) El original de cada documento comercial constará de una única página, por ambos lados o, si se necesita más espacio, se dispondrá de tal manera que todas las páginas en cuestión formen un todo integrado e indivisible de forma fehaciente.
d) Si, por razones de identificación de las partes del envío, se añaden hojas al documento, éstas se considerarán también parte del documento original y cada una de ellas deberá llevar la firma de la persona responsable.
e) Cuando el documento comercial, incluidas las hojas adicionales mencionadas en la letra d), conste de más de una página, cada una irá numerada al pie —(página número) de (número total de páginas)— y llevará en la cabecera el número de código del documento que la persona responsable le haya asignado.
f) La persona responsable cumplimentará y firmará el documento comercial original.
En el documento comercial deberán constar:
i) la fecha en la que el material sale de los locales;
ii) la descripción del material, incluida;
- su identificación con arreglo a una de las categorías mencionadas en los artículos 8, 9 y 10 del Reglamento (CE) nº 1069/2009;
- la especie animal y la referencia específica al apartado pertinente del artículo 10 del Reglamento (CE) nº 1069/2009 en el caso de material de la categoría 3 y productos derivados del mismo destinados a ser usados como pienso y,
- en su caso, el número de marca auricular del animal;
iii) la cantidad de material, en volumen, peso o cantidad de envases;
iv) el lugar de origen del material, desde donde se envía el material;
v) el nombre y la dirección del transportista del material;
vi) el nombre y la dirección del consignatario y, en su caso, su número de autorización o de registro, expedido con arreglo a lo dispuesto en el Reglamento (CE) nº 1069/2009 o en los Reglamentos (CE) nº 852/2004, (CE) nº 853/2004 o (CE) nº 183/2005, según proceda, y
vii) si procede, el número de autorización o de registro del establecimiento o planta de origen, expedido con arreglo a lo dispuesto en el Reglamento (CE) nº 1069/2009 o en los Reglamentos (CE) nº 852/2004, (CE) nº 853/2004 o (CE) nº 183/2005, según proceda, así como la naturaleza de los métodos de tratamiento.
g) El color de la firma de la persona responsable deberá ser distinto al del texto impreso.
h) El número de referencia del documento y el número de referencia local se expedirán de forma única para cada envío.
Documento comercial
para el transporte en la Unión Europea de subproductos animales y productos derivados no destinados al consumo humano, de conformidad con el Reglamento (CE) nº 1069/2009
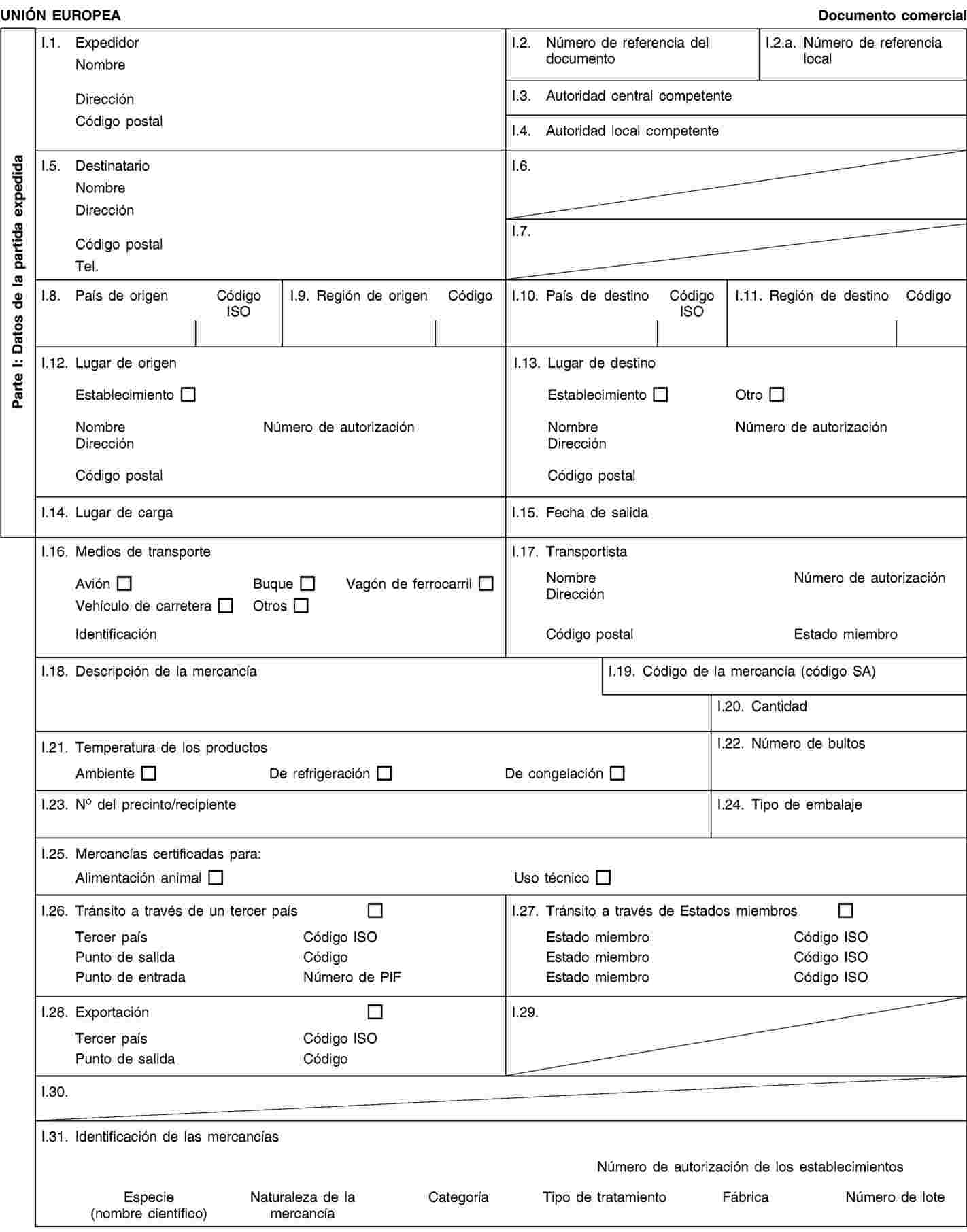

1. Los registros a los que se hace referencia en el artículo 22, apartado 1, del Reglamento (CE) nº 1069/2009 para los subproductos animales y productos derivados distintos de los piensos compuestos conforme a lo definido en el artículo 3, apartado 2, letra h), del Reglamento (CE) nº 767/2009, que se han fabricado a partir de subproductos animales y productos derivados y que son introducidos en el mercado de conformidad con el artículo 4 del Reglamento (CE) nº 767/2009, contendrán:
a) una descripción de:
i) la especie animal para los materiales de la categoría 3 y los productos derivados de los mismos destinados a ser usados como ingredientes para piensos y, en su caso, en el caso de canales enteras y cabezas, el número de marca auricular;
ii) la cantidad de material;
b) en el caso de registros conservados por quienes envíen subproductos animales o productos derivados, la siguiente información:
i) la fecha en la que el material sale de los locales;
ii) el nombre y la dirección del transportista y del consignatario y, en su caso, su número de autorización o de registro;
c) en el caso de registros conservados por quienes transporten subproductos animales o productos derivados, la siguiente información:
i) la fecha en la que el material sale de los locales;
ii) el lugar de origen del material, desde dónde se envía el material;
iii) el nombre y la dirección del consignatario y, en su caso, su número de autorización o registro;
d) en el caso de registros conservados por quienes reciban subproductos animales o productos derivados, la siguiente información:
i) la fecha en la que se recibe el material;
ii) el lugar de origen del material, desde dónde se envía el material;
iii) el nombre y la dirección del transportista.
2. No obstante lo dispuesto en el punto 1 de la presente sección, los explotadores no tendrán que conservar la información aludida en el punto 1, letra a), punto 1, letra b), inciso i), punto 1, letra c), incisos i) y iii), y punto 1, letra d), incisos ii) y iii) de forma separada, si conservan una copia del documento comercial previsto en el capítulo III para cada envío y ponen dicha información a disposición junto con la restante información exigida en el punto 1 de la presente sección.
3. Los explotadores de plantas de incineración y coincineración mantendrán registros de las cantidades y categorías de los subproductos animales y productos derivados incinerados o coincinerados, si procede, así como la fecha en la que se llevaron a cabo tales actividades.
Además de los registros exigidos en virtud de la sección I, los explotadores mantendrán los siguientes registros en relación con el material relevante si los subproductos animales son usados para fines especiales de alimentación animal con arreglo al capítulo II del anexo VI:
1. en el caso de los usuarios finales, la cantidad utilizada, los animales a cuya alimentación se destinan los materiales y su fecha de utilización;
2. en el caso de los centros de recogida:
i) la cantidad manipulada o tratada de conformidad con el punto 4 de la sección 1 del capítulo I del anexo VI;
ii) el nombre y la dirección de cada usuario final del material;
iii) las instalaciones a las que se transportará el material para ser utilizado;
iv) la cantidad enviada, y
v) la fecha de expedición del material.
Los explotadores de las granjas contempladas en el capítulo I del anexo II mantendrán registros como mínimo de:
a) la cantidad de pieles y canales de animales alimentados con materiales procedentes de su propia especie, y
b) todo envío, para garantizar la rastreabilidad del material.
Las personas responsables de la tierra a la que se aplican abonos y enmiendas del suelo de origen orgánico, distintos de los materiales mencionados en el párrafo segundo del capítulo II del anexo II y a la que tienen acceso los animales de granja o de la que se siega hierba de pasto para la alimentación de animales de granja, deberán mantener registros al menos durante dos años de la siguiente información:
1. las cantidades utilizadas de abonos y enmiendas del suelo de origen orgánico;
2. las fechas y lugares en los que se aplicaron a las tierras abonos y enmiendas del suelo de origen orgánico;
3. las fechas en las que se ha permitido al ganado pastar o en las que se ha segado hierba de pasto para la alimentación de los animales tras la aplicación de los abonos o enmiendas del suelo de origen orgánico.
Las plantas de transformación que producen harina de pescado u otros piensos derivados de animales acuáticos mantendrán registros de:
a) las cantidades producidas diariamente;
b) la especie de origen, incluida la indicación de si los animales acuáticos habían sido capturados en el mar o eran producto de la acuicultura;
c) en el caso de harina de pescado derivada de peces de piscifactoría destinada a la alimentación de peces de piscifactoría de otra especie, el nombre científico de la especie de origen.
En caso de incineración o enterramiento de subproductos animales de acuerdo con el artículo 19, apartado 1, del Reglamento (CE) nº 1069/2009, la persona responsable de la incineración o el enterramiento deberá mantener registros de:
a) las cantidades, categorías y especies de los subproductos animales enterrados o incinerados;
b) la fecha y el lugar de enterramiento e incineración.
Los explotadores de las fábricas fotográficas autorizadas mencionadas en la sección 11 del capítulo II del anexo XIV llevarán un registro detallado de las compras y usos de gelatina fotográfica, así como de la eliminación de los residuos y el material excedente.
1. En las plantas de transformación que procesen material de las categorías 1 o 2, los productos derivados deberán estar marcados permanentemente con triheptanoato de glicerol (GTH), de forma que:
a) el GTH se añada a los productos derivados que han sido sometidos previamente a un tratamiento térmico de higienización a una temperatura interna mínima de 80 °C y que quedan protegidos posteriormente de una recontaminación;
b) todos los productos derivados contengan de forma homogénea en toda su masa una concentración mínima de 250 mg de GTH por kg de grasa.
2. Los explotadores de las plantas de transformación mencionadas en el punto 1, deberán disponer de un sistema de control y registro de los parámetros adecuados para demostrar a la autoridad competente que se ha alcanzado la concentración mínima homogénea exigida.
Dicho sistema de control y registro incluirá la determinación del contenido de GTH intacto como triglicérido en un extracto de GTH lavado con éter de petróleo 40-70 de las muestras tomadas periódicamente.
3. El marcado con GTH no será obligatorio en:
a) los productos derivados líquidos destinados a plantas de biogás o de compostaje;
b) los productos derivados utilizados para alimentación de animales de peletería de conformidad con el capítulo I del anexo II;
c) el biodiésel producido de conformidad con la letra D de la sección 2 del capítulo IV del anexo IV;
d) los productos derivados obtenidos de conformidad con el artículo 12, letra a), inciso ii), el artículo 12, letra b), inciso ii), el artículo 13, letra a), inciso ii), el artículo 13, letra b), inciso ii), y el artículo 16, letra e), del Reglamento (CE) nº 1069/2009, cuando dichos productos:
i) se trasladen desde la planta de transformación mediante un sistema transportador cerrado de paso obligatorio, y siempre que dicho sistema haya sido autorizado por la autoridad competente para:
- su incineración directa o coincineración inmediatas;
- su utilización inmediata según un método autorizado para los subproductos animales de las categorías 1 y 2 con arreglo al capítulo IV del anexo IV, o
ii) se destinen a los fines de investigación y otros fines específicos a los que se refiere el artículo 17 del Reglamento (CE) nº 1069/2009, autorizados por la autoridad competente.
Los establecimientos o plantas de fabricación de alimentos para animales de compañía contemplados en el artículo 24, apartado 1, letra e), del Reglamento (CE) nº 1069/2009 deberán disponer de instalaciones adecuadas para:
a) almacenar y tratar el material entrante con total seguridad, y
b) eliminar, de conformidad con el presente Reglamento, los subproductos animales sin utilizar que queden tras la elaboración de los mencionados productos o, de lo contrario, dicho material deberá enviarse a una planta de transformación, de incineración, de coincineración o, para materiales de la categoría 3, a una planta de biogás o de compostaje, con arreglo a lo dispuesto en los artículos 12, 13 y 14 del Reglamento (CE) nº 1069/2009 y en el presente Reglamento.
Las condiciones establecidas en el presente capítulo se aplicarán al almacenamiento de los subproductos animales mencionados en el artículo 24, apartado 1, letra i), del Reglamento (CE) nº 1069/2009 y a las siguientes actividades que implican manipulación de subproductos animales tras su recogida, según se contempla en el artículo 24, apartado 1, letra h), de dicho Reglamento:
a) clasificación;
b) corte;
c) refrigeración;
d) congelación;
e) salazón u otros procesos de conservación;
f) separación de las pieles;
g) extracción del material especificado de riesgo;
h) operaciones de manipulación de subproductos animales realizadas de conformidad con las obligaciones de la legislación veterinaria de la Unión, como examen post mortem o toma de muestras;
i) higienización/pasteurización de los subproductos animales destinados a su transformación en biogás o compostaje previamente a dicha transformación o compostaje en otro establecimiento o planta de conformidad con lo dispuesto en el anexo V del presente Reglamento;
j) cribado.
1. Los locales e instalaciones donde se realicen las actividades intermedias cumplirán como mínimo las condiciones siguientes:
a) deberán estar correctamente separados de las vías públicas a través de las cuales se puede propagar la contaminación así como de otros locales, como mataderos. El diseño de la planta deberá garantizar la total separación del material de las categorías 1 y 2 del material de la categoría 3 desde la recepción hasta la reexpedición, salvo que se realice en un edificio totalmente separado;
b) la planta deberá disponer de un espacio cubierto para recibir los subproductos animales, a menos que estos se descarguen a través de instalaciones que impidan la propagación de riesgos para la salud pública y la salud animal, como a través de tuberías cerradas para subproductos animales líquidos;
c) la planta deberá estar construida de forma que facilite su limpieza y desinfección. Los suelos estarán construidos de una manera que facilite la evacuación de los líquidos;
d) la planta deberá disponer de servicios, vestuarios y lavabos adecuados para el personal y, si procede, una zona de oficina que se podrá poner a disposición del personal que lleve a cabo los controles oficiales;
e) la planta deberá contar con dispositivos apropiados de protección contra las plagas, como insectos, roedores y aves;
f) cuando sea necesario para alcanzar los objetivos del presente Reglamento, las plantas deberán contar con instalaciones de almacenamiento adecuadas con temperatura controlada y capacidad suficiente para mantener los subproductos animales a temperaturas adecuadas y diseñadas para permitir el control y registro de esas temperaturas.
2. Las plantas de transformación dispondrán de instalaciones adecuadas para limpiar y desinfectar los contenedores o recipientes en los que se reciban los subproductos animales y los vehículos en que se transporten, con excepción de los buques. Deberán proveerse las instalaciones adecuadas para la desinfección de las ruedas de los vehículos.
1. La clasificación de los subproductos animales deberá llevarse a efecto de forma que se evite todo riesgo de propagación de enfermedades animales.
2. Durante su almacenamiento, los subproductos animales deberán manipularse y almacenarse en todo momento por separado de otras mercancías y de manera que se evite la propagación de agentes patógenos.
3. Los subproductos animales deberán almacenarse adecuadamente, incluyendo unas condiciones adecuadas de temperatura, hasta su reexpedición.
El proceso de higienización/pasteurización mencionado en la letra i), del párrafo inicial del presente capítulo se llevará a cabo de conformidad con las normas de transformación contempladas en el punto 1 de la sección 1 del capítulo I del anexo V o con arreglo a parámetros alternativos de transformación que hayan sido autorizados de conformidad con el punto 1 de la sección 2 del capítulo III del mismo anexo.
Los locales e instalaciones donde se almacenen productos derivados cumplirán como mínimo las condiciones siguientes:
1. Los locales e instalaciones de almacenamiento de productos derivados a partir de material de la categoría 3 no deberán estar ubicados en el mismo lugar que los dedicados al almacenamiento de productos derivados a partir de material de las categorías 1 y 2, a menos que se impida la contaminación cruzada gracias al diseño y gestión de los locales, como por medio del almacenamiento en edificios completamente distintos.
2. Los almacenes deberán ajustarse a los siguientes requisitos:
a) disponer de un espacio cubierto para recibir y reexpedir los productos derivados, a menos que los productos derivados:
i) sean descargados a través de instalaciones que impidan la propagación de riesgos para la salud pública y la salud animal, como mediante tuberías cerradas para productos líquidos, o
ii) sean recibidos en envases, como sacos, o en contenedores o medios de transporte a prueba de fugas;
b) estar construidos de modo que facilite su limpieza y desinfección. Los suelos deberán estar construidos de una manera que facilite la evacuación de los líquidos;
c) disponer de servicios, vestuarios y lavabos adecuados para el personal;
d) contar con dispositivos apropiados de protección contra las plagas, como insectos, roedores y aves.
3. La planta deberá disponer de instalaciones adecuadas para limpiar y desinfectar los contenedores o recipientes en los que se reciban los productos derivados y los vehículos en los que se transporten, con excepción de los buques.
4. Los productos derivados deberán almacenarse de modo adecuado hasta su reexpedición.
1. El almacenamiento de los productos contemplados en la parte II de la sección 4 del capítulo II del anexo X deberá efectuarse a una temperatura adecuada al objeto de evitar riesgos para la salud pública o para la salud animal en establecimientos o plantas de almacenamiento autorizados o registrados o en una zona de almacenamiento específica independiente dentro de un establecimiento o planta de almacenamiento autorizado o registrado.
2. Las muestras de los productos finales tomadas durante el almacenamiento o al término del mismo deberán cumplir, como mínimo, las normas microbiológicas previstas en el capítulo I del anexo X.
1. Los explotadores de plantas o establecimientos registrados u otros explotadores registrados manipularán los productos animales y productos derivados con arreglo a las siguientes condiciones:
a) los locales deberán estar construidos de una manera que permita su limpieza y desinfección efectivas, cuando proceda;
b) los locales deberán contar con dispositivos apropiados de protección contra las plagas, como insectos, roedores y aves;
c) las instalaciones y equipo deberán mantenerse en condiciones higiénicas, según proceda;
d) los subproductos animales y productos derivados deberán almacenarse en condiciones que impidan su contaminación.
2. Los explotadores mantendrán registros de forma accesible para la autoridad competente.
3. En particular, los explotadores registrados que transporten subproductos animales o productos derivados, salvo entre las instalaciones del mismo explotador:
a) tendrán información a su disposición al respecto de la identificación de sus vehículos, que permita la verificación del uso de los mismos para el transporte de subproductos animales o productos derivados;
b) limpiarán y desinfectarán sus vehículos, si procede;
c) adoptarán todas las medidas necesarias adicionales al objeto de impedir la contaminación y la propagación de enfermedades transmisibles a personas o animales.
Normas microbiológicas para productos derivados
Se aplicarán las siguientes normas microbiológicas a los productos derivados:
Las muestras de los productos finales tomadas durante el período de almacenamiento en la planta de transformación o al término del mismo deberán cumplir las normas siguientes:
Salmonella: ausente en 25 g: n = 5, c = 0, m = 0, M = 0;
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 300 en 1 g;
donde:
n = número de muestras del ensayo;
m = valor umbral del número de bacterias; el resultado se considera satisfactorio si el número de bacterias en todas las muestras no es superior a m;
M = valor máximo del número de bacterias; el resultado se considera insatisfactorio si el número de bacterias en una o más muestras es igual o superior a M; y
c = número de muestras cuyo recuento de bacterias puede situarse entre m y M; la muestra sigue considerándose aceptable si el recuento de bacterias de las demás muestras es igual o inferior a m;
No obstante, no se aplicarán las normas microbiológicas establecidas en el presente capítulo a las grasas extraídas y al aceite de pescado derivado de la transformación de subproductos animales, cuando la proteína animal transformada que se obtiene durante la transformación, se someta a muestreo para garantizar el cumplimiento de esas normas.
A. Materias primas
Solo los subproductos animales derivados de material de la categoría 3 o los productos derivados de tales subproductos animales, distintos de los materiales de la categoría 3 recogidos en el artículo 10, letras n), o) y p), del Reglamento (CE) nº 1069/2009 se podrán usar para la producción de proteínas animales transformadas.
B. Normas de transformación
1. Las proteínas de mamíferos transformadas deberán someterse previamente al método de transformación 1 (esterilización por presión) según se expone en el capítulo III del anexo IV.
No obstante:
a) la sangre de porcino o las fracciones de sangre de porcino para la fabricación de harina de sangre podrán someterse en cambio a cualquiera de los métodos de transformación 1 a 5 o al método de transformación 7 recogidos en el capítulo III del anexo IV, si en el caso del método de transformación 7 se ha aplicado un tratamiento térmico en toda su masa a una temperatura mínima de 80 °C;
b) las proteínas de mamíferos transformadas:
i) podrán someterse a cualquiera de los métodos de transformación 1 a 5 o al método de transformación 7 recogidos en el capítulo III del anexo IV, si se eliminan posteriormente o se utilizan como combustible;
ii) cuando se destinan exclusivamente a su uso en alimentos para animales de compañía, podrán someterse a cualquiera de los métodos de transformación 1 a 5 o al método de transformación 7 recogidos en el capítulo III del anexo IV, si:
- se transportan en contenedores específicos no utilizados para el transporte de subproductos animales o piensos para animales de granja, y
- se envían directamente desde una planta de transformación de material de la categoría 3 a la fábrica de alimentos para animales de compañía o a una planta de almacenamiento autorizada desde la que se reexpedirán directamente a la fábrica de alimentos para animales de compañía.
2. Las proteínas de animales no mamíferos transformadas, con excepción de la harina de pescado, deberán someterse previamente a cualquiera de los métodos de transformación del 1 al 5 o al método de transformación 7 recogidos en el capítulo III del anexo IV.
3. La harina de pescado deberá haber sido sometida a:
a) cualquiera de los métodos de transformación recogidos en el capítulo III del anexo IV, o
b) otro método que garantice que el producto cumple las normas microbiológicas aplicables a productos derivados recogidas en el capítulo I del presente anexo.
C. Almacenamiento
1. Las proteínas animales transformadas se envasarán y almacenarán en bolsas nuevas o esterilizadas o se almacenarán en silos o depósitos adecuadamente construidos.
Se adoptarán las medidas suficientes para reducir al máximo la condensación dentro de los silos, transportadores o ascensores.
2. Dentro de los transportadores, ascensores y silos, los productos se protegerán contra la contaminación accidental.
3. El equipo de manipulación de las proteínas animales trasformadas deberá mantenerse limpio y seco; deberán proveerse puntos de inspección adecuados para poder examinar la limpieza del equipo.
Todas las instalaciones de almacenamiento deberán vaciarse y limpiarse con regularidad, según sea necesario para impedir la contaminación.
4. Las proteínas animales transformadas deberán mantenerse secas.
Deberán evitarse las pérdidas y la condensación en la zona de almacenamiento.
A. Materia prima
Solo podrá utilizarse para la producción de hemoderivados la sangre prevista en el artículo 10, letra a), y en el artículo 10, letra b), inciso i), del Reglamento (CE) nº 1069/2009.
B. Normas de transformación
Los hemoderivados deberán haber sido sometidos a:
a) cualquiera de los métodos de transformación del 1 al 5 o al método de transformación 7 recogidos en el capítulo III del anexo IV, o
b) otro método que garantice que el hemoderivado cumple las normas microbiológicas aplicables a productos derivados recogidas en el capítulo I del presente anexo.
A. Materias primas
1. Grasas extraídas
Solo podrá utilizarse para la producción de grasas extraídas procedentes de material de la categoría 3 el material de la categoría 3 distinto de los materiales previstos en el artículo 10, letras i), j), n), o) y p), del Reglamento (CE) nº 1069/2009.
2. Aceite de pescado.
Solo podrá utilizarse para la producción de aceite de pescado el material de la categoría 3 previsto en el artículo 10, letras i) y j), del Reglamento (CE) nº 1069/2009 y el material de la categoría 3 originario de animales acuáticos previsto en el artículo 10, letras e) y f), del citado Reglamento.
B. Normas de transformación
Salvo cuando el aceite de pescado o las grasas extraídas se hayan producido de conformidad con las secciones VIII o XII del anexo III del Reglamento (CE) nº 853/2004, respectivamente, las grasas extraídas deberán haberse obtenido utilizando cualquiera de los métodos de transformación 1 a 5 o el método de transformación 7, y los aceites de pescado deberán haberse producido:
a) por cualquiera de los métodos de transformación 1 a 7 recogidos en el capítulo III del anexo IV, o
b) por otro método que garantice que el producto cumple las normas microbiológicas aplicables a productos derivados recogidas en el capítulo I del presente anexo.
Las grasas extraídas de rumiantes deberán purificarse de forma que los niveles máximos de impurezas insolubles restantes no superen un 0,15 % del peso.
Los derivados de grasas a partir de grasas extraídas de la categoría 3 o de aceite de pescado de la categoría 3 deberán producirse de conformidad con uno de los métodos de transformación recogidos en el capítulo III del anexo IV.
C. Normas de higiene
Cuando la grasa extraída o el aceite de pescado estén envasados, deberán estarlo en recipientes nuevos o limpios y desinfectados si procede para impedir la contaminación y respecto de los que deberán tomarse todas las precauciones necesarias para evitar su recontaminación.
Cuando esté previsto transportar los productos a granel, los tubos, bombas y depósitos, así como cualquier otro contenedor de transporte a granel o camión cisterna utilizado para transportar los productos desde la fábrica, bien directamente al buque o a los depósitos de costa, bien directamente a las plantas, deberán haber sido limpiados antes de ser utilizados.
Primera parte
Condiciones generales
A. Materia prima
Solo podrá utilizarse para la producción de leche, productos lácteos y productos derivados de la leche la leche prevista en el artículo 10, letra e), del Reglamento (CE) nº 1069/2009 distinta de los lodos de centrifugado o de separación, y la leche prevista en el artículo 10, letras f) y h), del Reglamento (CE) nº 1069/2009.
Solo podrá utilizarse calostro a condición de que proceda de animales vivos y que no presente ningún signo de una enfermedad transmisible a personas o animales a través del calostro:
B. Normas de transformación
1. La leche será objeto de uno de los tratamientos siguientes:
1.1. Esterilización a un valor F0 [*] de tres o superior;
1.2. UHT [**] combinado con uno de los siguientes;
a) un tratamiento físico subsiguiente, a saber:
i) un procedimiento de desecado combinado con el calentamiento a un mínimo de 72 °C en el caso de la leche para piensos, o
ii) un descenso del pH por debajo de 6,0 durante un mínimo de una hora;
b) la condición de que la leche, el producto lácteo o el producto derivado de la leche se haya producido un mínimo de 21 días antes del envío y que durante dicho período no se haya detectado caso alguno de fiebre aftosa en el Estado miembro de origen;
1.3. HTST [***] aplicado dos veces;
1.4. HTST combinado con uno de los siguientes:
a) un tratamiento físico subsiguiente, a saber:
i) un procedimiento de desecado combinado con el calentamiento a un mínimo de 72 °C en el caso de la leche para piensos, o
ii) un descenso del pH por debajo de 6 durante un mínimo de una hora;
b) la condición de que la leche, el producto lácteo o el producto derivado de la leche se haya producido un mínimo de 21 días antes del envío y que durante dicho período no se haya detectado caso alguno de fiebre aftosa en el Estado miembro de origen.
2. Los productos lácteos y productos derivados de la leche deberán someterse al menos a uno de los tratamientos previstos en el punto 1 o producirse a partir de leche tratada de conformidad con dicho punto.
3. El lactosuero que se vaya a suministrar a animales de las especies sensibles a la fiebre aftosa y se produzca a partir de leche tratada con arreglo al punto 1 deberá:
a) recogerse cuando hayan pasado al menos 16 horas desde la coagulación de la leche, siendo su pH registrado inferior a 6,0 antes de su transporte a las explotaciones, o
b) haberse producido como mínimo 21 días antes del envío, sin que durante dicho período se haya detectado caso alguno de fiebre aftosa en el Estado miembro de origen.
4. Además de los requisitos establecidos en los puntos 1, 2 y 3, la leche, los productos lácteos y los productos derivados de la leche deberán cumplir los siguientes:
4.1. una vez concluido el tratamiento, se adoptarán todas las precauciones necesarias para evitar la contaminación de los productos;
4.2. el producto final debe etiquetarse para indicar que contiene material de la categoría 3 y que no está destinado al consumo humano, y deberá:
a) envasarse en recipientes nuevos, o
b) transportarse a granel en contenedores u otros medios de transporte cuidadosamente limpiados y desinfectados antes de su utilización.
5. La leche cruda deberá producirse en condiciones que ofrezcan unas garantías zoosanitarias adecuadas.
6. El calostro y los productos a base de calostro deberán:
6.1. obtenerse de animales bovinos mantenidos en una explotación en la que todos los rebaños bovinos se reconocen como oficialmente indemnes de tuberculosis, oficialmente indemnes de brucelosis y oficialmente indemnes de leucosis bovina enzoótica tal como se definen el artículo 2, apartado 2, letras d), f) y j), de la Directiva 64/432/CEE;
6.2. haberse producido como mínimo 21 días antes del envío, sin que durante dicho período se haya detectado caso alguno de fiebre aftosa en el Estado miembro de origen;
6.3. haberse sometido a un único tratamiento HTST [***];
6.4. cumplir los requisitos del punto 4 de la presente parte.
Parte II
Excepciones aplicables a la introducción en el mercado de leche transformada de conformidad con normas nacionales
1. Las condiciones establecidas en los puntos 2 y 3 se aplicarán a la transformación, uso y almacenamiento de leche, productos lácteos y productos derivados de la leche que se cataloguen como material de la categoría 3, según lo dispuesto en el artículo 10, letra e), del Reglamento (CE) nº 1069/2009, distintos de los lodos de centrifugado o de separación, y la leche mencionada en el artículo 10, letras f) y h), del citado Reglamento, que no se hayan transformado de conformidad con la parte primera de la presente sección.
2. La autoridad competente autorizará el suministro de leche, productos lácteos y productos derivados de la leche para los fines contemplados en el punto 3 de la presente parte desde establecimientos de transformación de leche autorizados o registrados con arreglo al artículo 4 del Reglamento (CE) nº 853/2004 a condición que de los establecimientos en cuestión garanticen la rastreabilidad de los productos.
3. La leche, productos lácteos y productos derivados de la leche se podrán suministrar y usar como ingredientes para piensos:
a) en el Estado miembro en cuestión y en las zonas transfronterizas con las que el Estado miembro en cuestión haya firmado un acuerdo al efecto, en el caso de productos derivados, incluida el agua blanca, que han estado en contacto con leche cruda y/o leche pasteurizada de conformidad con las condiciones relativas al tratamiento térmico definidas en el punto II.1, letras a) o b), del capítulo II de la sección IX del anexo III del Reglamento (CE) nº 853/2004, si dichos productos derivados se han sometido a alguno de los tratamientos siguientes:
i) UHT;
ii) un proceso de esterilización que haya permitido alcanzar un valor Fc igual o superior a 3, o que se haya llevado a cabo a una temperatura mínima de 115 °C durante 15 minutos o una combinación equivalente de temperatura y tiempo;
iii) la pasteurización o esterilización distinta de la mencionada en el inciso ii), seguida de:
- en el caso de la leche en polvo o de los productos lácteos o productos derivados de la leche en polvo, a un proceso de desecado;
- en el caso de los productos lácteos acidificados, a un proceso que permita reducir el pH a un nivel inferior a 6 y mantener ese nivel durante al menos una hora;
b) en el Estado miembro en cuestión,
i) en el caso de productos derivados, incluida el agua blanca, que han estado en contacto con leche que solo ha sido pasteurizada de conformidad con las condiciones relativas al tratamiento térmico definidas en el punto II.1, letra a), del capítulo II de la sección IX del anexo III del Reglamento (CE) nº 853/2004, y el lactosuero producido a partir de productos lácteos no sometidos a tratamiento térmico, recogido como mínimo 16 horas después de la coagulación y cuyo pH registrado es inferior a 6,0 antes de su suministro para fines de alimentación animal, siempre que se envíen a una cantidad limitada de explotaciones animales autorizadas, seleccionadas sobre la base de la evaluación de riesgos para las situaciones hipotéticas más favorables y más desfavorables realizada por el Estado miembro en cuestión en el proceso de elaboración de los planes de contingencia de enfermedades epizoóticas, en particular de la fiebre aftosa;
ii) en el caso de productos crudos, incluida el agua blanca, que han estado en contacto con leche cruda y otros productos para los que no se puede garantizar su sometimiento a los tratamientos contemplados en las letras a) y b)(i), siempre que se envíen a una cantidad limitada de explotaciones animales autorizadas, seleccionadas sobre la base de la determinación de riesgos para las situaciones hipotéticas más favorables y más desfavorables realizada por el Estado miembro en cuestión en el proceso de elaboración de los planes de contingencia de enfermedades epizoóticas, en particular de la fiebre aftosa, y a condición que los animales presentes en las explotaciones animales autorizadas solo se pueden trasladar
- bien directamente a un matadero ubicado en el mismo Estado miembro, o
- a otra explotación dentro del mismo Estado miembro, en cuyo caso la autoridad competente garantiza que los animales sensibles a la fiebre aftosa solo pueden abandonar la explotación bien directamente a un matadero ubicado en el mismo Estado miembro o, si los animales han sido enviados a una explotación que no utilice como pienso los productos mencionados en el presente inciso ii), una vez transcurrido un período de 21 días de moratoria desde la introducción de los animales.
4. La autoridad competente podrá autorizar el suministro de calostro que no satisface las condiciones establecidas en la letra B, apartado 6, de la parte I de una granja a otra dentro del mismo Estado miembro para fines de alimentación animal, en condiciones que impidan la transmisión de riesgos para la salud.
Parte III
Condiciones especiales aplicables a los lodos de centrifugado o de separación
El material de la categoría 3 que contenga lodos de centrifugado o de separación deberá haberse sometido a un tratamiento térmico a 70 °C como mínimo durante 60 minutos o a 80 °C como mínimo durante 30 minutos, antes de introducirse en el mercado para alimentación de animales de granja.
A. Materias primas
Solo los subproductos animales de material de la categoría 3 o los productos derivados de tales subproductos animales, distintos de los materiales mencionados en el artículo 10, letras m), n), o) y p), del Reglamento (CE) nº 1069/2009 se podrán usar para la producción de gelatina y proteínas hidrolizadas.
B. Normas de transformación de la gelatina
1. Salvo que la gelatina se haya producido de conformidad con la sección XIV del anexo III del Reglamento (CE) nº 853/2004, deberá producirse mediante un proceso que garantice que el material de la categoría 3 se somete a un tratamiento con ácidos o bases, seguido de uno o más aclarados.
el pH deberá ajustarse posteriormente; la gelatina deberá extraerse mediante uno o varios calentamientos sucesivos, seguidos por una purificación mediante filtrado y esterilización.
2. Una vez concluidos los procedimientos indicados en el punto 1, la gelatina podrá someterse al proceso de desecado y, según corresponda, al de pulverización o laminación.
3. Está prohibido el uso de conservantes distintos del dióxido de azufre y del peróxido de hidrógeno.
C. Otras condiciones aplicables a la gelatina
La gelatina deberá envasarse, embalarse, almacenarse y transportarse en condiciones de higiene satisfactorias.
En particular:
a) deberá reservarse un local o una sala para almacenar los materiales de envasado y embalaje;
b) las operaciones de envasado y embalaje deberán efectuarse en un local o lugar destinado a tal efecto.
D. Normas de transformación de las proteínas hidrolizadas
Las proteínas hidrolizadas deberán producirse mediante un proceso que incluya las medidas apropiadas para reducir al máximo la contaminación. La proteína hidrolizada derivada de rumiantes deberá tener un peso molecular inferior a 10000 Dalton.
Además de las condiciones establecidas en el párrafo primero, las proteínas hidrolizadas derivadas total o parcialmente de pieles de rumiantes se producirán en una planta de transformación dedicada únicamente a la producción de proteínas hidrolizadas mediante un proceso que suponga la preparación de la materia prima de la categoría 3 mediante encurtido, encalado y lavado intensivo, seguida de exposición del material a:
a) un pH superior a 11 durante más de tres horas a una temperatura superior a 80 °C, seguida de un tratamiento térmico a más de 140 °C durante 30 minutos a más de 3,6 bares, o
b) un pH comprendido entre 1 y 2 y, a continuación, a un pH superior a 11, seguida de un tratamiento térmico a 140 °C durante 30 minutos a 3 bares.
A. Materias primas
Solo los subproductos animales de material de la categoría 3 o los productos derivados de tales subproductos animales, distintos de los materiales mencionados en el artículo 10, letras m), n), o) y p), del Reglamento (CE) nº 1069/2009 se podrán usar para la producción de fosfato dicálcico.
B. Normas de transformación
1. El fosfato dicálcico deberá producirse mediante un procedimiento que comprenda las tres fases siguientes:
a) en primer lugar, garantice que todo el material óseo de la categoría 3 se tritura finamente, se desgrasa con agua caliente y se trata con ácido clorhídrico diluido (de una concentración mínima del 4 % y un pH inferior a 1,5) durante un período mínimo de dos días;
b) en segundo lugar, tras la parte del procedimiento descrito en el punto a), someta el líquido fosfórico así obtenido a un tratamiento con cal, lo que producirá un precipitado de fosfato dicálcico con un pH comprendido entre 4 y 7;
c) que por último, deje secar al aire dicho precipitado de fosfato dicálcico con una temperatura de entrada comprendida entre 65 y 325 °C y una temperatura final de entre 30 y 65 °C.
2. En caso del fosfato dicálcico derivado de huesos desgrasados, deberá derivarse de los huesos mencionados en el artículo 10, letra a), del Reglamento (CE) nº 1069/2009.
A. Materias primas
Solo los subproductos animales de material de la categoría 3 o los productos derivados de tales subproductos animales, distintos de los materiales mencionados en el artículo 10, letras m), n), o) y p), del Reglamento (CE) nº 1069/2009 se podrán usar para la producción de fosfato tricálcico.
B. Normas de transformación
El fosfato tricálcico deberá producirse mediante un procedimiento que garantice que:
a) todo el material óseo de la categoría 3 se tritura finamente y se desgrasa con flujo contrario de agua caliente (astillas de hueso inferiores a 14 mm);
b) se aplica un calentamiento continuo con vapor a 145 °C durante 30 minutos a 4 bares;
c) se separa el caldo de la proteína de la hidroxiapatita (fosfato tricálcico) mediante centrifugado;
d) se granula después de secarlo en un lecho fluidificado con aire a 200 °C.
A. Materias primas
Solo los subproductos animales de material de la categoría 3 o los productos derivados de tales subproductos animales, distintos de los materiales mencionados en el artículo 10, letras m), n), o) y p), del Reglamento (CE) nº 1069/2009 se podrán usar para la producción de colágeno.
B. Normas de transformación
1. Salvo que el colágeno se haya producido de conformidad con las condiciones aplicables al colágeno definidas en la sección XV del anexo III del Reglamento (CE) nº 853/2004, deberá producirse mediante un proceso que garantice que el material de la categoría 3 sin transformar se somete a un tratamiento con lavado, ajuste del pH con ácidos o bases, seguido de uno o más aclarados, filtración y extrusión.
Después de este tratamiento, el colágeno podrá someterse a un procedimiento de desecado.
2. Estará prohibido el uso de conservantes que no estén autorizados con arreglo a la legislación de la Unión.
C. Otras prescripciones
El colágeno deberá envasarse, embalarse, almacenarse y transportarse en condiciones de higiene satisfactorias. En particular:
a) deberá reservarse un local o una sala para almacenar los materiales de envasado y embalaje;
b) las operaciones de envasado y embalaje deberán efectuarse en un local o lugar destinado a tal efecto.
A. Materias primas
Solo podrán utilizarse para la producción de ovoproductos los subproductos animales previstos en el artículo 10, letras e) y f), y en el artículo 10, letra k), inciso ii), del Reglamento (CE) nº 1069/2009.
B. Normas de transformación
Los ovoproductos deberán:
a) someterse previamente a cualquiera de los métodos de transformación del 1 al 5 o al método de transformación 7 recogidos en el capítulo III del anexo IV;
b) someterse a otro método y parámetros que garanticen que los productos cumplen las normas microbiológicas aplicables a los productos derivados definidas en el capítulo I, o
c) tratarse de conformidad con las condiciones aplicables a los huevos y ovoproductos definidas en los capítulos I, II y III de la sección X del anexo III del Reglamento (CE) nº 853/2004.
El material de la categoría 3 compuesto por productos de origen animal, o los productos alimenticios que contengan productos de origen animal que ya no estén destinados al consumo humano por motivos comerciales, problemas de fabricación, defectos de envasado u otros defectos que no conlleven ningún riesgo para la salud pública o la salud animal, según se recoge en el artículo 10, letra f), del Reglamento (CE) nº 1069/2009, podrá introducirse en el mercado como piensos para animales de granja a condición de que:
a) el material no esté compuesto y no haya entrado en contacto con material de origen animal que no haya sido sometido a transformación:
i) con arreglo a lo dispuesto en el presente Reglamento;
ii) tal como se define en el artículo 2, apartado 1, letra m), del Reglamento (CE) nº 852/2004;
b) se hayan adoptado todas las medidas necesarias para impedir la contaminación del material.
1. Los subproductos de productos de la pesca o invertebrados acuáticos y los productos derivados de los mismos destinados a la fabricación de piensos para peces de piscifactoría o para otras especies de la acuicultura deberán:
a) manipularse y transformarse de manera separada del material no autorizado a tal fin;
b) proceder
i) de peces silvestres y otros animales acuáticos, excepto mamíferos marinos, desembarcados con fines comerciales, o de subproductos animales de peces silvestres procedentes de plantas de fabricación de productos de pescado para el consumo humano, o
ii) de peces de piscifactoría, si se utilizan para la alimentación de peces de piscifactoría de otra especie;
c) transformarse en una planta de transformación conforme a un método que garantice la producción de productos microbiológicamente seguros, incluso con respecto a patógenos de peces.
2. La autoridad competente podrá establecer otras condiciones, orientadas a impedir los riesgos inaceptables para la transmisión de enfermedades transmisibles a personas o animales, para el uso de animales acuáticos y de animales invertebrados acuáticos o terrestres:
a) como pienso para peces de piscifactoría o para animales invertebrados acuáticos, cuando los subproductos animales no se han transformado de conformidad con el punto 1, letra c);
b) como cebo de pesca, incluido cebo para animales invertebrados acuáticos.
[*] F0 es el efecto letal calculado sobre las esporas bacterianas. Un valor F0 igual a 3,00 significa que se ha calentado el punto más frío del producto lo suficiente para alcanzar un efecto letal equivalente al de 121 °C (250 °F) en 3 minutos con calentamiento y enfriamiento instantáneos.
[**] UHT = tratamiento de temperatura ultraalta a 132 °C durante por lo menos 1 segundo.
[***] HTST = Breve pasteurización a alta temperatura: pasteurización a 72 °C durante al menos 15 segundos o con efecto de pasteurización equivalente que dé una reacción negativa en la prueba de la fosfatasa.
1. El comercio de estiércol sin transformar de especies distintas de las aves de corral o los équidos entre los Estados miembros estará sometido a las siguientes condiciones, además de al consentimiento del Estado miembro de destino mencionado en el artículo 48, apartado 1, del Reglamento (CE) nº 1069/2009:
a) queda prohibido el comercio de estiércol sin transformar de especies distintas de las aves de corral o los équidos, con excepción del estiércol:
i) originario de una zona que no esté sujeta a restricciones derivadas de la presencia de una enfermedad transmisible grave, y
ii) destinado a ser aplicado, bajo la supervisión de la autoridad competente, a las tierras de una única explotación situada a ambos lados de la frontera entre dos Estados miembros;
b) no obstante, la autoridad competente del Estado miembro de destino podrá conceder una autorización específica, teniendo en consideración el origen del estiércol, su destino y otras consideraciones sanitarias, para la introducción en su territorio de:
i) estiércol destinado a:
- su transformación en una fábrica de productos derivados para usos externos a la cadena alimentaria animal, o
- su transformación en biogás o compost con arreglo al Reglamento (CE) nº 1069/2009 y al anexo V del presente Reglamento con vistas a la fabricación de los productos recogidos en la sección 2 del presente capítulo.
En dichos casos la autoridad competente tendrá en cuenta el origen del estiércol cuando autorice su introducción en dichas plantas, o
ii) estiércol destinado a ser aplicado a la tierra en una explotación, a condición de que la autoridad competente del Estado miembro de origen haya comunicado su aprobación de dicho comercio.
c) en los casos mencionados en el punto b), al documento comercial que acompaña al envío de estiércol se adjuntará un certificado sanitario conforme al modelo establecido en el punto 3.
2. El comercio de estiércol sin transformar de las aves de corral entre los Estados miembros estará sometido a las siguientes condiciones, además de al consentimiento del Estado miembro de destino mencionado en el artículo 48, apartado 1, del Reglamento (CE) nº 1069/2009:
a) el estiércol deberá ser originario de una zona que no esté sometida a restricciones derivadas de la enfermedad de Newcastle o la influenza aviar;
b) además, el estiércol sin transformar procedente de manadas de aves vacunadas contra la enfermedad de Newcastle no podrá expedirse a una región que haya obtenido la calificación sanitaria de "región que no practica la vacunación contra la enfermedad de Newcastle" conforme a lo dispuesto en el apartado 2 del artículo 15 de la Directiva 2009/158/CE, y
c) al documento comercial que acompaña al envío de estiércol se adjuntará un certificado sanitario conforme al modelo establecido en el punto 3.
3. Modelo de certificado sanitario para adjuntar al documento comercial:
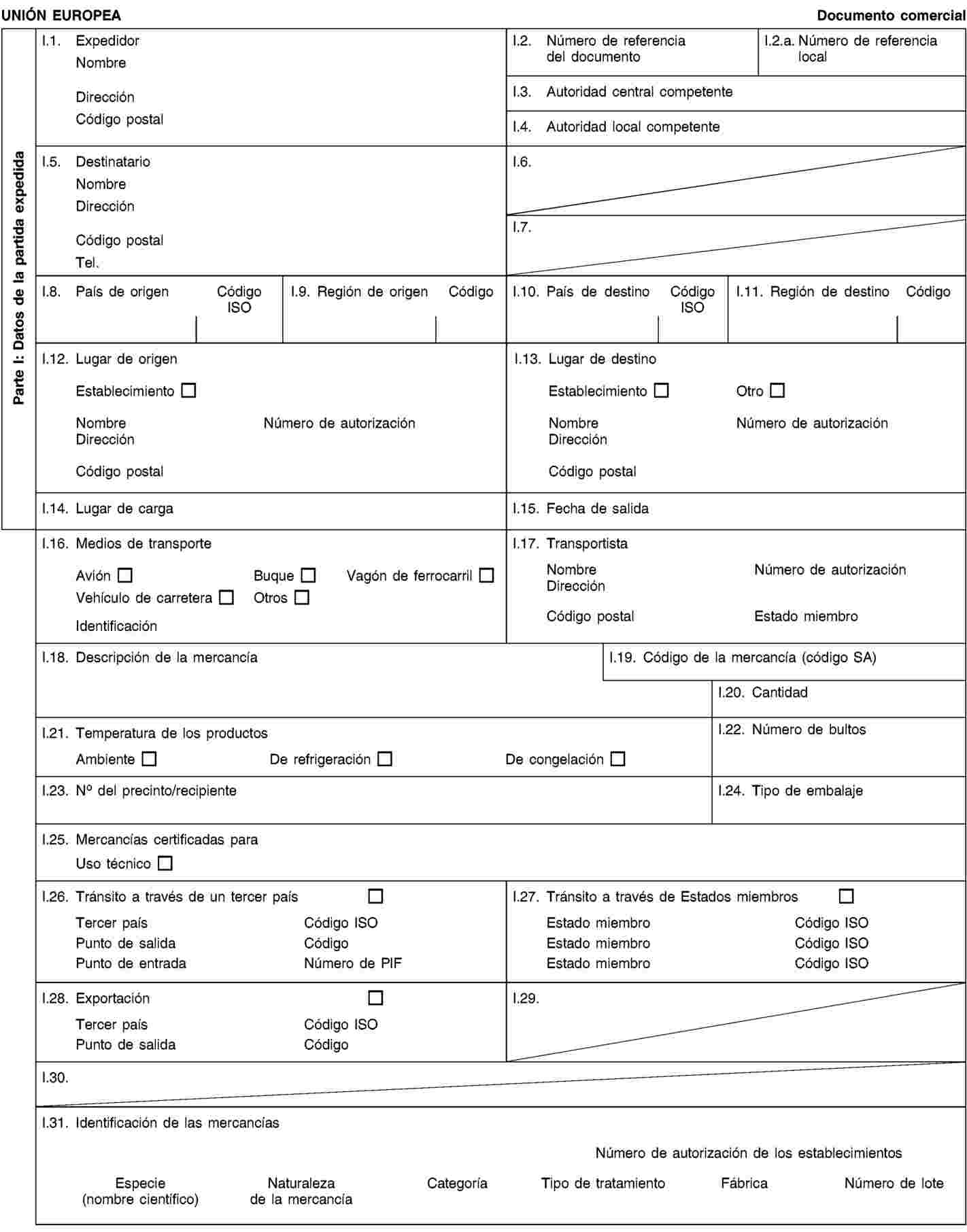

4. Se autoriza el comercio entre Estados miembros de estiércol sin transformar de équidos, a condición de que el Estado miembro de destino haya dado su consentimiento al comercio conforme a lo dispuesto en el artículo 48, apartado 1), del Reglamento (CE) nº 1069/2009 y, a condición de que no proceda de una explotación sujeta a restricciones sanitarias en relación con el muermo, la estomatitis vesicular, el carbunco o la rabia, de conformidad con el artículo 4, apartado 5, de la Directiva 2009/156/CE.
5. A tenor de lo dispuesto en el artículo 48, apartado 1, letra c), inciso ii), del Reglamento (CE) nº 1069/2009, la autoridad competente del Estado miembro de destino podrá exigir a los explotadores que envíen estiércol sin transformar desde otro Estado miembro:
a) que faciliten información adicional sobre el envío previsto, tal como las indicaciones geográficas precisas del lugar de descarga del estiércol, y
b) que almacenen el estiércol antes de su aplicación a la tierra.
6. La autoridad competente podrá autorizar el envío de estiércol transportado entre dos puntos situados en la misma granja sujeto a condiciones de control de los riesgos para la salud, como las obligaciones de los explotadores afectados de llevar los registros adecuados.
La introducción en el mercado de estiércol transformado, productos a base de estiércol transformado y guano de murciélago estará sometida a las siguientes condiciones, además del consentimiento del Estado miembro de destino mencionado en el artículo 48, apartado 1, del Reglamento (CE) nº 1069/2009:
a) Deberán proceder de una planta para productos derivados destinados a usos externos a la cadena alimentaria animal o de una planta de biogás o de compostaje o de una fábrica de abonos o enmiendas del suelo de origen orgánico.
b) Deberán haber sido sometidos a un tratamiento térmico de al menos 70 °C durante un mínimo de 60 minutos y a un tratamiento de reducción de las bacterias esporuladas y toxígenas, cuando hayan sido identificadas como peligro relevante.
c) Sin embargo, la autoridad competente podrá autorizar el uso de otros parámetros normalizados para los procesos distintos de los recogidos en la letra b) siempre y cuando el solicitante demuestre que dichos parámetros reducen al mínimo los riesgos biológicos;
La demostración incluirá una validación, que se llevará a cabo de la manera siguiente:
i) identificación y análisis de los riesgos, incluido el impacto del material aportado, basándose en una definición completa de las condiciones de transformación, y una determinación del riesgo que evalúe cómo se alcanzan en la práctica, en situaciones normales y atípicas, las condiciones de transformación específicas;
ii) validación del proceso previsto
ii-1) midiendo la reducción de la viabilidad/infectividad de los organismos indicadores endógenos durante el proceso, cuando el indicador:
- está constantemente presente en la materia prima, en altos niveles,
- no es menos termorresistente a los aspectos letales del proceso de tratamiento, pero tampoco significativamente más resistente que los patógenos para los que se usa como control,
- es relativamente fácil de cuantificar, identificar y confirmar, o
ii-2) midiendo la reducción de la viabilidad/infectividad, durante la exposición, de un organismo o virus de ensayo caracterizado introducido en la materia prima en un testigo adecuado;
iii) la validación contemplada en el inciso ii) deberá demostrar que el proceso consigue reducir globalmente el riesgo de la manera siguiente:
- por lo que se refiere a los procesos térmicos y químicos, mediante una reducción de Enterococcus faecalis de al menos 5 log10 y una reducción del título de infectividad de virus termorresistentes como los parvovirus, cuando se identifiquen como un peligro pertinente, de al menos 3 log10,
- por lo que se refiere también a los procesos químicos, una reducción de parásitos resistentes como los huevos de Ascaris sp. de al menos el 99,9 % (3 log10) de fases viables;
iv) concepción de un programa completo de control que incluya procedimientos para controlar el proceso;
v) medidas que garanticen la vigilancia y supervisión continuas de los parámetros pertinentes del proceso fijados en el programa de control durante el funcionamiento de la planta.
Deberán recogerse y conservarse datos de los parámetros pertinentes del proceso utilizados en una planta, así como otros puntos críticos de control, de forma que el propietario, el encargado o su representante y la autoridad competente puedan controlar su funcionamiento. La información relativa a un proceso autorizado en virtud de este punto deberá entregarse a la Comisión previa solicitud;
d) las muestras representativas del estiércol tomadas durante o inmediatamente después del tratamiento en la planta para controlar el proceso deberán cumplir las normas siguientes:
Escherichia coli: n = 5, c = 5, m = 0, M = 1000 en 1 g;
o
Enterococaceae: n = 5, c = 5, m = 0, M = 1000 en 1 g;
y
las muestras representativas del estiércol tomadas durante el almacenamiento o en el momento de la salida del almacén en la planta de producción o en la planta de biogás o de compostaje deberán cumplir las normas siguientes:
Salmonella: ausente en 25 g: n = 5; c = 0; m = 0; M = 0
donde:
n = número de muestras del ensayo;
m = valor umbral del número de bacterias; el resultado se considera satisfactorio si el número de bacterias en todas las muestras no es superior a m;
M = valor máximo del número de bacterias; el resultado se considera insatisfactorio si el número de bacterias en una o más muestras es igual o superior a M; y
c = número de muestras cuyo recuento de bacterias puede situarse entre m y M; la muestra sigue considerándose aceptable si el recuento de bacterias de las demás muestras es igual o inferior a m;
El estiércol transformado y los productos a base de estiércol transformado que no cumplan las normas del presente apartado se considerarán como no transformados;
e) deberán almacenarse de forma que, una vez trasformados, se minimice su contaminación, infección secundaria o humedad. Por lo tanto, deberán almacenarse en:
i) silos bien cerrados y aislados o depósitos adecuadamente construidos, o
ii) envases bien cerrados, como bolsas de plástico o sacos.
1. Los abonos y enmiendas del suelo de origen orgánico, distintos del estiércol, del contenido del tubo digestivo, el compost, la leche, los productos lácteos, los productos derivados de la leche, el calostro, los productos a base de calostro y los residuos de fermentación procedentes de la transformación de subproductos animales o productos derivados en biogás, se fabricarán:
a) aplicando el método de transformación 1 (esterilización por presión), cuando la materia prima pertenece a la categoría 2;
b) utilizando la proteína animal transformada que se ha obtenido de material de la categoría 3 con arreglo a la sección 1 del capítulo II del anexo X, o de materiales sometidos a otro tratamiento, cuando estos materiales puedan ser utilizados en abonos o enmiendas del suelo de origen orgánico en virtud de lo dispuesto en el presente Reglamento, o
c) aplicando uno de los métodos de tratamiento 1 a 7 recogidos en el capítulo III del anexo IV, cuando la materia prima pertenece a la categoría 3 y no se utiliza en la elaboración de proteína animal transformada.
2. Los abonos y enmiendas del suelo de origen orgánico consistentes o fabricados a partir de harinas de hueso y carne derivadas de material de la categoría 2 o de proteínas animales transformadas, se mezclarán en un establecimiento o planta registrados, con la proporción mínima suficiente de un ingrediente autorizado por la autoridad competente del Estado miembro en el que se pretende aplicar dicho producto a la tierra, con el propósito de excluir todo uso posterior de la mezcla con fines de alimentación animal.
3. La autoridad competente autorizará el ingrediente mencionado en el punto 2 conforme a lo siguiente:
a) el ingrediente consistirá en cal, estiércol, orina, compost o residuos de fermentación procedentes de la transformación de subproductos animales en biogás o en otras sustancias, como fertilizantes minerales, que no se utilicen para la alimentación animal y que excluyan el uso posterior de la mezcla con fines de alimentación animal de acuerdo con las buenas prácticas agrícolas;
b) el ingrediente se determinará en función de una evaluación de las condiciones relativas al clima y al suelo para el uso de la mezcla como fertilizante, de las condiciones que indiquen que el ingrediente hace que la mezcla no sea apetecible para los animales o que de cualquier otra forma sea eficaz para impedir el uso de la mezcla con fines de alimentación animal y conforme a los requisitos establecidos en la legislación de la Unión o, si procede, en la legislación nacional, para la protección del medio ambiente en lo que respecta a la protección del suelo y las aguas subterráneas.
La autoridad competente pondrá la lista de ingredientes autorizados a disposición de la Comisión y de otros Estados miembros previa solicitud.
4. Sin embargo, los requisitos mencionados en el punto 2 no se aplicarán a:
a) abonos y enmiendas del suelo de origen orgánico en envases destinados a la venta directa con un peso de 50 kg como máximo para uso del consumidor final, o
b) abonos y enmiendas del suelo de origen orgánico en grandes sacos con un peso de 1000 kg como máximo, si se indica en dichos envases o sacos que no están destinados a su aplicación en tierras a las que tienen acceso los animales de granja, a condición de que el Estado miembro en el que se prevé aplicar el abono o la enmienda de suelo de origen orgánico a la tierra haya autorizado el uso de dichos sacos de conformidad con una determinación de la probabilidad de la posible desviación de los materiales a explotaciones ganaderas o a tierras a las que tienen acceso animales de granja.
5. Los fabricantes de abonos y enmiendas del suelo de origen orgánico deben garantizar que, antes de que éstos se comercialicen, se someten a la descontaminación de patógenos de conformidad con:
- el capítulo I del anexo X, en el caso de proteína animal transformada o productos derivados de material de las categorías 2 o 3;
- la sección 3 del capítulo III del anexo V en el caso de compost y residuos de la fermentación procedentes de la transformación en biogás de subproductos animales o productos derivados.
Tras la transformación, los abonos y enmiendas del suelo de origen orgánico deberán almacenarse y transportarse correctamente:
a) a granel, en condiciones adecuadas para impedir la contaminación;
b) envasados o en sacos, en el caso de abonos o enmiendas del suelo de origen orgánico destinados a la venta a usuarios finales, o
c) en el caso de almacenamiento en explotaciones ganaderas, en un espacio de almacenamiento adecuado al que no tengan acceso los animales de la granja.
De conformidad con el artículo 34, apartado 2, del Reglamento (CE) nº 1069/2009, la importación y tránsito a través de la Unión de productos intermedios deberá cumplir lo siguiente:
1. La importación y tránsito de los productos intermedios serán autorizados a condición de que:
a) se deriven de los materiales siguientes:
i) materiales de la categoría 3, distintos de los materiales contemplados en el artículo 10, letras c), n), o) y p), del Reglamento (CE) nº 1069/2009;
ii) los productos generados por los animales contemplados en el artículo 10, letras i), l) y m), del Reglamento (CE) nº 1069/2009, o
iii) las mezclas de los materiales a los que se refieren los incisos i) y ii);
b) en el caso de productos intermedios destinados a la fabricación de productos sanitarios, productos para el diagnóstico in vitro y reactivos de laboratorio, proceden de:
i) materiales que cumplen los criterios mencionados en la letra a), salvo que pueden proceder de animales que se hayan sometido a un tratamiento ilegal, tal como se define en el artículo 1, apartado 2, letra d), de la Directiva 96/22/CE o en el artículo 2, letra b), de la Directiva 96/23/CE;
ii) materiales de la categoría 2 contemplados en el artículo 9, letras f) y h), del Reglamento (CE) nº 1069/2009, o
iii) las mezclas de los materiales a los que se refieren los incisos i) y ii);
c) en el caso de productos intermedios destinados a la fabricación de productos implantables activos, medicamentos y medicamentos veterinarios, se derivan de los materiales contemplados en la letra b), cuando la autoridad competente considere justificado el uso de tales materiales para la protección de la salud pública o animal;
d) procedan de un tercer país que figure como miembro de la Organización Mundial de Sanidad Animal (OIE) en el Boletín de la OIE;
e) procedan de un establecimiento o planta registrado o autorizado por la autoridad competente de un tercer país contemplado en la letra d) de conformidad con las condiciones que se establecen en el punto 2;
f) cada envío vaya acompañado de una declaración del importador con arreglo al modelo de declaración establecido en el capítulo 20 del anexo XV, que estará redactada al menos en una de las lenguas oficiales del Estado miembro en el cual se llevará a cabo la inspección en el puesto de inspección fronterizo y del Estado miembro de destino; dichos Estados miembros podrán admitir el uso de otras lenguas y solicitar traducciones oficiales de declaraciones en esas otras lenguas;
g) en el caso de los materiales mencionados en la letra b), el importador demuestra a la autoridad competente que los materiales:
i) no plantean riesgos de transmisión de enfermedades transmisibles a personas o animales; o
ii) se transportan en condiciones que evitan la transmisión de enfermedades transmisibles a personas o animales.
2. Un establecimiento o planta puede ser registrado o autorizado por la autoridad competente de un tercer país, según se contempla en la letra e) del punto 1, a condición de que:
a) el explotador o propietario de la planta o su representante:
i) demuestre que la planta dispone de las instalaciones adecuadas para la transformación del material contemplado en las letras a), b) o c), del punto 1, con el fin de garantizar que se completan las fases de diseño, transformación y fabricación necesarias;
ii) establece y aplica métodos de vigilancia y control de los puntos críticos en función de los procedimientos utilizados;
iii) mantiene un registro de la información obtenida con arreglo a lo dispuesto en el inciso ii) durante un período mínimo de dos años para su presentación a la autoridad competente;
iv) informa a la autoridad competente en el caso de que cualquier información disponible ponga de manifiesto un riesgo grave para la salud pública o animal;
b) periódicamente, la autoridad competente del tercer país efectuará inspecciones y controles en el establecimiento o planta y lo supervisará de conformidad con lo siguiente:
i) la frecuencia de tales inspecciones y controles dependerá del tamaño de la planta, del tipo de productos que se fabriquen, de la evaluación del riesgo y de las garantías ofrecidas con arreglo a un sistema de controles establecido de conformidad con los principios del sistema de análisis de peligros y puntos críticos de control (APPCC);
ii) si las inspecciones efectuadas por la autoridad competente ponen de manifiesto que no se cumplen las disposiciones del presente Reglamento, dicha autoridad tomará las medidas oportunas;
iii) la autoridad competente elaborará una lista de establecimientos o plantas autorizados o registrados de conformidad con el presente anexo y asignará un número oficial a cada uno de ellos, de manera que les identifique con respecto a la naturaleza de sus actividades; la lista y sus modificaciones posteriores se enviarán al Estado miembro en el cual deberá llevarse a cabo la inspección en el puesto de inspección fronterizo y al Estado miembro de destino.
3. Los productos intermedios importados en la Unión se someterán a controles en el puesto de inspección fronterizo de conformidad con el artículo 4 de la Directiva 97/78/CE y se transportarán directamente desde el puesto de inspección fronterizo:
a) bien a una planta o establecimiento registrado para la producción de los productos derivados mencionados en el artículo 33 del Reglamento (CE) nº 1069/2009, donde los productos intermedios seguirán mezclándose, se utilizarán para el recubrimiento o se montarán, embalarán o etiquetarán antes de su introducción en el mercado o puesta en servicio de conformidad con la legislación de la Unión aplicable al producto derivado;
b) o a un establecimiento o planta autorizado para el almacenamiento de subproductos animales de conformidad con lo dispuesto en el artículo 24, apartado 1, letra i), del Reglamento (CE) nº 1069/2009, desde el que solo se enviarán a un establecimiento o planta descritos en la letra a) del presente punto para los usos mencionados en la misma.
4. Los productos intermedios en tránsito por la Unión se transportarán conforme a lo dispuesto en el artículo 11 de la Directiva 97/78/CE.
5. El veterinario oficial del puesto de inspección fronterizo afectado informará del envío a la autoridad responsable del establecimiento o planta en el lugar de destino mediante el sistema TRACES.
6. El explotador o propietario del establecimiento o planta de destino o su representante mantendrán un registro conforme a lo dispuesto en el artículo 22 del Reglamento (CE) nº 1069/2009 y facilitará a la autoridad competente, previa solicitud, los datos necesarios relativos a las compras, ventas, usos, existencias y eliminación de excedentes de los productos intermedios con el fin de verificar el cumplimiento del presente Reglamento.
7. La autoridad competente, con arreglo a la Directiva 97/78/CE, velará por que los envíos de productos intermedios se expidan desde el Estado miembro en el que deberá llevarse a cabo la inspección en el puesto de inspección fronterizo hasta la planta de destino contemplada en el punto 3 o, en caso de tránsito, al puesto de salida.
8. Periódicamente, la autoridad competente llevará a cabo controles documentales con objeto de hacer cuadrar las cantidades de productos intermedios importados, por una parte, y las almacenadas, utilizadas, expedidas o eliminadas, por otra, con el fin de verificar el cumplimiento del presente Reglamento.
9. Para los envíos de productos intermedios en tránsito, las autoridades competentes responsables de los puestos de inspección fronterizos de entrada y salida, respectivamente, cooperarán en lo necesario para velar por que se lleven a cabo controles efectivos y garantizar la trazabilidad de dichos envíos.
Los establecimientos o plantas que fabrican los productos derivados mencionados en el presente anexo y las plantas de fabricación de alimentos para animales de compañía dispondrán de las instalaciones adecuadas para:
a) almacenar y tratar el material entrante en condiciones que impidan la aparición de riesgos para la salud pública y la salud animal;
b) eliminar los subproductos animales que no se utilicen y los productos derivados que queden tras la producción, salvo cuando el material sin utilizar vaya a ser enviado a una planta de transformación o eliminación o a otro establecimiento o planta, de conformidad con lo dispuesto en el presente Reglamento.
1. Alimentos crudos para animales de compañía
Los explotadores solo podrán utilizar para la producción de alimentos crudos para animales de compañía el material de la categoría 3 previsto en el artículo 10, letra a), y en el artículo 10, letra b), incisos i) y ii), del Reglamento (CE) nº 1069/2009.
Los alimentos crudos para animales de compañía deberán envasarse en envases nuevos a prueba de pérdidas.
Deberán ser objeto de medidas efectivas dirigidas a garantizar que el producto no está expuesto a la contaminación en ninguna fase de la cadena de producción y hasta llegar al punto de venta.
2. Materia prima para alimentos transformados para animales de compañía y accesorios masticables para perros
Los explotadores solo podrán utilizar para la producción de alimentos transformados para animales de compañía y accesorios masticables para perros:
a) materiales de la categoría 3, distintos del material contemplado en el artículo 10, letras n), o) y p), del Reglamento (CE) nº 1069/2009, y
b) en el caso de alimentos importados para animales de compañía y alimentos para animales de compañía fabricados a partir de materiales importados, materiales de la categoría 1 consistentes en subproductos animales derivados de animales que se hayan sometido a un tratamiento ilegal, tal como se define en el artículo 1, apartado 2, letra d), de la Directiva 96/22/CE o el artículo 2, letra b), de la Directiva 96/23/CE.
3. Alimentos transformados para animales de compañía
a) Los alimentos en conserva para animales de compañía deberán someterse a un tratamiento térmico que alcance un valor Fc mínimo de 3.
b) Los alimentos transformados para animales de compañía que no estén en conserva deberán:
i) someterse a un tratamiento térmico de al menos 90 °C en toda la masa del producto final;
ii) someter a un tratamiento térmico de al menos 90 °C los ingredientes de origen animal; o
iii) ser producidos, con respecto a los ingredientes para piensos de origen animal, utilizando exclusivamente:
- subproductos animales o productos derivados de carne o productos cárnicos que se hayan sometido a un tratamiento térmico de al menos 90 °C en toda su masa;
- los siguientes productos derivados que hayan sido producidos de conformidad con los requisitos del presente Reglamento: leche y productos lácteos, gelatina, proteínas hidrolizadas, ovoproductos, colágeno, productos sanguíneos según se recoge en la sección 2 del capítulo II del anexo X, proteínas animales transformadas, incluida la harina de pescado, grasas extraídas, aceites de pescado, fosfato dicálcico, fosfato tricálcico o subproductos aromatizantes;
iv) si lo autoriza la autoridad competente, someterse a un tratamiento como secado o fermentación, que garantice que los alimentos para animales de compañía no entrañan ningún riesgo inaceptable para la salud pública ni la salud animal;
v) en el caso de los subproductos animales mencionados en el artículo 10, letras l) y m), del Reglamento (CE) nº 1069/2009 y en el caso de los subproductos de animales acuáticos e invertebrados acuáticos o terrestres, y en caso de ser autorizado por la autoridad competente, someterse a un tratamiento que garantice que los alimentos para animales de compañía no entrañan ningún riesgo inaceptable para la salud pública ni la salud animal.
Después de la fabricación, deberán tomarse todas las precauciones a fin de garantizar que dichos alimentos transformados para animales de compañía no estén expuestos a contaminación.
Los alimentos transformados para animales de compañía deberán envasarse en envases nuevos.
4. Los accesorios masticables para perros deberán someterse a un tratamiento suficiente para destruir los organismos patógenos, incluida Salmonella.
Tras ese tratamiento, deberán ser objeto de todas las precauciones necesarias para garantizar que no se contaminan.
Los accesorios masticables para perros deberán envasarse en envases nuevos.
5. Durante la producción o el almacenamiento de los productos (antes de su expedición), deberán tomarse muestras de manera aleatoria de los accesorios masticables para perros y de los alimentos transformados para animales de compañía, distintos de los alimentos en conserva o de los alimentos transformados para animales de compañía que se hayan tratado conforme a lo establecido en el punto 3, letra b), inciso i), con el fin de comprobar que cumplen las normas siguientes:
Salmonella: ausencia en 25 g, n = 5, c = 0, m = 0; M = 0;
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 300 en 1 g;
Donde:
n = número de muestras del ensayo;
m = valor umbral del número de bacterias; el resultado se considerará satisfactorio si el número de bacterias en todas las muestras no es superior a m;
M = valor máximo del número de bacterias; el resultado se considerará insatisfactorio si el número de bacterias en una o más muestras es igual o superior a M, y
c = número de muestras cuyo recuento de bacterias puede situarse entre m y M; la muestra sigue considerándose aceptable si el recuento de bacterias de las demás muestras es igual o inferior a m.
6. Durante la producción o el almacenamiento (antes de su expedición), deberán tomarse muestras de manera aleatoria de los alimentos crudos para animales de compañía con el fin de comprobar que cumplen las normas siguientes:
Salmonella: ausencia en 25 g, n = 5, c = 0, m = 0; M = 0;
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 5000 en 1 g;
Donde:
n = número de muestras del ensayo;
m = valor umbral del número de bacterias; el resultado se considerará satisfactorio si el número de bacterias en todas las muestras no es superior a m;
M = valor máximo del número de bacterias; el resultado se considerará insatisfactorio si el número de bacterias en una o más muestras es igual o superior a M, y
c = número de muestras cuyo recuento de bacterias puede situarse entre m y M; la muestra sigue considerándose aceptable si el recuento de bacterias de las demás muestras es igual o inferior a m.
7. Punto final para alimentos transformados para animales de compañía y accesorios masticables para perros
De conformidad con lo dispuesto en el presente Reglamento, podrán introducirse en el mercado sin restricción alguna:
a) los alimentos transformados para animales de compañía
i) que se hayan fabricado y envasado en la Unión de conformidad con el punto 3 y que se hayan sometido a pruebas de conformidad con el punto 5, o
ii) que se hayan sometido a controles veterinarios en un puesto de inspección fronterizo de conformidad con la Directiva 97/78/CE;
b) los accesorios masticables para perros
i) que se hayan fabricado y envasado en la Unión de conformidad con el punto 4 y que se hayan sometido a pruebas de conformidad con el punto 5, o
ii) que se hayan sometido a controles veterinarios en un puesto de inspección fronterizo de conformidad con la Directiva 97/78/CE.
1. Para la fabricación de líquidos o productos derivados deshidratados utilizados para realzar el sabor de los alimentos para animales de compañía, los explotadores solo podrán utilizar los subproductos animales que pueden usarse como materia prima para alimentos transformados de para animales de compañía y accesorios masticables para perros de conformidad con el punto 2 del capítulo II.
2. Los subproductos aromatizantes deberán haberse sometido a un método de tratamiento y parámetros que garanticen el cumplimiento de las normas microbiológicas establecidas en punto 5 del capítulo II del presente anexo. Tras este tratamiento, deberán ser objeto de todas las precauciones necesarias para garantizar que no se contaminan.
3. El producto final deberá:
a) envasarse en recipientes nuevos o esterilizados, o
b) transportarse a granel en contenedores u otros medios de transporte cuidadosamente limpiados y desinfectados antes de su utilización.
La introducción en el mercado de sangre y hemoderivados de équidos con fines distintos de la alimentación animal estará sujeta a las condiciones siguientes:
1. La sangre podrá introducirse en el mercado con esos fines a condición de que haya sido recogida:
a) de équidos que:
i) en la inspección efectuada el día de la recogida de la sangre no presentaban signos clínicos de ninguna enfermedad de declaración obligatoria indicada en el anexo I de la Directiva 2009/156/CE ni de gripe equina, piroplasmosis equina, rinoneumonía equina y arteritis viral equina, indicadas en el punto 4 del artículo 1.2.3 del Código Sanitario para los Animales Terrestres de la OIE, edición de 2010;
ii) hayan permanecido al menos los treinta días previos a la fecha de la recogida de la sangre, y durante la misma, en explotaciones bajo supervisión veterinaria que no fueran objeto de una orden de prohibición de acuerdo con el apartado 5 del artículo 4 de la Directiva 2009/156/CE o de restricciones de acuerdo con el artículo 5 de la citada Directiva;
iii) durante los períodos establecidos en el artículo 4, apartado 5, de la Directiva 2009/156/CE, no hayan tenido ningún contacto con équidos de explotaciones sujetas a una orden de prohibición por razones zoosanitarias de acuerdo con el citado artículo y, al menos en los cuarenta días previos a la recogida de la sangre y durante la misma, no hayan tenido ningún contacto con équidos de un Estado miembro o un tercer país que no esté considerado indemne de peste equina de conformidad con el artículo 5, apartado 2, letra a), de la citada Directiva;
b) bajo supervisión veterinaria:
i) en mataderos registrados o autorizados de acuerdo con el Reglamento (CE) nº 853/2004, o
ii) en instalaciones autorizadas, provistas de un número de autorización veterinaria y supervisadas por la autoridad competente a efectos de la recogida de sangre de équidos para la elaboración de hemoderivados con fines distintos de la alimentación animal.
2. Los hemoderivados podrán introducirse en el mercado con esos fines a condición de que:
a) se hayan tomado todas las precauciones para evitar su contaminación con agentes patógenos durante la producción, la manipulación y el envasado;
b) hayan sido elaborados a partir de sangre que:
i) satisfaga las condiciones establecidas en el punto 1, letra a); o
ii) se haya sometido al menos a uno de los tratamientos siguientes, seguido de un control de efectividad, para inactivar los posibles patógenos causantes de la peste equina, todos los tipos de encefalomielitis equina, incluida la encefalomielitis equina venezolana, la anemia infecciosa equina, la estomatitis vesicular y el muermo (Burkholderia mallei):
- tratamiento térmico a una temperatura de 65 °C durante un mínimo de tres horas;
- irradiación con una dosis de rayos gamma de 25 kGy;
- cambio del pH a 5 durante dos horas;
- tratamiento térmico a un mínimo de 80 °C en toda su masa.
3. La sangre y los hemoderivados de équidos deberán envasarse en recipientes impermeables sellados que, en el caso de la sangre de équidos, indique el número de autorización del matadero o establecimiento de recogida mencionado en el punto 1, letra b).
A. Establecimientos y plantas
La autoridad competente podrá conceder autorización a plantas que manipulen pieles, inclusive las pieles encaladas, para suministrar recortes y piel dividida para la producción de gelatina para el consumo animal o de abonos y enmiendas del suelo de origen orgánico, a condición de que:
a) las plantas dispongan de salas de almacenamiento con suelos duros y paredes lisas que sean fáciles de limpiar y desinfectar y, en su caso, con instalaciones de refrigeración;
b) las salas de almacenamiento se mantengan en un estado de limpieza y de conservación satisfactorio, de forma que no constituyan una fuente de contaminación para las materias primas;
c) en caso de que en estos locales se almacenen o transformen materias primas que no se ajusten al presente capítulo, deberán separarse de las materias primas que sí los cumplan durante el período de recepción, almacenamiento, transformación y expedición;
d) en el caso de recortes y piel dividida de pieles encaladas, éstos se someten a un tratamiento que garantice que no permanece ningún riesgo para la salud pública y la salud animal antes de su uso para la fabricación de:
i) gelatina destinada al consumo animal, o
ii) abonos o enmiendas del suelo de origen orgánico.
B. Introducción en el mercado de subproductos animales y productos derivados
1. Las pieles sin tratar podrán introducirse en el mercado sujetas a las condiciones sanitarias aplicables a la carne fresca de conformidad con la Directiva 2002/99/CE.
2. Las pieles tratadas podrán introducirse en el mercado a condición de que:
a) no hayan estado en contacto con ningún otro producto de origen animal ni con animales vivos que presenten algún riesgo de propagación de una enfermedad transmisible grave;
b) el documento comercial establecido en el capítulo III del anexo VIII contenga una declaración en la que se confirme que se han tomado todas las precauciones para evitar su contaminación con agentes patógenos.
C. Punto final para las pieles tratadas
1. Las pieles de ungulados que conforme a la decisión del explotador estén destinadas a fines distintos del consumo humano, y que cumplan los requisitos establecidos en el Reglamento (CE) nº 853/2004 para materias primas para gelatina o colágeno destinados a su uso en alimentación podrán introducirse en el mercado sin restricciones de acuerdo con el presente Reglamento.
2. De conformidad con lo dispuesto en el presente Reglamento, podrán introducirse en el mercado sin restricción alguna las siguientes pieles tratadas:
a) las pieles que hayan sido sometidas al proceso completo de curtido;
b) las pieles en estado "wet blue";
c) las pieles encurtidas o piqueladas ("pickled pelts")
d) las pieles encaladas (tratamiento con cal y en salmuera a un pH comprendido entre 12 y 13 durante al menos ocho horas).
3. No obstante lo dispuesto en el punto C.2, la autoridad competente podrá exigir que las partidas de pieles tratadas mencionadas en el punto 2, letras c) y d), vayan acompañadas de un documento comercial conforme al modelo dispuesto en el punto 6, del capítulo III del anexo VIII, cuando sean enviadas a establecimientos o plantas de fabricación de alimentos para animales de compañía, abonos o enmiendas del suelo de origen orgánico o de transformación de dichos materiales en biogás.
A. Las disposiciones del presente capítulo se aplicarán sin perjuicio de las medidas de protección de la fauna salvaje, adoptadas en el marco del Reglamento (CE) nº 338/97.
B. Aprovisionamiento seguro
Los trofeos de caza y otras preparaciones de animales, cuando para dichas preparaciones los subproductos animales se hayan sometido a un tratamiento o se presenten en un estado que no entrañe riesgos para la salud, podrán introducirse en el mercado, a condición de que procedan de:
a) especies distintas de los ungulados, aves y animales de las clases biológicas Insecta o Aracnida, y
b) animales originarios de una zona que no esté sometida a restricciones derivadas de la aparición de enfermedades transmisibles graves a las que sean sensibles los animales de las especies en cuestión.
C. Tratamiento seguro
1. Los trofeos de caza u otras preparaciones de animales, cuando para dichas preparaciones los subproductos animales se hayan sometido a un tratamiento o se presenten en un estado que no entrañe riesgos para la salud, podrán introducirse en el mercado, a condición de que:
a) procedan de ungulados o aves que hayan sufrido un tratamiento taxidérmico completo que asegure su conservación a temperatura ambiente;
b) consistan en ungulados o aves montados o partes montadas de dichos animales;
c) se hayan sometido a preparación anatómica, como la plastinación, o
d) sean animales de las clases biológicas Insecta o Aracnida que se hayan sometido a un tratamiento como el secado para evitar cualquier propagación de enfermedades transmisibles a personas y animales.
2. Los trofeos de caza y otros preparados distintos de los mencionados en las letras B y C, apartado 1, que procedan de animales originarios de una zona sometida a restricciones debido a la aparición de enfermedades transmisibles graves a las que sean sensibles los animales de las especies en cuestión, podrán introducirse en el mercado, a condición de que:
a) en el caso de trofeos de caza u otros preparados consistentes únicamente en huesos, cuernos, pezuñas, garras, astas y dientes, estos:
i) hayan permanecido inmersos en agua hirviendo durante el tiempo necesario para que se desprenda de ellos todo material distinto de los huesos, cuernos, pezuñas, garras, astas o dientes;
ii) hayan sido desinfectados con un producto autorizado por la autoridad competente, en particular con peróxido de hidrógeno cuando se trate de partes óseas;
iii) hayan sido envasados inmediatamente después de su tratamiento, sin haber estado en contacto con otros productos de origen animal que pudieran contaminarlos, en envases individuales, transparentes y cerrados para evitar toda contaminación posterior; y
iv) vayan acompañados de un certificado sanitario en el que conste que se han cumplido las condiciones estipuladas en los incisos i), ii) y iii);
b) en el caso de los trofeos de caza u otros preparados consistentes únicamente en pieles, estas:
i) hayan sido:
- secadas;
- saladas en seco o en salmuera durante un período mínimo de catorce días antes de la fecha de su expedición, o
- sometidas a un proceso de conservación distinto del curtido;
ii) hayan sido envasadas inmediatamente después de su tratamiento, sin haber estado en contacto con otros productos de origen animal que pudieran contaminarlas, en envases individuales, transparentes y cerrados para evitar toda contaminación posterior; y
iii) vayan acompañadas de un documento comercial o certificado sanitario en el que conste que se han cumplido las condiciones estipuladas en los incisos i) y ii).
A. Materia prima
1. La lana, pelo, cerdas, plumas, trozos de plumas y plumón sin tratar deberán ser materiales de la categoría 3 contemplados en el artículo 10, letra b), incisos iii), iv) y v), el artículo 10, letras h) y n), del Reglamento (CE) nº 1069/2009.
Deberán estar secos y en envases bien cerrados.
No obstante, en el caso de plumas y partes de plumas y plumón sin tratar enviados directamente del matadero a la planta de transformación, la autoridad competente podrá conceder una excepción al requisito de que los materiales transportados en su territorio estén secos, a condición de que:
a) se adopten las medidas necesarias para evitar toda posible propagación de enfermedades;
b) el transporte se realice en contenedores impermeables o en vehículos que se limpien y se desinfecten después de cada uso.
2. Estará prohibido el traslado de cerdas desde las regiones donde la peste porcina africana sea endémica, excepto si:
a) han sido hervidas, teñidas o blanqueadas, o
b) han sido sometidas a algún otro tipo de tratamiento que pueda eliminar con absoluta seguridad los agentes patógenos, siempre que ello se demuestre mediante un certificado expedido por el veterinario responsable del lugar de origen. El lavado en fábrica no podrá considerarse tratamiento a los efectos de la presente disposición.
3. Lo dispuesto en el punto 1 no se aplicará a las plumas ornamentales ni a las plumas:
a) que lleven los viajeros para su uso particular, o
b) que se envíen a particulares con fines no industriales.
B. Punto final para la lana y el pelo
La lana y el pelo lavados en fábrica, y la lana y el pelo que hayan sido tratados con otro método que garantice que no permanece ningún riesgo inaceptable, podrán introducirse en el mercado sin restricciones de conformidad con lo dispuesto en el presente Reglamento.
Los Estados miembros podrán autorizar la introducción en el mercado de lana y pelo sin tratar procedentes de granjas o de establecimientos o plantas registrados de conformidad con lo dispuesto en el artículo 23 del Reglamento (CE) nº 1069/2009 o autorizados de conformidad con lo dispuesto en el artículo 24, apartado 1, letra i), del citado reglamento en su territorio sin restricciones de conformidad con lo dispuesto en el presente Reglamento, si consideran que la lana y el pelo no entrañan ningún riesgo inaceptable para la salud pública y animal.
C. Punto final para las plumas y el plumón
Las plumas, las partes de plumas y el plumón que hayan sido lavados en fábrica y tratados con vapor caliente a 100 °C durante 30 minutos como mínimo podrán introducirse en el mercado sin restricciones de conformidad con lo dispuesto en el presente Reglamento.
Punto final
Las pieles que hayan sido secadas a temperatura ambiente de 18 °C durante dos días con una humedad del 55 % podrán introducirse en el mercado sin restricciones de conformidad con lo dispuesto en el presente Reglamento.
Los subproductos de la apicultura destinados exclusivamente a utilizarse en la apicultura:
1. no deberán proceder de una zona sujeta a prohibiciones relacionadas con la presencia de:
a) loque americana (Paenibacillus larvae larvae), salvo si la autoridad competente ha determinado que el riesgo es insignificante, ha emitido una autorización específica para el uso de los productos exclusivamente en el Estado miembro en cuestión, y ha adoptado las demás medidas necesarias para garantizar que no se propague dicha enfermedad;
b) acariosis [Acarapis woodi (Rennie)], salvo si la zona de destino ha obtenido garantías adicionales de acuerdo con el artículo 14, apartado 2, de la Directiva 92/65/CEE;
c) pequeño escarabajo de la colmena (Aethina tumida), o
d) ácaro Tropilaelaps (Tropilaelaps spp.), y
2. deberán cumplir las condiciones establecidas en la letra a) del artículo 8 de la Directiva 92/65/CEE.
1. Las grasas extraídas derivadas de materiales de las categorías 1 o 2 destinadas para usos oleoquímicos deberán producirse con arreglo a uno de los métodos de transformación 1 a 5 recogidos en el capítulo III del anexo IV.
2. Las grasas extraídas de rumiantes deberán purificarse de forma que los niveles máximos de impurezas insolubles restantes no superen un 0,15 % del peso.
1. Podrán utilizarse los procesos siguientes para producir derivados de grasas a partir de grasas extraídas procedentes de material de las categorías 1 y 2:
a) transesterificación o hidrólisis a una temperatura mínima de 200 °C, a la presión apropiada, durante 20 minutos (glicerol, ácidos grasos y ésteres);
b) saponificación con NaOH 12M (glicerol y jabón):
i) mediante un proceso discontinuo a 95 °C durante 3 horas, o
ii) mediante un proceso continuo a 140 °C, a 2 bares (2000 hPa) durante ocho minutos, o
c) hidrogenización a 160 °C a 12 bares (12000 hPa) de presión durante 20 minutos.
2. Los derivados de grasas fabricados de conformidad con el presente capítulo podrán introducirse en el mercado únicamente:
a) para otros usos distintos de piensos, cosméticos o medicamentos;
b) asimismo, en el caso de derivados de grasas de material de la categoría 1, para otros usos distintos de abonos y enmiendas del suelo de origen orgánico.
La introducción en el mercado de cuernos y productos a base de cuerno, salvo la harina de cuerno, y de pezuñas y productos a base de pezuña, salvo la harina de pezuña, destinados a la producción de abonos o enmiendas del suelo de origen orgánico estará sujeta a las condiciones siguientes:
a) deberán proceder de animales que:
i) hayan sido sacrificados en un matadero tras haber sido sometidos a una inspección ante mórtem y, a raíz de dicha inspección, hayan sido declarados aptos para el sacrificio con vistas al consumo humano de conformidad con la legislación de la Unión, o
ii) no presentaban signos clínicos de ninguna enfermedad transmisible a personas o animales a través de esos productos;
b) deberán haberse sometido a un tratamiento térmico durante una hora a una temperatura mínima de 80 °C en su núcleo;
c) los cuernos deberán haberse retirado sin abrir la cavidad craneal;
d) han sido objeto de todas las precauciones necesarias en todas las fases de transformación, almacenamiento y transporte para evitar contaminaciones cruzadas;
e) deberán ir en envases o contenedores nuevos, o transportarse en vehículos o contenedores a granel que hayan sido desinfectados, antes de la carga, con un producto aprobado por la autoridad competente;
f) los envases o contenedores deberán:
i) indicar el tipo de producto (como cuernos, productos a base de cuerno, pezuñas o productos a base de pezuña);
ii) estar marcados con el nombre y la dirección del establecimiento o planta de destino autorizados o registrados.
Según se contempla en el artículo 41, apartado 1, letra a), y en el artículo 41, apartado 3, del Reglamento (CE) nº 1069/2009, las partidas importadas de materiales de la categoría 3 y los productos derivados de los mismos para su uso en la cadena alimentaria animal salvo en alimentos para animales de compañía y piensos para animales de peletería, así como las partidas de dichos materiales y productos en tránsito deberán cumplir las siguientes condiciones:
a) deberán consistir o haberse elaborado a partir de materiales de la categoría 3, si procede, indicado en la columna "materias primas" del cuadro 1;
b) deberán satisfacer las condiciones de importación y tránsito definidas en la columna "condiciones de importación y tránsito" del cuadro 1;
c) deberán proceder de un tercer país o parte de un tercer país que figure en la columna "lista de terceros países" del cuadro 1, y
d) irán acompañadas durante su transporte hasta el punto de entrada en la Unión en el cual se realizarán los controles veterinarios por el certificado sanitario indicado en la columna "certificados/modelos de documentos" del cuadro 1, o
e) se presentarán en el punto de entrada en la Unión donde se realizarán los controles veterinarios acompañadas por un documento correspondiente al modelo indicado en la columna "certificados/modelos de documentos" del cuadro 1.
Cuadro 1
|
No |
Producto |
Materias primas [referencia a las disposiciones del Reglamento (CE) nº 1609/2009] |
Condiciones de importación y tránsito |
Listas de terceros países |
Certificados/modelos de documentos |
||||||||||||||||
|
1 |
Proteína animal transformada |
Los materiales de la categoría 3 mencionados en el artículo 10, letras a), b), d), e), f), h), i), j), k), l) y m). |
|
|
Anexo XV, capítulo 1. |
||||||||||||||||
|
2 |
Hemoderivados para piensos |
Los materiales de la categoría 3 mencionados en el artículo 10, letra a), y artículo 10, letra b), inciso i). |
Los hemoderivados deberán haberse elaborado de conformidad con la sección 2 del capítulo II del anexo X. |
|
anexo XV, capítulo 4, letra B). |
||||||||||||||||
|
3 |
Grasas extraídas y aceites de pescado |
|
|
|
|
||||||||||||||||
|
4 |
Leche, productos lácteos y productos derivados de la leche, calostro y productos a base de calostro |
|
La leche, los productos lácteos, el calostro y los productos a base de calostro deberán cumplir las condiciones adicionales establecidas en la sección 4 del presente capítulo. |
|
|
||||||||||||||||
|
5 |
Gelatina y proteína hidrolizada |
Los materiales de la categoría 3 mencionados en el artículo 10, letras a), b), e), f), g), i) y j), y en el caso de proteína hidrolizada: los materiales de la categoría 3 mencionados en el artículo 10, letras d), h) y k). |
La gelatina y proteína hidrolizada deberá haberse elaborado de conformidad con la sección 5 del capítulo II del anexo X. |
|
|
||||||||||||||||
|
6 |
Fosfato dicálcico |
Los materiales de la categoría 3 mencionados en el artículo 10, letras a), b), d), e), f), g), h), i), j) y k). |
El fosfato dicálcico deberá haberse elaborado de conformidad con la sección 6 del capítulo II del anexo X. |
los terceros países que figuran en la parte 1 del anexo II del Reglamento (UE) nº 206/2010, y los países siguientes:
|
Anexo XV, capítulo 12. |
||||||||||||||||
|
7 |
Fosfato tricálcico |
Los materiales de la categoría 3 mencionados en el artículo 10, letras a), b), d), e), f), g), h), i) y k). |
El fosfato tricálcico deberá haberse elaborado de conformidad con la sección 7 del capítulo II del anexo X. |
los terceros países que figuran en la parte 1 del anexo II del Reglamento (UE) nº 206/2010, y los países siguientes:
|
Anexo XV, capítulo 12. |
||||||||||||||||
|
8 |
Colágeno |
Los materiales de la categoría 3 mencionados en el artículo 10, letras a), b), e), f), g), i) y j). |
El colágeno deberá haberse elaborado de conformidad con la sección 2 del capítulo II del anexo X. |
los terceros países que figuran en la parte 1 del anexo II del Reglamento (UE) nº 206/2010, y los países siguientes:
|
Anexo XV, capítulo 11. |
||||||||||||||||
|
9 |
Ovoproductos |
Los materiales de la categoría 3 mencionados en el artículo 10, letras e) y f), y artículo 10, letra k), inciso ii). |
Los ovoproductos deberán haberse elaborado de conformidad con la sección 9 del capítulo II del anexo X. |
Los terceros países que figuran en la parte 1 del anexo II del Reglamento (UE) nº 206/2010, y los terceros países o partes de terceros países que figuran en la parte 1 del anexo I del Reglamento (CE) nº 798/2008 desde los cuales los Estados miembros autorizan la importación de carne fresca de aves de corral, huevos y ovoproductos. |
Anexo XV, capítulo 15. |
Las siguientes condiciones se aplicarán a la importación de proteínas animales transformadas:
1. Con anterioridad al despacho a libre circulación en la Unión de los lotes, la autoridad competente deberá efectuar controles por muestreo de las proteínas animales transformadas importadas en el puesto de inspección fronterizo, con arreglo a las disposiciones generales del capítulo I del anexo X.
La autoridad competente procederá además a lo siguiente:
a) efectuar controles por muestreo de cada lote de productos transportados a granel;
b) efectuar controles por muestreo aleatorio de los lotes de productos envasados en la fábrica de origen.
2. Como excepción al punto 1, cuando seis controles consecutivos sobre lotes a granel originarios de un tercer país determinado resulten negativos, la autoridad competente del puesto de inspección fronterizo podrá efectuar controles por muestreo aleatorio de los sucesivos lotes a granel originarios de ese mismo tercer país.
Si uno de estos controles resultara positivo, la autoridad competente encargada del mismo deberá informar al respecto a la autoridad competente del tercer país de origen, de forma que ésta pueda tomar las medidas adecuadas para poner remedio a la situación.
La autoridad competente del tercer país de origen deberá comunicar dichas medidas a la autoridad competente responsable de los controles de importación.
En caso de que vuelva a obtenerse un resultado positivo para productos de la misma procedencia, la autoridad competente del puesto de inspección fronterizo deberá efectuar controles por muestreo sobre cada lote de la misma procedencia hasta que seis controles consecutivos resulten negativos.
3. Las autoridades competentes deberán llevar un registro de los resultados de los controles efectuados en todos los lotes de los que se hayan tomado muestras durante tres años como mínimo.
4. Cuando el resultado de las pruebas de detección de Salmonella en un lote importado a la Unión sea positivo o cuando el lote no cumpla las normas microbiológicas para Enterobacteriaceae definidas en el capítulo I del anexo X, el lote deberá:
a) tratarse conforme al procedimiento establecido en el artículo 17, apartado 2, letra a), de la Directiva 97/78/CE, o
b) transformarse de nuevo en una planta de transformación o descontaminarse mediante un tratamiento autorizado por la autoridad competente. El lote no deberá despacharse hasta que haya sido tratado y sometido a pruebas de detección de Salmonella o Enterobacteriaceae, según proceda, por la autoridad competente, de conformidad con el capítulo I del anexo X, con resultados negativos.
Las siguientes condiciones se aplicarán a la importación de grasas extraídas:
Las grasas extraídas deberán:
a) derivarse total o parcialmente de materia prima de porcino y proceder de un tercer país o parte del territorio de un tercer país que haya estado indemne de fiebre aftosa en los veinticuatro meses anteriores y de peste porcina clásica y peste porcina africana en los doce meses anteriores;
b) derivarse total o parcialmente de materia prima de aves de corral y proceder de un tercer país o parte del territorio de un tercer país que haya estado indemne de enfermedad de Newcastle y de influenza aviar durante los seis meses anteriores;
c) derivarse total o parcialmente de materia prima de rumiantes y proceder de un tercer país o parte del territorio de un tercer país que haya estado indemne de fiebre aftosa en los veinticuatro meses anteriores y de peste bovina en los doce meses anteriores, o
d) habiéndose producido un brote de las enfermedades mencionadas en las letras a), b) y c) durante los períodos correspondientes en cada una de ellas, haber sido sometidas a uno de los tratamientos térmicos siguientes:
i) al menos 70 °C durante treinta minutos como mínimo, o
ii) al menos 90 °C durante quince minutos como mínimo,
Los explotadores deberán recoger y conservar datos sobre los puntos de control crítico de forma que el propietario, el encargado o su representante y, en caso necesario, la autoridad competente, puedan proceder al control del funcionamiento de la planta; entre los datos que es preciso registrar y controlar se incluyen la dimensión granulométrica, la temperatura crítica y, según proceda, el tiempo absoluto, el perfil de presión, la velocidad de alimentación de la materia prima y el coeficiente de reciclado de la grasa.
A. Las siguientes condiciones se aplicarán a la importación de leche, productos lácteos, productos derivados de la leche, calostro y productos a base de calostro:
1. La leche, productos lácteos y derivados de la leche deberán:
a) haberse sometido al menos a uno de los tratamientos previstos en los puntos 1.1, 1.2, 1.3 y en la letra a) del punto B.1.4 de la parte I de la sección 4 del capítulo II del anexo X;
b) cumplir lo dispuesto en los puntos B.2 y B.4, y, en el caso del lactosuero, el punto B.3 de la parte I de la sección 4 del capítulo II del anexo X.
2. No obstante lo dispuesto en el punto B.1.4 de la parte I de la sección 4 del capítulo II del anexo X, se podrá importar leche, productos lácteos y productos derivados de la leche de los terceros países autorizados al efecto que figuran en la columna A del anexo I del Reglamento (UE) nº 605/2010, si la leche, los productos lácteos o los productos derivados han sido sometidos a un único tratamiento HTST y:
a) no se han enviado antes de que haya transcurrido un plazo mínimo de 21 días a partir de la producción, sin que durante dicho período se haya detectado caso alguno de fiebre aftosa en el tercer país exportador, o
b) han sido presentados en un puesto de inspección fronterizo de entrada en la Unión como mínimo 21 días después de su producción, sin que durante dicho período se haya detectado caso alguno de fiebre aftosa en el tercer país exportador.
B. Las siguientes condiciones se aplicarán a la importación de calostro y productos a base de calostro:
1. Los materiales han sido sometidos a un único tratamiento HTST y:
a) no se han enviado antes de que haya transcurrido un plazo mínimo de 21 días a partir de la producción, sin que durante dicho período se haya detectado caso alguno de fiebre aftosa en el tercer país exportador, o
b) han sido presentados en un puesto de inspección fronterizo de entrada en la Unión como mínimo 21 días después de su producción, sin que durante dicho período se haya detectado caso alguno de fiebre aftosa en el tercer país exportador.
2. Los materiales han sido obtenidos de animales bovinos sometidos a inspecciones veterinarias periódicas para garantizar que proceden de explotaciones en las que todos los rebaños bovinos:
a) bien están reconocidos como oficialmente indemnes de tuberculosis y oficialmente indemnes de brucelosis, tal como se define en el artículo 2, apartado 2, letras d) y f), de la Directiva 64/432/CEE, o no tienen ninguna restricción con arreglo a la legislación nacional del tercer país de origen del calostro por lo que se refiere a la erradicación de la tuberculosis y la brucelosis, y
b) bien están reconocidos como oficialmente indemnes de leucosis bovina enzoótica, tal como se define en el artículo 2, apartado 2, letra j), de la Directiva 64/432/CEE, o están incluidos en un sistema oficial para el control de la leucosis bovina enzoótica y no ha habido en el rebaño ningún resultado de pruebas clínicas y de laboratorio que indique la existencia de dicha enfermedad durante los últimos dos años.
3. Una vez concluido el tratamiento, se habrán adoptado todas las precauciones necesarias para evitar la contaminación del calostro o los productos a base de calostro.
4. El producto final deberá haberse etiquetado para indicar que contiene material de la categoría 3 y que no está destinado al consumo humano, y:
a) envasarse en recipientes nuevos, o
b) transportarse a granel en contenedores u otros medios de transporte cuidadosamente limpiados y desinfectados antes de su utilización.
Según se contempla en el artículo 41, apartado 1, letra a), y en el artículo 41, apartado 3, del Reglamento (CE) nº 1069/2009, las partidas importadas de subproductos animales y productos derivados para su uso en fines externos a la cadena alimentaria de animales de granja y las partidas de dichos productos en tránsito deberán cumplir las siguientes condiciones específicas:
a) deberán consistir o haberse elaborado a partir de subproductos animales indicados en la columna "materias primas" del cuadro 2;
b) deberán satisfacer las condiciones de importación y tránsito definidas en la columna "condiciones de importación y tránsito" del cuadro 2;
c) deberán proceder de un tercer país o parte de un tercer país que figure en la columna "lista de terceros países" del cuadro 2, y
d) irán acompañadas durante su transporte hasta el punto de entrada en la Unión en el cual se realizarán los controles veterinarios por el certificado sanitario —o, en su caso, otro documento— indicado en la columna "certificados/modelos de documentos" del cuadro 2, o
e) se presentarán en el punto de entrada en la Unión donde se realizarán los controles veterinarios acompañadas por un documento correspondiente al modelo indicado en la columna "certificados/modelos de documentos" del cuadro 2.
Cuadro 2
|
No |
Producto |
Materias primas [referencia a las disposiciones del Reglamento (CE) nº 1069/2009] |
Condiciones de importación y tránsito |
Listas de terceros países |
Certificados/modelos de documentos |
||||||||||||||||||||||||||||||
|
1 |
Estiércol transformado, productos a base de estiércol transformado y guano de murciélago |
Los materiales de la categoría 2 mencionados en el artículo 9, letra a). |
El estiércol transformado, los productos derivados de estiércol transformado y el guano de murciélago deberán haberse elaborado de conformidad con lo dispuesto en la sección 2 del capítulo I del anexo XI. |
Los terceros países que figuran en:
|
Anexo XV, capítulo 17. |
||||||||||||||||||||||||||||||
|
2 |
Hemoderivados, excluidos los procedentes de équidos, para la fabricación de productos derivados para usos externos a la cadena alimentaria de animales de granja |
Los materiales de la categoría 1 mencionados en el artículo 8, letras c) y d) y los materiales de la categoría 3 mencionados en el artículo 10, letras a), b), d) y h). |
Los hemoderivados deberán haberse elaborado de conformidad con la sección 2. |
Los terceros países siguientes:
|
|
||||||||||||||||||||||||||||||
|
3 |
Sangre y hemoderivados de équidos |
Los materiales de la categoría 3 mencionados en el artículo 10, letras a), b), d) y h). |
La sangre y los hemoderivados deberán cumplir las condiciones establecidas en la sección 3. |
Los terceros países siguientes:
|
anexo XV, capítulo 4, letra A). |
||||||||||||||||||||||||||||||
|
4 |
Pieles frescas o refrigeradas de ungulados |
Los materiales de la categoría 3 mencionados en el artículo 10, letra a), y artículo 10, letra b), inciso iii). |
Las pieles deberán cumplir las condiciones adicionales establecidas en la sección 4, puntos 1 y 4. |
Las pieles proceden de un tercer país, o de una parte de un tercer país en caso de regionalización con arreglo a la normativa de la Unión, de la lista establecida en la parte 1 del anexo II del Reglamento (UE) nº 206/2010, desde los cuales está autorizada la importación de carne fresca de la misma especie. |
anexo XV, capítulo 5, letra A). |
||||||||||||||||||||||||||||||
|
5 |
Pieles tratadas de ungulados |
Los materiales de la categoría 3 mencionados en el artículo 10, letra a), artículo 10, letra b), incisos i) y iii), y artículo 10, letra n). |
Las pieles deberán cumplir las condiciones adicionales establecidas en la sección 4, puntos 2, 3 y 4. |
|
|
||||||||||||||||||||||||||||||
|
6 |
Trofeos de caza y otros preparados de animales |
Los materiales de la categoría 2 mencionados en el artículo 9, letra f), procedentes de animales salvajes no sospechosos de estar infectados por enfermedades transmisibles a personas o animales y los materiales de la categoría 3 mencionados en el artículo 10, letra a), artículo 10, letra b), incisos i), iii) y v), y artículo 10, letra n). |
Los trofeos de caza y otros preparados deberán cumplir las condiciones adicionales establecidas en la sección 5. |
|
|
||||||||||||||||||||||||||||||
|
7 |
Cerdas |
Los materiales de la categoría 3 mencionados en el artículo 10, letra b), inciso iv). |
Las cerdas deberán proceder de cerdos del país de origen, sacrificados en un matadero de dicho tercer país. |
|
|
||||||||||||||||||||||||||||||
|
8 |
Lana y pelo sin tratar |
Los materiales de la categoría 3 mencionados en el artículo 10, letras h) y n). |
La lana y el pelo sin tratar deberán
|
Cualquier tercer país. |
No será necesario el certificado sanitario para la importación de lana y pelo sin tratar. |
||||||||||||||||||||||||||||||
|
9 |
Plumas, partes de plumas y plumón transformados |
Los materiales de la categoría 3 mencionados en el artículo 10, letra b), inciso v), y artículo 10, letras h) y n). |
Las plumas o partes de plumas transformadas deberán cumplir las condiciones adicionales establecidas en la sección 6. |
Cualquier tercer país. |
No será necesario el certificado sanitario para la importación de plumas, partes de plumas y plumón sometidos a tratamiento. |
||||||||||||||||||||||||||||||
|
10 |
Subproductos de la apicultura |
Los materiales de la categoría 3 mencionados en el artículo 10, letra e). |
|
|
|
||||||||||||||||||||||||||||||
|
11 |
Huesos y productos óseos (excluida la harina de huesos y carne), cuernos y productos córneos (excluida la harina de cuernos) y pezuñas y productos a base de pezuña (excluida la harina de pezuñas) no destinados a ser utilizados como material para piensos, fertilizantes o enmiendas del suelo de origen orgánico |
Los materiales de la categoría 3 mencionados en el artículo 10, letra a), artículo 10, letra b), incisos i) y iii), y artículo 10, letra n). |
Los productos cumplirán los requisitos establecidos en la sección 7. |
Cualquier tercer país. |
Los productos irán acompañados de:
|
||||||||||||||||||||||||||||||
|
12 |
Alimentos para animales de compañía y accesorios masticables para perros |
|
Los alimentos para animales de compañía y los accesorios masticables para perros deberán haberse elaborado de conformidad con el capítulo II del anexo XIII. |
|
|
||||||||||||||||||||||||||||||
|
13 |
Subproductos aromatizantes para la fabricación de alimentos de animales de compañía |
Los materiales mencionados en el artículo 35, letra a). |
Los subproductos aromatizantes deberán haberse elaborado de conformidad con el capítulo III del anexo XIII. |
Los terceros países que figuran en la Parte 1 del anexo II del Reglamento (UE) nº 206/2010 desde los cuales los Estados miembros autorizan la importación de carne fresca de las mismas especies y en los que solo se autoriza la carne con hueso. En el caso de los subproductos aromatizantes de pescado, los terceros países que figuran en el anexo II de la Decisión 2006/766/CE |
Anexo XV, capítulo 3, letra E). |
||||||||||||||||||||||||||||||
|
14 |
Subproductos animales para la fabricación de productos alimentos para animales de compañía distintos de los alimentos crudos y de productos derivados para usos externos a la cadena alimentaria animal |
|
Los productos cumplirán los requisitos establecidos en la sección 8. |
|
|
||||||||||||||||||||||||||||||
|
15 |
Subproductos animales para uso como alimentos de animales de compañía |
Los materiales de la categoría 3 mencionados en el artículo 10, letra a), y artículo 10, letra b), incisos i) y ii). |
Los productos cumplirán los requisitos establecidos en la sección 8. |
Los terceros países que figuran en la Parte 1 del anexo II del Reglamento (UE) nº 206/2010 desde los cuales los Estados miembros autorizan la importación de carne fresca de las mismas especies y en los que solo se autoriza la carne con hueso. En el caso de material de pescado, los terceros países que figuran en el anexo II de la Decisión 2006/766/CE. |
Anexo XV, capítulo 3, letra D). |
||||||||||||||||||||||||||||||
|
16 |
Subproductos animales para uso como pienso para animales de peletería: |
Los materiales de la categoría 3 mencionados en el artículo 10, letra a), y artículo 10, letra b), incisos i) y ii). |
Los productos cumplirán los requisitos establecidos en la sección 8. |
Los terceros países que figuran en la Parte 1 del anexo II del Reglamento (UE) nº 206/2010 o en el anexo I del Reglamento (CE) nº 798/2008 desde los cuales los Estados miembros autorizan la importación de carne fresca de las mismas especies y en los que solo se autoriza la carne con hueso. En el caso de material de pescado, los terceros países que figuran en el anexo II de la Decisión 2006/766/CE. |
Anexo XV, capítulo 3, letra D). |
||||||||||||||||||||||||||||||
|
17 |
Grasas extraídas para determinados usos externos a la cadena alimentaria de animales de granja |
|
Las grasas extraídas cumplirán los requisitos establecidos en la sección 9. |
Los terceros países que figuran en la parte 1 del anexo II del Reglamento (UE) nº 206/2010 y, en el caso de los materiales de pescado, los terceros países que figuran en el anexo II de la Decisión 2006/766/CE. |
anexo XV, capítulo 10, letra B). |
||||||||||||||||||||||||||||||
|
18 |
Derivados de grasas |
|
Los derivados de grasas extraídas cumplirán los requisitos establecidos en la sección 10. |
Cualquier tercer país. |
|
||||||||||||||||||||||||||||||
|
19 |
Gelatina fotográfica |
Los materiales de la categoría 1 mencionados en el artículo 8, letra b), y los materiales de la categoría 3 mencionados en el artículo 10. |
La gelatina fotográfica cumplirá los requisitos establecidos en la sección 11. |
La gelatina fotográfica solo podrá importarse de establecimientos de origen en los Estados Unidos y en Japón que sean autorizados conforme a lo dispuesto en la sección 11. |
Anexo XV, capítulo 19. |
||||||||||||||||||||||||||||||
|
20 |
Cuernos y productos a base de cuerno, salvo la harina de cuerno, y pezuñas y productos a base de pezuña, salvo la harina de pezuña, destinados a la producción de abonos o enmiendas del suelo de origen orgánico |
Los materiales de la categoría 3 mencionados en el artículo 10, letras a), b), h) y n). |
Los productos cumplirán los requisitos establecidos en la sección 12. |
Cualquier tercer país. |
Anexo XV, capítulo 18. |
Las siguientes condiciones serán de aplicación a la importación de sangre y hemoderivados, excluidos los procedentes de équidos, para la fabricación de productos derivados para usos externos a la cadena alimentaria de animales de granja:
1. Los hemoderivados deberán proceder de una planta de producción de productos derivados para usos externos a la cadena alimentaria de animales de granja que satisfaga las condiciones específicas establecidas en el presente Reglamento o de un establecimiento de recogida.
2. La sangre a partir de la cual se elaboran los hemoderivados para la fabricación de productos derivados para usos externos a la cadena alimentaria de animales de granja deberá haberse recogido:
a) en mataderos autorizados con arreglo a la legislación de la Unión;
b) en mataderos autorizados y supervisados por la autoridad competente del tercer país; o
c) de animales vivos en instalaciones aprobadas y supervisadas por la autoridad competente del tercer país.
3.1. En el caso de los hemoderivados para la fabricación de productos derivados para usos externos a la cadena de alimentación de animales de granja procedentes de animales pertenecientes a los órdenes de los artiodáctilos, los perisodáctilos y los proboscídeos, incluidos sus cruces, deberán cumplir bien las condiciones de la letra a), bien las de la letra b):
a) los productos deberán haberse sometido a uno de los tratamientos que se indican a continuación, garantizándose así la ausencia de agentes patógenos de las enfermedades a que se hace referencia en la letra b):
i) tratamiento térmico a una temperatura de 65 °C durante al menos tres horas, seguido de un control de eficacia;
ii) irradiación a 25 kGy mediante rayos gamma, seguida de un control de eficacia;
iii) tratamiento térmico a una temperatura mínima de 80 °C en toda su masa, seguido de un control de eficacia;
iv) únicamente en el caso de los animales distintos de los suidos y los tayasuidos: modificación del pH a 5 durante dos horas, seguida de un control de eficacia;
b) en el caso de los hemoderivados no tratados de conformidad con la letra a), los productos deberán proceder de un tercer país o de una región:
i) en los que no se ha registrado ningún caso de peste bovina, peste de los pequeños rumiantes ni fiebre del Valle del Rift como mínimo en los doce meses previos y en los que no se han realizado vacunaciones contra esas enfermedades como mínimo durante el mismo período;
ii) en los que no se ha registrado ningún caso de fiebre aftosa durante los 12 meses previos, y
- en los que no se han realizado vacunaciones contra esta enfermedad como mínimo durante los 12 meses previos, o
- en los que se están llevando a cabo y se están controlando oficialmente programas de vacunación contra esa enfermedad en rumiantes domésticos al menos en los 12 meses previos; en este caso, tras los controles veterinarios previstos en la Directiva 97/78/CE, y de conformidad con las condiciones fijadas en el artículo 8, apartado 4, de dicha Directiva, los productos deberán transportarse directamente a la planta técnica de destino y deberán adoptarse todas las precauciones, incluida la eliminación segura de los residuos y del material no utilizado o sobrante, con el propósito de evitar todo riesgo de propagación de enfermedades a personas o animales.
3.2. Además de lo dispuesto en el punto 3.1, letra b), incisos i) e ii), en el caso de los animales distintos de los suidos y los tayasuidos, deberá cumplirse una de las condiciones siguientes:
a) en el tercer país o la región de origen no se ha registrado ningún caso de estomatitis vesicular ni de lengua azul (incluida la presencia de animales seropositivos) como mínimo en los doce meses previos y no se han realizado vacunaciones contra esas enfermedades en las especies sensibles como mínimo durante el mismo período;
b) tras los controles veterinarios previstos en la Directiva 97/78/CE, y de conformidad con las condiciones fijadas en el artículo 8, apartado 4, de dicha Directiva, los productos deberán transportarse directamente a la planta de destino y deberán adoptarse todas las precauciones, incluida la eliminación segura de los residuos y del material no utilizado o sobrante, con el propósito de evitar todo riesgo de propagación de enfermedades a personas o animales.
3.3. Además de lo dispuesto en el punto 3.1, letra b), incisos i) y ii), en el caso de los suidos y los tayasuidos, en el tercer país o la región de origen no se ha registrado ningún caso de enfermedad vesicular porcina, peste porcina clásica ni peste porcina africana como mínimo en los doce meses previos, no se han realizado vacunaciones contra esas enfermedades como mínimo durante el mismo período y se cumple una de las condiciones siguientes:
a) en el país o la región de origen no se ha registrado ningún caso de estomatitis vesicular (incluida la presencia de animales seropositivos) en los doce meses previos y no se han realizado vacunaciones contra esa enfermedad en las especies sensibles como mínimo durante el mismo período;
b) tras los controles veterinarios previstos en la Directiva 97/78/CE, y de conformidad con las condiciones fijadas en el artículo 8, apartado 4, de dicha Directiva, los productos deberán transportarse directamente al establecimiento o planta de destino registrados y deberán adoptarse todas las precauciones, incluida la eliminación segura de los residuos y del material no utilizado o sobrante, con el propósito de evitar todo riesgo de propagación de enfermedades a personas o animales.
4. En el caso de los hemoderivados para la fabricación de productos derivados para usos externos a la cadena de alimentación de animales de granja procedentes de aves de corral y otras especies aviares, deberán cumplir bien las condiciones de la letra a), bien las de la letra b):
a) los productos deberán haberse sometido a uno de los tratamientos que se indican a continuación, garantizándose así la ausencia de agentes patógenos de las enfermedades a que se hace referencia en la letra b):
i) tratamiento térmico a una temperatura de 65 °C durante al menos tres horas, seguido de un control de eficacia;
ii) irradiación a 25 kGy mediante rayos gamma, seguida de un control de eficacia;
iii) tratamiento térmico a una temperatura mínima de 70 °C en toda su masa, seguido de un control de eficacia;
b) en el caso de los hemoderivados no tratados de conformidad con la letra a), los productos deberán proceder de un tercer país o de una región:
i) que han estado indemnes de la enfermedad de Newcastle y de la influenza aviar altamente patógena, tal como se recoge en el Código Sanitario para los Animales Terrestres de la OIE, edición de 2010;
ii) que durante los últimos 12 meses no han realizado vacunaciones contra la influenza aviar;
iii) en los cuales las aves de corral u otras especies aviares de las que derivan los productos no fueron vacunadas contra la enfermedad de Newcastle con vacunas preparadas a partir de una cepa madre del virus de la enfermedad de Newcastle con una patogenicidad superior a la de las cepas lentógenas del virus.
Las siguientes condiciones se aplicarán a la importación de sangre y hemoderivados de équidos:
1. La sangre deberá cumplir las condiciones establecidas en la letra a) del punto 1 del capítulo IV del anexo XIII y recogerse bajo supervisión veterinaria:
a) en mataderos
i) autorizados de acuerdo con el Reglamento (CE) nº 853/2004, o
ii) autorizados y supervisados por la autoridad competente del tercer país, o
b) en instalaciones autorizadas y provistas de un número de autorización veterinaria y supervisadas por la autoridad competente del tercer país a efectos de la recogida de sangre de équidos para la producción de hemoderivados con fines distintos de la alimentación animal.
2. Los hemoderivados deberán cumplir las condiciones establecidas en el punto 2 del capítulo IV del anexo XIII.
Además, los hemoderivados contemplados en el punto 2, letra b), inciso i), del capítulo IV del anexo XIII deberán haberse elaborado a partir de sangre de équidos que hayan permanecido al menos los tres meses previos a la fecha de la recogida, o desde su nacimiento si tienen menos de tres meses, en explotaciones bajo supervisión veterinaria en el tercer país de recogida y, en ese período y el período de recogida de la sangre, ha estado indemne de:
a) peste equina africana con arreglo al artículo 5, apartado 2, letra a), párrafo segundo, letras a) y b), de la Directiva 2009/156/CE;
b) encefalomielitis equina venezolana desde hace al menos dos años;
c) muermo:
i) desde hace tres años; o
ii) desde hace seis meses, en los que los animales no hayan presentado ningún signo clínico de muermo (Burkholderia mallei) en la inspección post mortem efectuada en el matadero mencionado en la letra a) del punto 1, incluido un minucioso examen de las membranas mucosas de la tráquea, la laringe, las cavidades nasales y los senos y sus ramificaciones, previa incisión de la cabeza en el plano mediano y ablación del tabique nasal;
d) en el caso de hemoderivados distintos del suero, estomatitis vesicular desde hace seis meses como mínimo.
3. Los hemoderivados deberán proceder de un establecimiento o planta que haya sido autorizado o registrado por la autoridad competente del tercer país.
4. La sangre y los hemoderivados se envasarán y se etiquetarán de acuerdo con lo dispuesto en el punto 3 del capítulo IV del anexo XIII.
Las siguientes condiciones se aplicarán a la importación de pieles de ungulados:
1. Las pieles frescas o refrigeradas se podrán importar si:
a) proceden de un tercer país que figura en la columna correspondiente de la fila 4 del cuadro 2 de la sección 1 y, en función de la especie en cuestión, que:
i) en los doce meses anteriores a la expedición de los productos, no ha padecido ninguna de las enfermedades que se indican a continuación:
- peste porcina clásica,
- peste porcina africana,
- peste bovina, y
ii) ha estado indemne de fiebre aftosa al menos durante los 12 meses previos a la fecha de envío y no se ha practicado vacunación alguna contra esta enfermedad en el mismo período;
b) han sido obtenidas a partir de:
i) animales que han permanecido en el territorio del tercer país de origen al menos durante los tres meses anteriores a su sacrificio o desde su nacimiento, en el caso de los animales de menos de tres meses;
ii) en el caso de las pieles de biungulados, animales que proceden de explotaciones donde no se ha producido ningún brote de fiebre aftosa durante los treinta días anteriores y en un radio de 10 km en torno a la cual no se ha registrado ningún caso de fiebre aftosa en los treinta días anteriores;
iii) en el caso de las pieles de cerdo, animales que proceden de explotaciones en las que no se ha producido ningún brote de enfermedad vesicular porcina durante los treinta días anteriores ni de peste porcina clásica o africana durante los cuarenta días anteriores y en un radio de 10 km en torno a las cuales no se ha registrado ningún caso de estas enfermedades en los treinta días anteriores, o
iv) animales que han pasado la inspección sanitaria ante mórtem en el matadero en las veinticuatro horas anteriores a su sacrificio sin presentar signo alguno de fiebre aftosa, peste bovina, peste porcina clásica, peste porcina africana o enfermedad vesicular porcina, y
c) han sido objeto de todas las precauciones necesarias para evitar su contaminación con agentes patógenos.
2. Las pieles tratadas mencionadas en la letra C, apartado 2, del capítulo V del anexo XIII podrán importarse sin restricciones.
3. Podrán importarse otras pieles frescas si:
a) proceden de:
i) un tercer país, o una parte de un tercer país en caso de regionalización con arreglo a la normativa de la Unión, que figure en la lista de la letra a) de la columna "lista de terceros países" de la fila no 5 del cuadro 2 dispuesto en la sección 1 del presente anexo desde donde está autorizada la importación de carne fresca de las especies correspondientes, y han sido tratadas de acuerdo con lo establecido en las letras a), b) y c) del punto 28 del anexo I;
ii) un tercer país que figure en la lista establecida en el apartado a) de la columna correspondiente de la fila no 5 del cuadro 2 dispuesto en la sección 1 y han sido tratadas conforme a lo dispuesto en el punto 28, letras c) o d) del anexo I, o
iii) équidos o rumiantes de un tercer país de la lista establecida en la letra b) de la columna "lista de terceros países" de la fila no 5 del cuadro 2 dispuesto en la sección 1, y han sido tratados de acuerdo con lo establecido en el punto 28, letras a), b) y c) del anexo I y, después del tratamiento, se han mantenido aisladas durante un mínimo de 21 días, y
b) en el caso de las pieles saladas transportadas por barco, han sido tratadas de conformidad con lo dispuesto en el apartado 28, letras b) o c) del anexo I y, después del tratamiento, se han transportado aisladas durante al menos catorce días en el caso contemplado en el punto 28, letra b) y durante siete días en el caso contemplado en el punto 28, letra c) antes de su importación, y el certificado sanitario que las acompaña acredita ese tratamiento y la duración del transporte.
4. Las pieles de ungulados frescas, refrigeradas o tratadas deberán importarse en contenedores, vehículos de carretera, vagones de tren o fardos precintados bajo la responsabilidad de la autoridad competente del tercer país expedidor.
Las siguientes condiciones se aplicarán a la importación de trofeos de caza y otros preparados de animales:
1. Los trofeos de caza y otros preparados de animales que satisfacen las condiciones mencionadas en las letras B y C, punto 1 del capítulo VI del anexo XIII podrán importarse sin restricciones.
2. Los trofeos de caza y otros preparados de aves y ungulados, compuestos únicamente de huesos, cuernos, pezuñas, garras, astas, dientes o pieles podrán importarse de terceros países si satisfacen las condiciones establecidas en la letra C, apartado 1, letra a), letra C, apartado 2, letra a), incisos i) a iii) y letra b), incisos i) y ii) del capítulo VI del anexo XIII.
No obstante, cuando se trate de pieles saladas en seco o en salmuera que se transporten en barco no será necesario que las pieles hayan sido saladas catorce días antes de su expedición siempre que hayan sido saladas durante al menos catorce días antes de su importación.
3. Los trofeos de caza u otros preparados de aves y ungulados compuestos por partes anatómicas enteras no tratadas podrán importarse si:
a) proceden de animales originarios de una zona que no esté sometida a restricciones derivadas de la aparición de enfermedades transmisibles graves a las que sean sensibles los animales de las especies en cuestión;
b) han sido envasados sin haber entrado en contacto con otros productos de origen animal con probabilidad de contaminarlos, en envases individuales, transparentes y cerrados para evitar cualquier contaminación posterior.
Las plumas, partes de plumas y plumón transformados podrán importarse:
a) si consisten en plumas decorativas tratadas, plumas transformadas que lleven los viajeros para su uso personal o envíos de plumas o plumón transformados destinadas a particulares y sin finalidad industrial, o
b) si van acompañados de un documento comercial que acredite que han sido tratados con una corriente de vapor o por otro método que garantice la eliminación de todo riesgo inaceptable y estén secos y en envases bien cerrados, y
c) si, salvo que el documento comercial indique que han sido lavados en fábrica y tratados con vapor caliente a 100 °C durante un mínimo de 30 minutos, se envían a un establecimiento o planta registrado para dicho tratamiento.
1. Los huesos y productos a base de hueso (salvo la harina de hueso), cuernos y productos a base de cuerno (salvo la harina de cuerno), pezuñas y productos a base de pezuña (salvo la harina de pezuña) podrán importarse para elaborar productos derivados destinados a usos externos a la cadena alimentaria animal siempre que:
a) los productos se sequen antes de la exportación a la Unión y no se refrigeren ni congelen;
b) los productos se transporten, únicamente por tierra o mar, directamente desde su tercer país de origen a un puesto de inspección fronterizo de entrada en la Unión, sin que medie transbordo alguno en cualquier puerto o lugar no perteneciente a la Unión;
c) los productos se envíen directamente al establecimiento o planta de destino registrados tras los controles documentales previstos en la Directiva 97/78/CE.
2. Cada partida deberá ir acompañada de un documento comercial sellado por la autoridad competente responsable de la supervisión del establecimiento de origen, que incluirá la información siguiente:
a) el tercer país de origen;
b) el nombre del establecimiento o planta de producción;
c) la naturaleza del producto (huesos secos/productos a base de huesos secos/cuernos secos/productos a base de cuernos secos/pezuñas secas/productos a base de pezuñas secas), y
d) la confirmación de que los productos:
i) proceden de animales sanos sacrificados en un matadero;
ii) han sido sometidos a un proceso de desecado durante 42 días a una temperatura media mínima de 20 °C;
iii) han sido calentados durante una hora hasta alcanzar una temperatura mínima de 80 °C en su núcleo antes de su secado;
iv) han sido incinerados durante una hora hasta alcanzar una temperatura mínima de 800 °C en su núcleo antes de su secado;
v) han sido sometidos a un proceso de acidificación que permita mantener un pH inferior a 6 en su núcleo durante al menos una hora antes de su secado, y no se prevé su desviación en ninguna fase para la alimentación humana o animal o su utilización como abonos o enmiendas del suelo.
3. En el momento de su expedición a la Unión, los productos deben colocarse en contenedores o camiones sellados o cargarse a granel en un buque.
Cuando se transporten en contenedores, éstos y, en cualquier caso, todos los documentos que acompañen a los productos, deberán llevar el nombre y la dirección del establecimiento o planta de destino registrados.
4. Tras los controles veterinarios previstos en la Directiva 97/78/CE y, de conformidad con las condiciones establecidas en el apartado 4 del artículo 8 de esa misma Directiva, el material deberá transportarse directamente al establecimiento o planta de destino registrados.
Los subproductos animales destinados a la fabricación de piensos para animales de peletería, alimentos para animales de compañía, distintos de los alimentos crudos para animales de compañía, y productos derivados para usos externos a la cadena alimentaria de animales de granja podrán importarse siempre que:
1. los subproductos animales hayan sido ultracongelados en la planta de origen o conservados de acuerdo con la legislación de la Unión de manera que no se deterioren entre el momento de su expedición y el de su entrega al establecimiento o planta de destino;
2. los subproductos animales han sido objeto de todas las precauciones necesarias para evitar su contaminación con agentes patógenos;
3. los subproductos animales han sido envasados con material nuevo a prueba de pérdidas o en envases limpiados y desinfectados antes de su uso;
4. tras los controles veterinarios previstos en la Directiva 97/78/CE y, de conformidad con las condiciones establecidas en el apartado 4 del artículo 8 de esa misma Directiva, los subproductos animales se transporten directamente:
a) a una fábrica de alimentos para animales de compañía o a un establecimiento o planta de destino registrados que hayan ofrecido garantías de que los subproductos animales solo se utilizarán en la elaboración de productos para los que esté autorizado o registrado, según el caso, de acuerdo con las especificaciones de la autoridad competente, si procede, y solo abandonarán el establecimiento o la planta sin tratamiento si van a ser eliminados directamente;
b) a un establecimiento o planta que haya sido autorizado conforme al artículo 24, apartado 1, letra h), del Reglamento (CE) nº 1069/2009;
c) a los locales de un usuario o centro de recogida registrados que hayan ofrecido garantías de que los subproductos animales solo van a utilizarse para los fines permitidos, de acuerdo con las especificaciones de la autoridad competente, si procede, o
d) a un establecimiento o planta que haya sido autorizado conforme al artículo 24, apartado 1, letra a), del Reglamento (CE) nº 1069/2009; y
5.1. en el caso de materias primas para elaboración de alimentos para animales de compañía contempladas en el artículo 35, letra a), inciso ii), del Reglamento (CE) nº 1069/2009, las materias primas:
a) hayan sido marcadas en el tercer país antes de su entrada en la Unión con una cruz de carbón vegetal licuado o carbono activado en todas las caras externas de cada bloque congelado o, si la materia prima se transporta en palés que no son separados en distintos envíos durante el transporte a la fábrica de alimentos para animales de compañía, en todas las caras externas de cada palé, de forma que la marca cubra al menos el 70 % de la longitud diagonal del lateral del bloque y tenga una anchura de al menos 10 centímetros;
b) si no están congeladas, hayan sido marcadas en el tercer país antes de su entrada en la Unión pulverizando sobre ellas carbón vegetal licuado o aplicándoles polvo de carbón vegetal de tal manera que sea claramente visible;
c) se transporten directamente:
i) a la planta de alimentos para animales de compañía, de acuerdo con lo dispuesto en la letra a) del punto 4, o
ii) a un establecimiento o planta autorizado de conformidad con lo dispuesto en el artículo 24, apartado 1, letra h), del Reglamento (CE) nº 1069/2009, de conformidad con el punto 4, letra b), de la presente sección y desde ahí, directamente a la planta de alimentos para animales de compañía contemplada en el inciso i), a condición de que dicha planta de destino:
- solo manipule material contemplado en el presente punto 5.1, o
- solo manipule material destinado a una planta de alimentos para animales de compañía según se recoge en el inciso i), y
d) Sean tratadas para eliminar el marcado previsto en los puntos (a) y (b) sólo en la planta de alimentos para animales de compañía de destino y sólo inmediatamente antes del uso del material para la elaboración de alimentos para animales de compañía de conformidad con las condiciones aplicables a los alimentos para animales de compañía elaborados a partir de materiales de la categoría 3 dispuestas en el capítulo II del anexo XIII;
5.2. en el caso de partidas compuestas de materias primas tratadas como se indica en el punto 5.1 anterior y de materias primas no tratadas, se habrán marcado todas las materias primas de la partida de acuerdo con lo establecido en las letras a) y b) del punto 5.1 anterior.
5.3. en el caso de materiales marcados de acuerdo con lo establecido en las letras a) y b) del punto 5.1 y en el punto 5.2, el marcado deberá ser visible desde la expedición hasta su recepción en la planta de destino;
6. en la planta de elaboración de alimentos para animales de compañía de destino, la materia prima para la elaboración de alimentos para animales de compañía contemplada en el artículo 35, letra a), inciso ii), del Reglamento (CE) nº 1069/2009 se almacenará antes de la elaboración, se utilizará y se eliminará en condiciones autorizadas por la autoridad competente, de forma que posibiliten la realización de controles oficiales sobre las cantidades de materias primas recibidas, usadas en el proceso de elaboración y eliminadas, si procede.
La autoridad competente podrá autorizar al explotador de la planta de alimentos para animales de compañía el almacenamiento de dichos materiales junto con los materiales de la categoría 3.
Las grasas extraídas no destinadas a la elaboración de piensos para animales de granja, la fabricación de cosméticos, medicamentos o productos sanitarios, podrán importarse a condición de que:
a) se deriven:
i) en el caso de material destinado a la producción de biodiésel, de los subproductos animales indicados en los artículos 8, 9 y 10 del Reglamento (CE) nº 1069/2009;
ii) en el caso de material destinado a la producción de abonos y enmiendas del suelo de origen orgánico, de los materiales de la categoría 2 contemplados en el artículo 9, letras c) y d), y artículo 9, letra f), inciso i), del Reglamento (CE) nº 1069/2009, o los materiales de la categoría 3, distintos de los materiales contemplados en el artículo 10, letras c) y p), del Reglamento (CE) nº 1069/2009;
iii) en el caso de otro material, los materiales de la categoría 1 mencionados en el artículo 8, letras b), c) y d), del Reglamento (CE) nº 1069/2009, los materiales de la categoría 2 contemplados en el artículo 9, letras c) y d), y artículo 9, letra f), inciso i), del Reglamento (CE) nº 1069/2009 o los materiales de la categoría 3, distintos de los contemplados en el artículo 10, letras c) y p), del Reglamento (CE) nº 1069/2009;
b) hayan sido transformadas por el método de transformación 1 (esterilización a presión) o de conformidad con alguno de los métodos de transformación contemplados en el capítulo III del anexo IV;
c) en el caso de grasas procedentes de rumiantes, han sido eliminadas las impurezas insolubles que superen un 0,15 % del peso;
d) han sido marcadas antes de su envío a la Unión de forma que se consiga la concentración mínima de GTH mencionada en el punto 1, letra b), del capítulo V del anexo VIII;
e) tras los controles veterinarios previstos en la Directiva 97/78/CE, las grasas extraídas se transporten directamente al establecimiento o planta de destino registrados, en condiciones que impidan la contaminación, y
f) estén etiquetadas con la indicación "NO APTO PARA EL CONSUMO HUMANO O ANIMAL" en su envase o recipiente.
1. Podrán importarse los derivados de grasas si el certificado sanitario que acompaña al lote certifica:
a) si los derivados de grasas proceden o no de materiales de las categorías 1, 2 o 3;
b) en el caso de derivados de grasas de materiales de la categoría 2, si los productos:
i) han sido elaborados mediante un método que cumpla como mínimo las normas de uno de los procesos descritos en el punto 1 del capítulo XI del anexo XIII, y
ii) van a utilizarse únicamente en abonos o enmiendas del suelo de origen orgánico, u otros usos externos a la cadena alimentaria de animales de granja, excepto en cosméticos, fármacos y productos médicos.
c) en el caso de derivados de grasas elaborados a partir de materiales de la categoría 1, que los productos no deberán emplearse en abonos o enmiendas del suelo de origen orgánico, cosméticos, medicamentos y productos sanitarios; no obstante, podrán emplearse con otros fines externos a la cadena alimentaria de animales de granja.
2. El certificado sanitario al que se hace referencia en el punto 1 deberá presentarse a la autoridad competente del puesto de inspección fronterizo del primer punto de entrada de las mercancías en la Unión, y una copia del mismo deberá acompañar al envío hasta la planta de destino.
3. Tras los controles veterinarios previstos en la Directiva 97/78/CE, y de conformidad con las condiciones establecidas en el apartado 4 del artículo 8 de dicha Directiva, los derivados de grasas deberán transportarse directamente a los establecimientos o plantas de destino registrados.
1. La gelatina elaborada a partir de material que consista en columnas vertebrales de bovinos compuestas por material de la categoría 1 de conformidad con lo dispuesto en el artículo 8, letra b), del Reglamento (CE) nº 1069/2009 y que está destinada a la industria fotográfica (gelatina fotográfica), podrá importarse a condición de que:
a) proceda de una de las plantas de origen que figuran en el cuadro 3;
b) haya sido producida de acuerdo con el punto 6;
c) se importe a través de uno de los puestos de inspección fronterizos de primera entrada en la Unión que figuran en el cuadro 3, y
d) esté destinada a la fabricación en una fábrica fotográfica autorizada que figura en el cuadro 3.
Cuadro 3
Importación de gelatina fotográfica
|
Tercer país de origen |
Fábricas de origen |
Estado miembro de destino |
Puesto de inspección fronterizo de primera entrada en la Unión |
Fábricas fotográficas autorizadas |
|||||||||||||||||
|
Japón |
|
Países Bajos |
Rotterdam |
|
|||||||||||||||||
|
Reino Unido |
Liverpool Felixstowe Heathrow |
|
||||||||||||||||||
|
República Checa |
Hamburgo |
|
|||||||||||||||||||
|
Estados Unidos |
|
Reino Unido |
Liverpool Felixstowe Heathrow |
|
|||||||||||||||||
|
República Checa |
Hamburgo |
|
2. Una vez que la gelatina fotográfica haya entrado en el Estado miembro de destino, no se comercializará entre Estados miembros, sino que se utilizará exclusivamente en la fábrica fotográfica autorizada en el mismo Estado miembro de destino y solamente a efectos de producción fotográfica.
3. Tras los controles veterinarios previstos en la Directiva 97/78/CE, la gelatina fotográfica deberá transportarse directamente a la fábrica fotográfica autorizada de destino, de conformidad con las condiciones establecidas en el apartado 4 del artículo 8 de dicha Directiva.
4. El transporte mencionado en el punto 3 podrá realizarse en vehículos o contenedores en los que la gelatina fotográfica se halle separada físicamente de cualquier otro producto destinado a la alimentación de personas o animales.
5. El explotador de la fábrica fotográfica autorizada velará por que cualquier excedente o residuo y otros desechos derivados de la gelatina fotográfica:
a) se transporten en contenedores estancos precintados, con el rótulo "solo para eliminación", en vehículos que satisfagan las condiciones de higiene adecuadas;
b) se eliminen de conformidad con el artículo 12, letra a), inciso i), del Reglamento (CE) nº 1069/2009 o se exporten al tercer país de origen de conformidad con el Reglamento (CE) nº 1013/2006.
6. La gelatina fotográfica se elaborará conforme a los siguientes requisitos:
a) La gelatina fotográfica se producirá solamente en plantas de transformación que no produzcan gelatina para la alimentación humana o animal destinada a la expedición a la Unión Europea, y que hayan sido autorizadas para ello por las autoridades competentes del tercer país en cuestión.
b) La gelatina fotográfica se producirá mediante un procedimiento que garantice que la materia prima se trata a través del método de transformación 1 (esterilización por presión) expuesto en el capítulo III del anexo IV o se somete a un tratamiento con ácidos o bases durante al menos dos días, un lavado con agua y
i) después de un tratamiento con ácidos, un tratamiento con una solución alcalina durante al menos veinte días, o
ii) después de un tratamiento con bases, un tratamiento con una solución ácida durante diez a doce horas.
El pH debe entonces ajustarse y el material purificarse mediante filtración y esterilización a 138 a 140 °C durante cuatro segundos.
c) Una vez concluido el procedimiento indicado en la letra b), la gelatina fotográfica podrá someterse al proceso de desecado y, según corresponda, al de pulverización o laminación.
d) La gelatina fotográfica deberá envasarse y embalarse en nuevos embalajes, almacenarse y transportarse en contenedores estancos precintados y rotulados en vehículos que satisfagan las condiciones de higiene adecuadas.
Si se observara la existencia de fugas, el vehículo y los contenedores se limpiarán completamente e inspeccionarán antes de volver a utilizarse.
e) En los envases y embalajes que contienen gelatina fotográfica debe figurar la advertencia "gelatina fotográfica destinada exclusivamente a la industria fotográfica".
Los cuernos y productos a base de cuerno, salvo la harina de cuerno, y a las pezuñas y productos a base de pezuña, salvo la harina de pezuña, destinados a la producción de abonos o enmiendas del suelo de origen orgánico, podrán importarse a condición de que:
1. hayan sido elaborados con arreglo a lo dispuesto en el capítulo XII del Anexo XIII, y
2. el material se transporte directamente al establecimiento o planta autorizados o registrados una vez realizados los controles veterinarios previstos en la Directiva 97/78/CE y, de conformidad con las condiciones establecidas en el apartado 4 del artículo 8 de esa misma Directiva.
Salvo cuando se conserven por motivos de referencia o se reexpidan al tercer país de origen, las muestras para diagnóstico e investigación y cualquier producto derivado del uso de dichas muestras se eliminarán:
a) como residuo mediante incineración;
b) por esterilización a presión y posterior eliminación o uso de conformidad con lo dispuesto en los artículos 12 a 14, del Reglamento (CE) nº 1069/2009, o
c) de conformidad con el punto 4, letra b) de la sección 1 del capítulo I del anexo VI en caso de;
i) cantidades que no superen los 2000 ml, y
ii) que las muestras o productos derivados hayan sido elaborados y enviados desde terceros países o partes de terceros países que figuran en la parte 1 del anexo II del Reglamento (UE) nº 206/2010 y desde los cuales los Estados miembros autorizan la importación de carne fresca de animales bovinos domésticos.
1. La autoridad competente podrá autorizar la importación y el tránsito de muestras comerciales siempre que:
a) procedan:
i) de terceros países que figuren en la columna "lista de terceros países" de la fila no 14 del cuadro 2 de la sección 1 del capítulo II del presente anexo;
ii) en el caso de muestras comerciales consistentes en leche, productos lácteos o productos derivados de la leche, de los terceros países autorizados que figuren en el anexo I del Reglamento (UE) nº 605/2010;
b) vayan acompañadas del certificado sanitario establecido en el capítulo 8 del Anexo XV, y
c) tras los controles veterinarios previstos en la Directiva 97/78/CE y, de conformidad con las condiciones establecidas en el apartado 4 del artículo 8 de esa misma Directiva, se transporten directamente al establecimiento o planta autorizados o registrados que constan en la autorización expedida por la autoridad competente.
2. Salvo cuando las muestras comerciales se conservan con fines de referencia, serán:
a) eliminadas o empleadas de conformidad con lo establecido en los artículos 12, 13 y 14 del Reglamento (CE) nº 1069/2009, o
b) devueltas al tercer país de origen;
3. Si las muestras comerciales se emplean para pruebas de maquinaria, éstas se llevarán a cabo:
a) con equipo de uso exclusivo, o
b) con equipo que sea limpiado y desinfectado antes de su uso para propósitos distintos de las pruebas.
Las muestras comerciales deberán transportarse en contenedores estancos hasta la planta o establecimiento autorizado o registrado.
1. La importación y tránsito de los artículos de exposición deberán cumplir las siguientes condiciones:
a) proceden de terceros países que figuren en la columna "lista de terceros países" de la fila no 14 del cuadro 2 de la sección 1 del capítulo II;
b) la introducción ha sido autorizada previamente por la autoridad competente del Estado miembro donde se prevé utilizar el objeto de exposición;
c) tras los controles veterinarios previstos en la Directiva 97/78/CE, los artículos de exposición deberán enviarse directamente al usuario autorizado.
2. Cada lote deberá envasarse en envases que no tengan pérdidas y deberán ir acompañados por un documento comercial que especifique:
a) la descripción del material y la especie animal de origen;
b) la categoría del material;
c) la cantidad de material;
d) el lugar de carga del material;
e) el nombre y la dirección del expedidor;
f) el nombre y la dirección del destinatario, y
g) la información que permita la identificar la autorización expedida por la autoridad competente de destino.
3. Tras la exposición o una vez finalizada la actividad artística, los artículos de exposición deberán:
a) devolverse al tercer país de origen;
b) enviadas a otro Estado miembro o tercer país, siempre que el envío sea previamente autorizado por la autoridad competente del Estado miembro o tercer país de destino, o
c) eliminarse o emplearse de conformidad con lo establecido en los artículos 12, 13 y 14 del Reglamento (CE) nº 1069/2009.
Los materiales contemplados en el artículo 26 serán importados en las siguientes condiciones:
1. Los materiales serán importados con una etiqueta en el envase, contenedor o vehículo que indique "prohibido en alimentos, piensos, fertilizantes, cosméticos, medicamentos o productos sanitarios".
2. Los materiales se entregarán directamente a un establecimiento o planta autorizados o registrados para la fabricación de productos derivados distintos de los contemplados en el punto 1.
3. Los materiales no utilizados o sobrantes se utilizarán o eliminarán de conformidad con el artículo 12 del Reglamento (CE) nº 1069/2009.
1. La autoridad competente podrá autorizar la importación de los siguientes materiales con fines distintos de la alimentación de animales de granja terrestres, salvo piensos para animales de peletería, a condición de que no existan riesgos inaceptables de propagación de enfermedades transmisibles a personas o animales:
a) los subproductos de animales acuáticos y los productos derivados de animales acuáticos;
b) los animales invertebrados acuáticos y los productos derivados de los mismos;
c) los animales invertebrados terrestres, incluida cualquiera de sus formas de transformación, como larvas, y los productos derivados de los mismos;
d) los productos generados por los animales mencionados en las letras a), b) y c), como las huevas de pescado;
e) los materiales de la categoría 3 compuestos por animales y sus partes de los órdenes zoológicos de los roedores y los lagomorfos.
2. La importación de lotes de los materiales contemplados en el punto 1 se efectuará de conformidad con los requisitos de certificación sanitaria dispuestos en la legislación nacional.
Los modelos de certificados sanitarios del presente anexo se aplicarán a la importación desde terceros países y al tránsito a través de la Unión Europea de los subproductos animales y productos derivados indicados en el modelo de certificado sanitario correspondiente.
Notas
a) El país exportador deberá elaborar los certificados sanitarios basándose en los modelos dispuestos en el presente anexo, según el modelo correspondiente a los subproductos animales o productos derivados en cuestión. Los certificados deberán incluir, siguiendo el orden numérico del modelo, las declaraciones exigidas a todo tercer país y, según el caso, las garantías adicionales exigidas al tercer país exportador o a parte del mismo.
b) En los casos en que el modelo de certificado indique que se conserve determinada declaración, el funcionario responsable de la certificación podrá tachar, con su rúbrica y sello, las declaraciones que no sean pertinentes, que también se podrán eliminar por completo del certificado.
c) El original de cada certificado constará de una sola página por ambos lados o, si se necesita más de una página, estará configurado de manera que todas las páginas formen un todo integrado e indivisible.
d) Estará redactado en al menos una de las lenguas oficiales del Estado miembro de la UE en el que se lleve a cabo la inspección en el puesto fronterizo y del Estado miembro de destino. No obstante, estos Estados miembros podrán autorizar el uso de certificados redactados en otras lenguas, acompañados, en su caso, de una traducción oficial.
e) Si, por razones de identificación de los componentes del envío, se adjuntan páginas adicionales al certificado, éstas se considerarán parte integrante del original mediante la aplicación de la firma y del sello del veterinario oficial expedidor del certificado en cada una de las páginas.
f) Cuando el certificado, incluidos los añadidos contemplados en la nota e), comprenda más de una página, cada una de ellas deberá ir numerada –(número de página) de (número total de páginas)– en su parte inferior y llevará en su parte superior el número de código del certificado que le haya atribuido la autoridad competente.
g) El original del certificado deberá estar cumplimentado y firmado por un veterinario oficial. De esta forma, las autoridades competentes del país exportador garantizarán el cumplimiento de los principios de certificación equivalentes a los establecidos en la Directiva 96/93/CE.
h) El color de la firma deberá ser diferente del color del texto impreso. La misma norma se aplicará a los sellos distintos de los troquelados o de filigrana.
i) El original del certificado deberá acompañar al envío hasta el puesto de inspección fronterizo de la Unión.
j) Si los certificados sanitarios se utilizan para envíos en tránsito, deberá cumplimentarse la casilla I.5 ("Consignatario") del certificado sanitario correspondiente con el nombre y la dirección del puesto de inspección fronterizo por el que está previsto que el envío salga de la Unión Europea.
de proteínas animales transformadas no destinadas al consumo humano, incluidas las mezclas y los productos distintos de los alimentos para animales de compañía que las contengan, que se enviarán a la Unión Europea o transitarán por ella (2)




de leche, productos lácteos y productos derivados de la leche no destinados al consumo humano que se enviarán a la Unión Europea o transitarán por ella (2)




de calostro y productos a base de calostro producidos a partir de animales bovinos no destinados al consumo humano que se enviarán a la Unión Europea o transitarán por ella (2)




de alimentos en conserva para animales de compañía, que se enviarán a la Unión Europea o transitarán por ella (2)




de alimentos transformados para animales de compañía, distintos de los alimentos en conserva, que se enviarán a la Unión Europea o transitarán por ella (2)






de accesorios masticables para perros, que se enviarán a la Unión Europea o transitarán por ella (2)




de alimentos crudos para animales de compañía destinados a la venta directa o subproductos animales para la alimentación de animales de peletería, que se enviarán a la Unión Europea o transitarán por ella (2)




de subproductos aromatizantes, para su uso en la fabricación de alimentos de animales de compañía, que se enviarán a la Unión Europea o transitarán por ella (2)





de subproductos animales (3) para la fabricación de alimentos de animales de compañía, que se enviarán a la Unión Europea o transitarán por ella (2)






para la importación de sangre y hemoderivados de équidos para uso externos a la cadena alimentaria animal, que se enviarán a la Unión Europea o transitarán por ella (2)




de hemoderivados no destinados al consumo humano, que podrían utilizarse como ingredientes para piensos, que se enviarán a la Unión Europea o transitarán por ella (2)



de hemoderivados sin tratar, exceptuando los de équidos, para la fabricación de productos derivados destinados a usos externos a la cadena alimentaria de animales de granja, que se enviarán a la Unión Europea o transitarán por ella (2)




de hemoderivados tratados, exceptuando los de équidos, para la fabricación de productos derivados destinados a usos externos a la cadena alimentaria de animales de granja, que se enviarán a la Unión Europea o transitarán por ella (2)




de pieles frescas o refrigeradas de ungulados, que se enviarán a la Comunidad Europea o transitarán por ella (2)
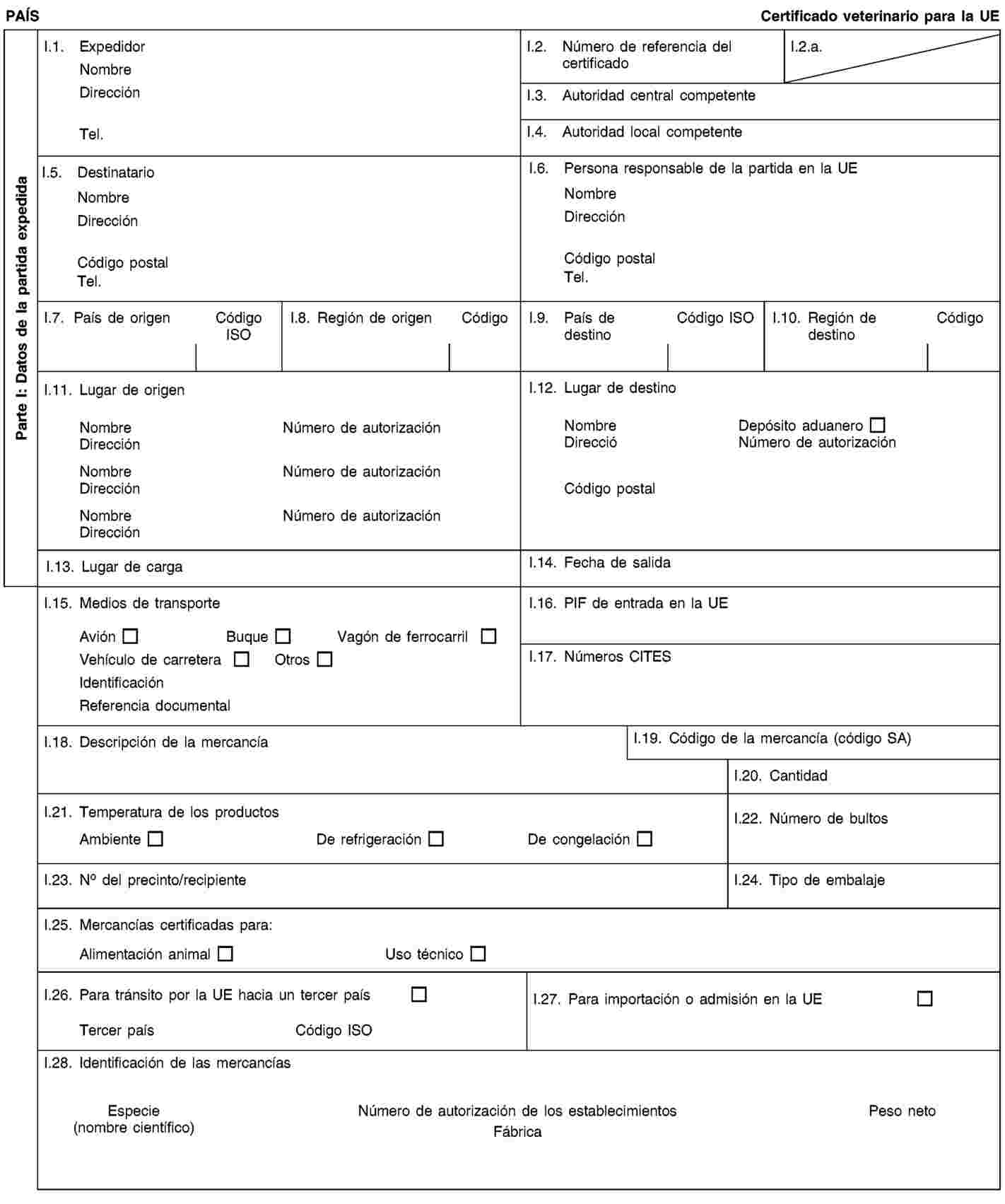


de pieles tratadas de ungulados que se enviarán a la Unión Europea o transitarán por ella (2)



de pieles tratadas de rumiantes y de équidos que se enviarán a la Unión Europea o transitarán por ella (1) y que se han mantenido separadas durante veintiún días o se transportarán ininterrumpidamente durante veintiún días antes de la importación
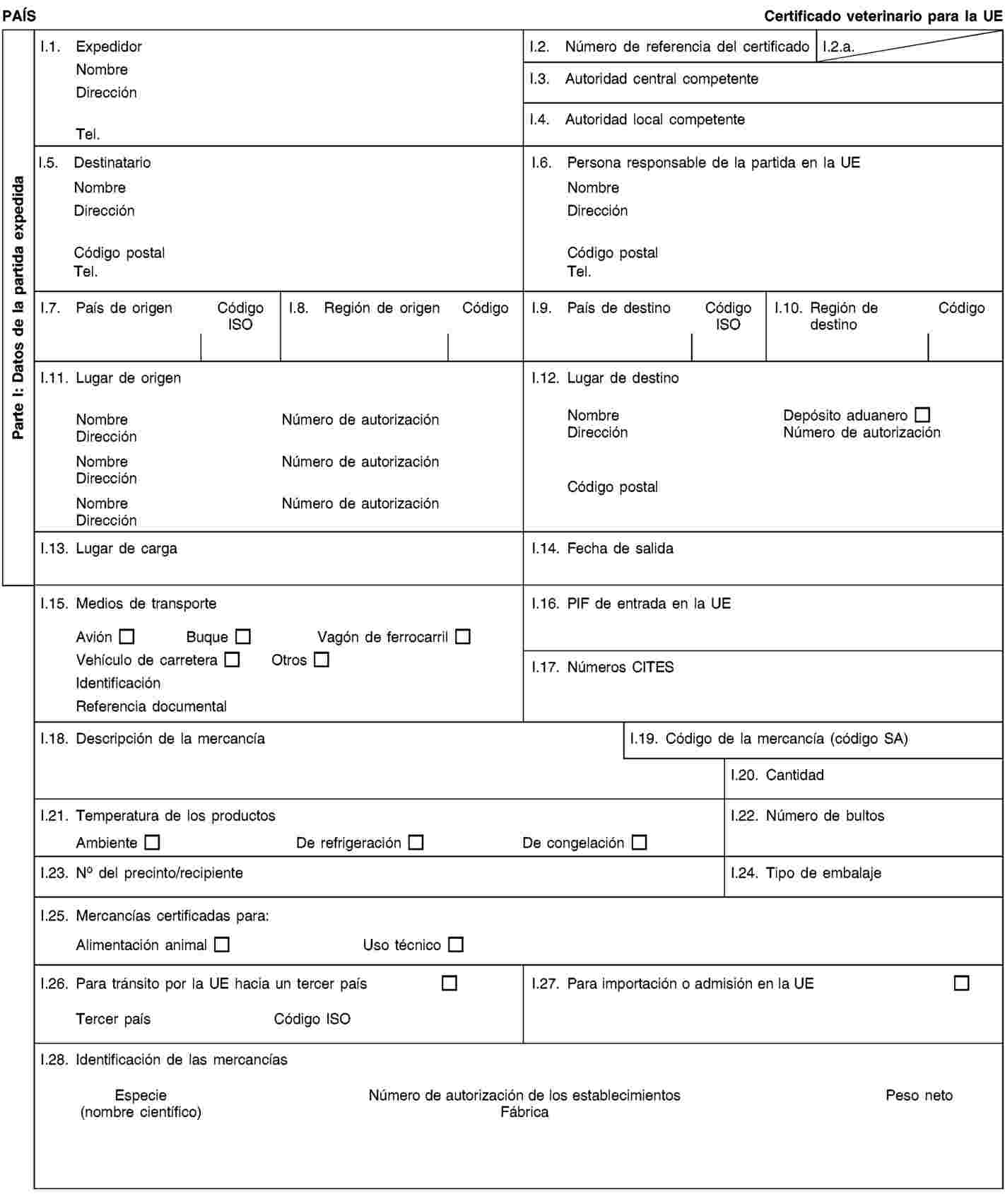


de trofeos de caza tratados y otros preparados de aves y ungulados, consistentes únicamente en huesos, cuernos, pezuñas, garras, astas, dientes o pieles, que se enviarán a la Comunidad Europea o transitarán por ella (2)



de trofeos de caza u otros preparados de aves y ungulados, consistentes en partes enteras no tratadas, que se enviarán a la Unión Europea o transitarán por ella (2)



de cerdas, procedentes de terceros países o regiones de terceros países indemnes de peste porcina africana, que se enviarán a la Unión Europea o transitarán por ella (2)
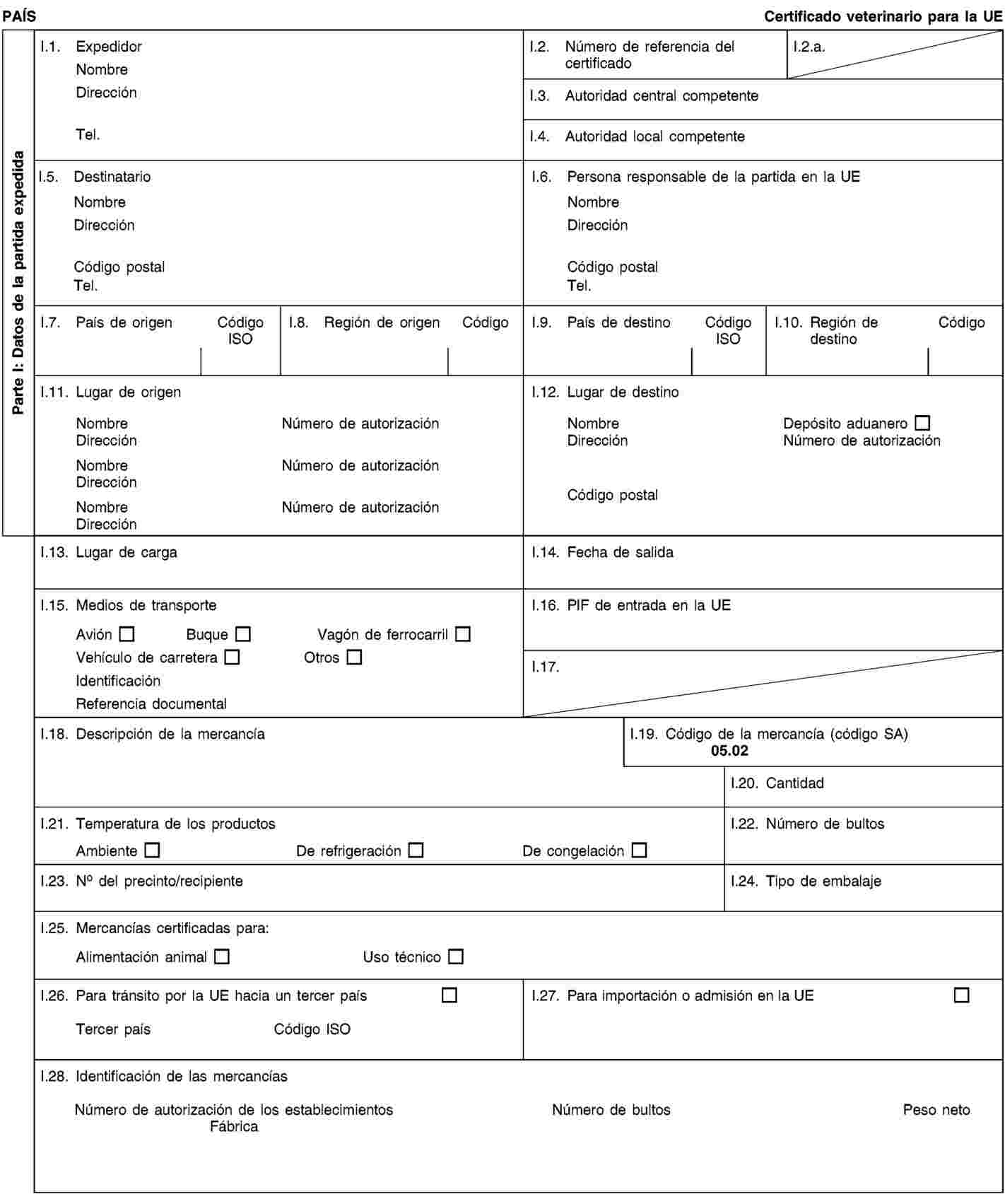

de cerdas, procedentes de terceros países o regiones de terceros países no indemnes de peste porcina africana, que se enviarán a la Unión Europea o transitarán por ella (2)
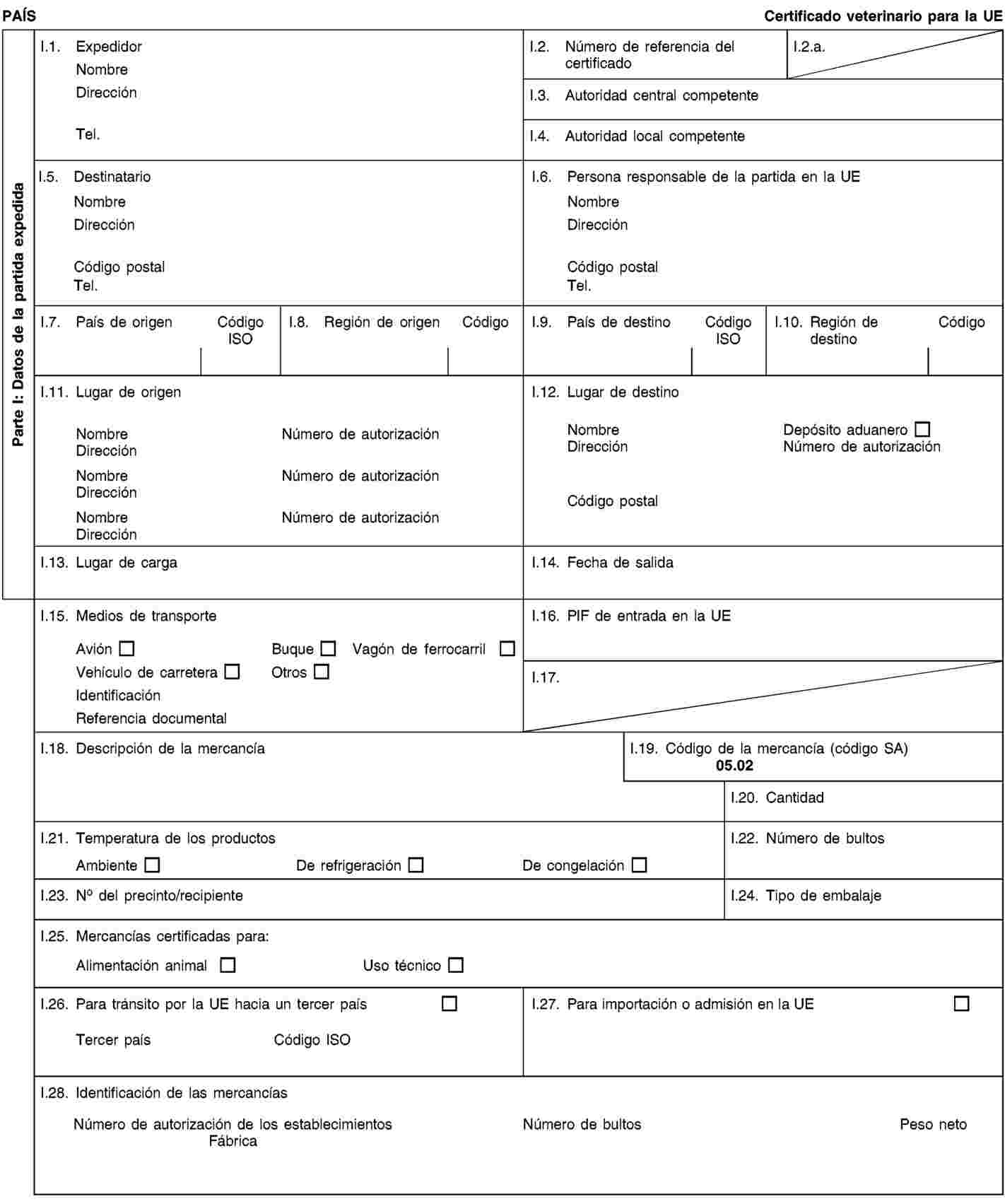


de subproductos animales para usos externos a la cadena alimentaria animal, o para muestras comerciales (2), que se enviarán a la Comunidad Europea o transitarán por ella (2)






de aceite de pescado no destinado al consumo humano, para uso como ingrediente para piensos o para usos externos a la cadena alimentaria animal, que se enviará a la Unión Europea o transitará por ella (2)



de grasas extraídas no aptas para el consumo humano, que podrían utilizarse como ingredientes para piensos, que se enviarán a la Unión Europea o transitarán por ella (2)





de grasas extraídas no destinadas al consumo humano, para determinados usos externos a la cadena alimentaria animal, que se enviarán a la Unión Europea o transitará por ella (2)
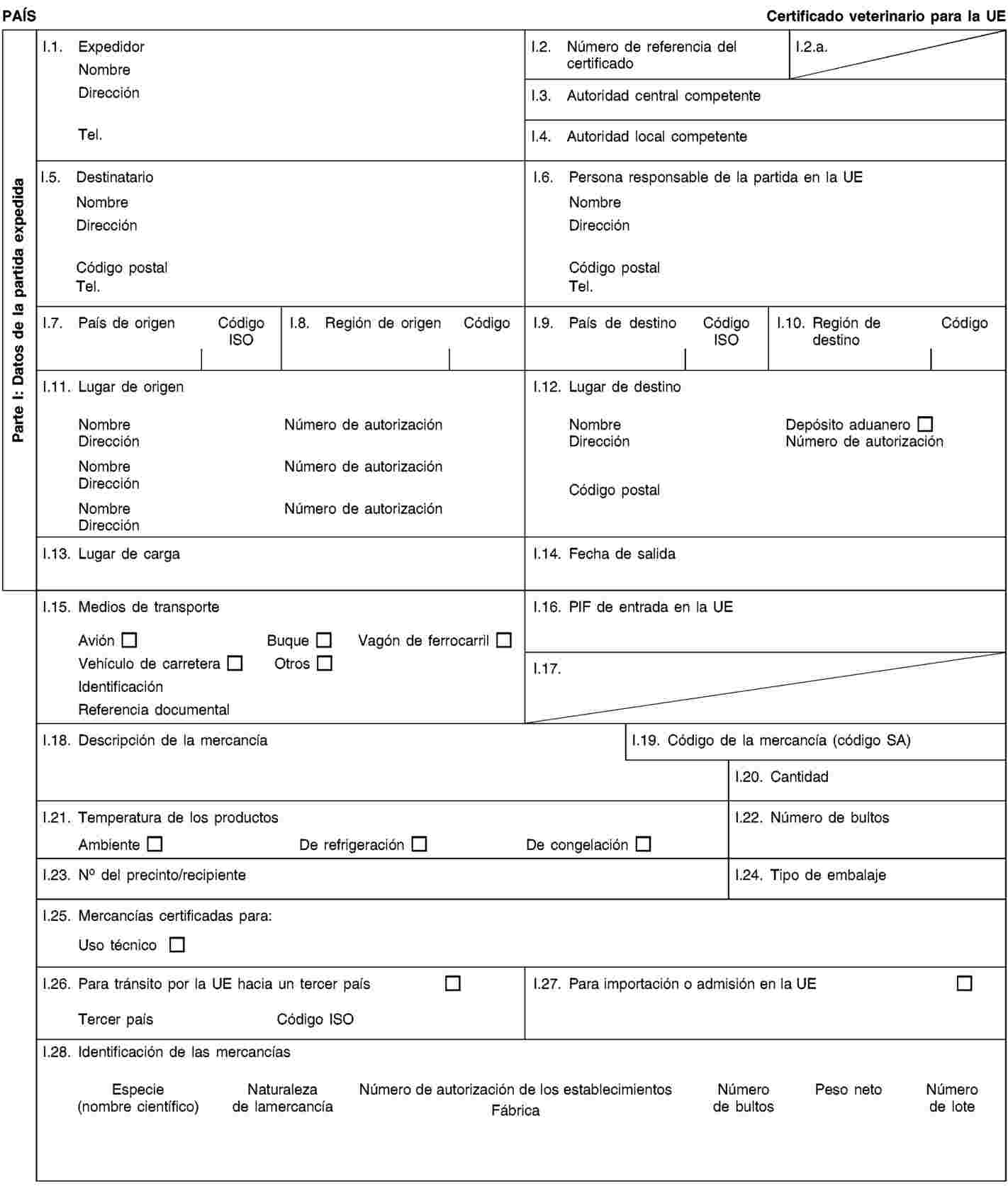



de gelatina y colágeno no destinados al consumo humano, para uso como ingrediente para piensos o para usos externos a la cadena alimentaria animal, que se enviarán a la Unión Europea o transitarán por ella (2)




de proteína hidrolizada, fosfato dicálcico y fosfato tricálcico no destinados al consumo humano, para uso como ingrediente para piensos o para usos externos a la cadena alimentaria animal, que se enviarán a la Unión Europea o transitarán por ella (2)





de subproductos de la apicultura destinados exclusivamente a usarse en apicultura, que se enviarán a la Unión Europea o transitarán por ella (2)


de derivados de grasas no destinados al consumo humano, para usos externos a la cadena alimentaria animal, que se enviarán a la Unión Europea o transitará por ella (2)




de derivados de grasas no destinados al consumo humano, para uso como ingredientes para piensos o para usos externos a la cadena alimentaria animal, que se enviarán a la Unión Europea o transitará por ella (2)



de ovoproductos no destinados al consumo humano, que podrían utilizarse como ingredientes para piensos, que se enviarán a la Unión Europea o transitarán por ella (2)




de estiércol transformado, productos a base de estiércol transformado y guano de murciélago, que se enviarán a la Unión Europea o transitarán por ella (2)
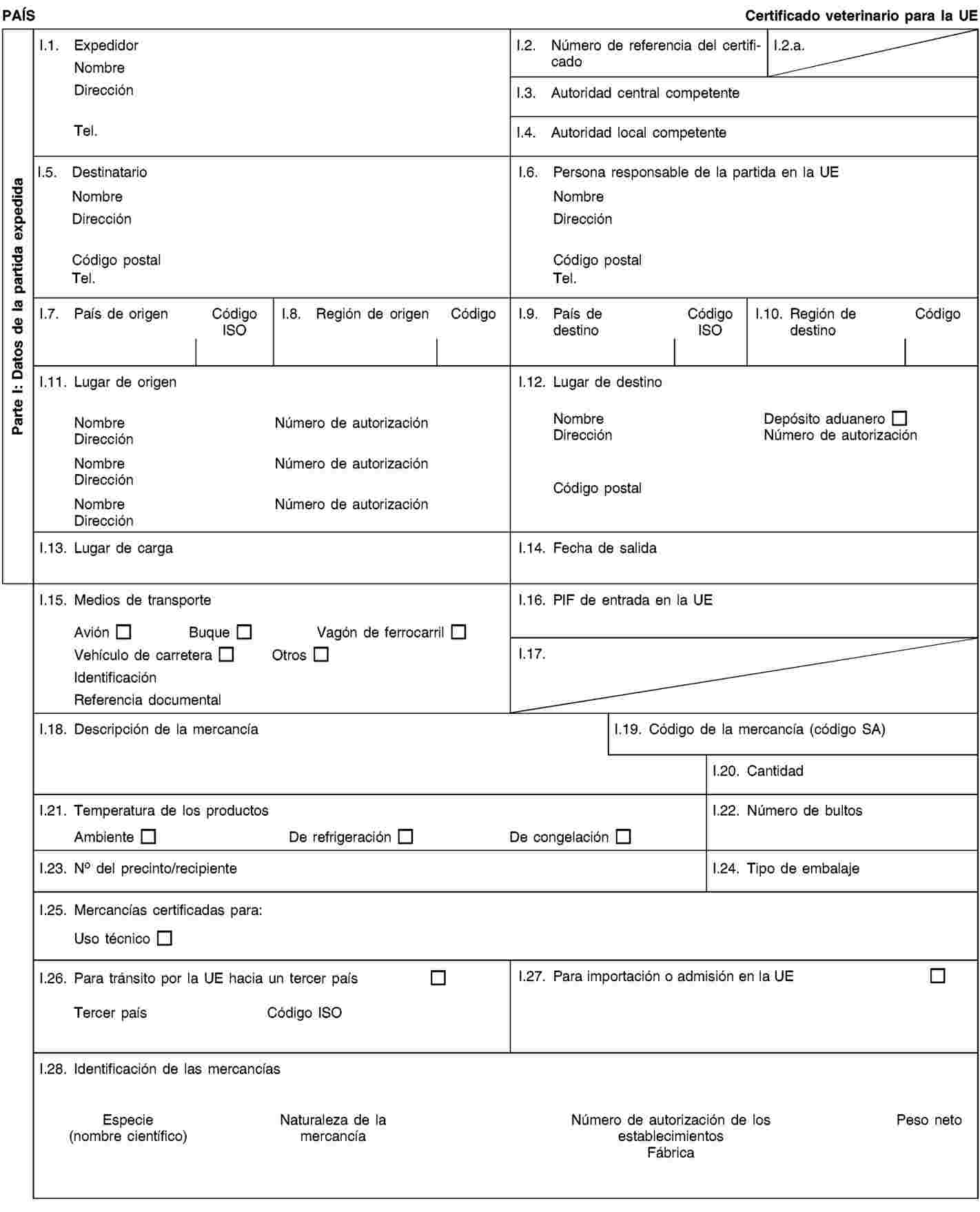


de cuernos y productos a base de cuerno, salvo la harina de cuerno, y pezuñas y productos a base de pezuña, salvo la harina de pezuña, destinados a la producción de abonos o enmiendas del suelo de origen orgánico, que se enviarán a la Unión Europea o transitarán por ella (2)



de gelatina no destinada al consumo humano para ser utilizada en la industria fotográfica, y destinada a la expedición a la Unión Europea
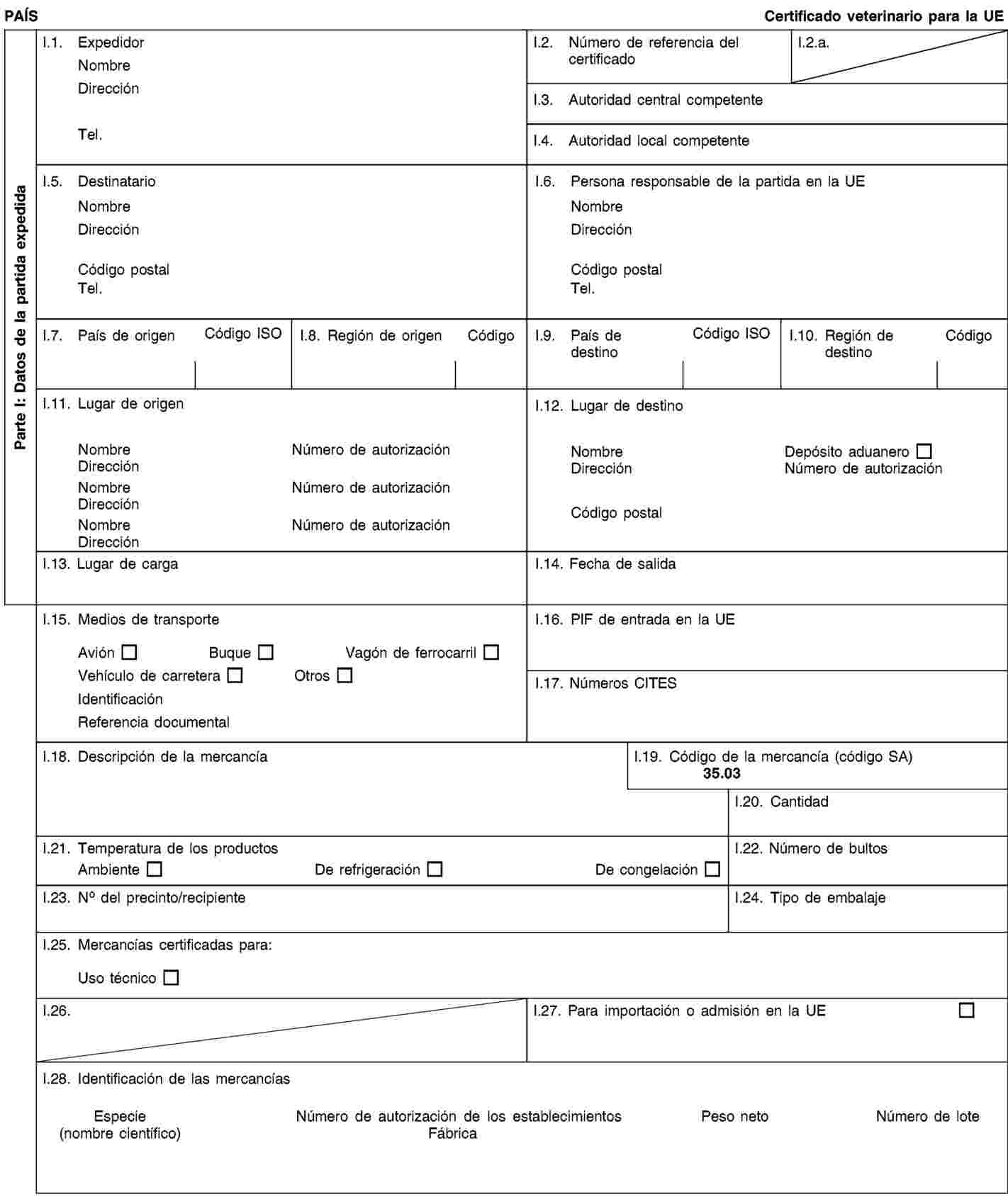


para la importación desde terceros países y el tránsito por la Unión Europea de productos intermedios para uso en la fabricación de medicamentos, medicamentos veterinarios, productos sanitarios, productos para el diagnóstico in vitro y reactivos de laboratorio




1. Las plantas de transformación serán supervisadas por la autoridad competente, la cual deberá cerciorarse del cumplimiento de las disposiciones del Reglamento (CE) nº 1069/2009 y del presente Reglamento.
En particular:
a) controlará:
i) las condiciones generales de higiene aplicables a los locales, el equipo y el personal;
ii) la eficacia de los controles propios de la planta, efectuados por el explotador de la planta de transformación de conformidad con el artículo 28 del Reglamento (CE) nº 1069/2009; dichos controles incluirán un examen de los resultados y, si fuere necesario, la toma de muestras;
iii) la aplicación eficaz del procedimiento escrito permanente basado en los principios APPCC de conformidad con lo dispuesto en el artículo 29, apartado 1, del Reglamento (CE) nº 1069/2009; dichos controles incluirán un examen de los resultados de tal aplicación y, si fuere necesario, la toma de muestras;
iv) las normas a las que responden los productos después de su tratamiento; los análisis y las pruebas deberán efectuarse con arreglo a métodos científicamente reconocidos, especialmente los establecidos en la legislación de la Unión o, de no existir disposiciones legislativas relativas a tales métodos, en normas internacionalmente reconocidas o, en su defecto, en normas nacionales, y
v) las condiciones de almacenamiento;
b) tomará las muestras necesarias para los exámenes de laboratorio, y
c) procederá a cualquier otro control que estime necesario para el cumplimiento del Reglamento (CE) nº 1069/2009 y del presente Reglamento.
2. La autoridad competente deberá poder acceder en cualquier momento a todas las partes de la planta de transformación y a sus registros, documentos comerciales y certificados sanitarios, con el fin de poder desempeñar las responsabilidades que le asigna el apartado 1.
1. Previamente a la concesión de autorización a una planta de transformación, según se dispone en el artículo 44, apartado 1, del Reglamento (CE) nº 1069/2009, la autoridad competente deberá verificar que el explotador ha realizado la validación de la planta de transformación con arreglo a los siguientes procedimientos e indicadores:
a) descripción del proceso (mediante un diagrama del flujo del procedimiento);
b) identificación de los puntos de control crítico, incluida la velocidad de transformación del material en caso del sistema continuo;
c) cumplimiento de los requisitos de transformación específicos establecidos en el presente Reglamento, y
d) cumplimiento de los requisitos siguientes:
i) dimensión de las partículas en los procesos de presión discontinua y continua: la dimensión de las partículas se determinará por la dimensión del orificio de la picadora o de los intersticios;
ii) temperatura, presión, tiempo de transformación y, en el caso de sistemas de transformación continua, la tasa de transformación del material, conforme a lo especificado en los apartados 2 y 3.
2. En caso de sistema de presión discontinua:
a) la temperatura debe controlarse con un termopar permanente y registrarse en tiempo real;
b) la fase de presión debe controlarse con un manómetro permanente y registrarse en tiempo real;
c) el tiempo de transformación debe indicarse mediante diagramas tiempo/temperatura y tiempo/presión.
Al menos una vez al año deberán calibrarse el termopar y el manómetro.
3. En caso de sistema de presión continua:
a) la temperatura y la presión deberán controlarse con termopares, o con una pistola de infrarrojos, y manómetros utilizados en posiciones precisas durante todo el sistema de transformación de tal manera que la temperatura y la presión cumplan las condiciones establecidas en el conjunto del sistema continuo o en una parte del mismo; la temperatura y la presión deben registrarse en tiempo real;
b) la medición del tiempo mínimo de tránsito en la parte completa relevante del sistema continuo en la que la temperatura y la presión cumplen las condiciones establecidas deberá facilitarse a las autoridades competentes, mediante el uso de marcadores insolubles, como por ejemplo, dióxido de manganeso, o de un método que ofrezca garantías equivalentes.
La medición y el control precisos de la velocidad de transformación es esencial, y se deberá efectuar durante la prueba de validación en función de un punto crítico de control que pueda controlarse continuamente, como:
i) número de revoluciones por minuto (rpm);
ii) potencia eléctrica (amperios con un determinado voltaje);
iii) porcentaje de evaporación o condensación, o
iv) número de golpes de bomba por unidad de tiempo.
Todo el equipo de medición y control deberá calibrarse al menos una vez al año.
4. Las autoridades competentes repetirán los procedimientos de validación cuando lo consideren necesario y, en cualquier caso, cada vez que el proceso experimente una alteración importante, como por ejemplo, el cambio de maquinaria o el cambio de materias primas.
1. Acceso a las listas de establecimientos, plantas y explotadores registrados y autorizados
Con el fin de ayudar a los Estados miembros en la tarea de poner a disposición de otros Estados miembros y de la población listas actualizadas de establecimientos, plantas y explotadores registrados y autorizados, la Comisión creará un sitio web que contendrá enlaces con los sitios web nacionales de cada Estado miembro, tal como se establece en el punto 2, letra a).
2. Formato de los sitios web nacionales
a) Cada Estado miembro proporcionará a la Comisión una dirección de enlace a un único sitio web nacional que contendrá la lista de referencia de todos los establecimientos, plantas y explotadores registrados y autorizados en su territorio ("lista de referencia").
b) Cada lista de referencia consistirá en una página y se presentará en una o varias lenguas oficiales de la UE.
3. El diseño de las listas de referencia, incluida la información relevante y códigos, respetará las especificaciones técnicas publicadas por la Comisión en su sitio web.
La autoridad competente realizará un control del funcionamiento del sistema de control y registro mencionado en el punto 2 del capítulo V del anexo VIII del presente Reglamento para verificar el cumplimiento de lo dispuesto en él y podrá, en su caso, solicitar el análisis de muestras adicionales con arreglo al método contemplado en el mismo punto.
La autoridad competente deberá realizar inspecciones de plantas incineradoras de baja capacidad antes de autorizar la incineración de materiales especificados de riesgo, y al menos una vez al año para controlar el cumplimiento de lo dispuesto en el Reglamento (CE) nº 1069/2009 y en el presente Reglamento.
En caso de eliminación de subproductos animales en zonas remotas de acuerdo con lo dispuesto en el artículo 19, apartado 1, letra b), del Reglamento (CE) nº 1069/2009, la autoridad competente deberá realizar un seguimiento periódico de las zonas consideradas remotas para asegurarse de que se realiza un control adecuado de esas zonas y de las operaciones de eliminación.
1. La autoridad competente adoptará las medidas necesarias para controlar:
a) la correcta composición, transformación y utilización de los piensos que contengan harina de carne y huesos u otros productos transformados de conformidad con los métodos de transformación dispuestos en el capítulo III del anexo IV derivados de cuerpos o partes de animales de la misma especie, y
b) que los animales son alimentados con los piensos a los que se hace referencia en la letra a), entre otras cosas, mediante:
i) una estrecha vigilancia de la calificación sanitaria de los animales, y
ii) una vigilancia adecuada de las EET que incluya muestreos y exámenes de laboratorio periódicos para la detección de EET.
2. Las muestras a las que se hace referencia en el apartado 1, letra b), inciso ii) incluirán muestras de animales que presenten síntomas neurológicos y de los animales reproductores más viejos.
1. La autoridad competente deberá:
a) incluir los centros de recogida en la lista elaborada de conformidad con lo dispuesto en el artículo 47, apartado 1, del Reglamento (CE) nº 1069/2009;
b) asignar un número oficial a cada centro de recogida, y
c) actualizar la lista de centros de recogida y hacerla pública junto con la lista elaborada de conformidad con lo dispuesto en el artículo 47, apartado 1, del Reglamento (CE) nº 1069/2009.
2. Las autoridades competentes llevarán a cabo controles oficiales en los centros de recogida con el fin de verificar el cumplimiento del presente Reglamento.
La autoridad competente vigilará la calificación sanitaria de los animales de granja de la región en la que la alimentación de aves necrófagas con materiales de la categoría 1 tiene lugar, y realizará una vigilancia adecuada de las EET que incluya muestreos y exámenes de laboratorio periódicos para la detección de EET.
En particular, se tomarán muestras de animales que presenten síntomas neurológicos y de los animales reproductores más viejos.
La autoridad competente realizará controles a lo largo de toda la cadena de producción y uso de abonos y enmiendas del suelo de origen orgánico conforme a las restricciones dispuestas en el capítulo II del anexo II.
Dichos controles incluirán la comprobación de la mezcla con un ingrediente conforme a lo dispuesto en el anexo XI, capítulo II, sección 1, punto 2, así como controles de existencias de tales productos almacenados en granjas y los registros mantenidos de conformidad con lo dispuesto en el Reglamento (CE) nº 1069/2009 y en el presente Reglamento.
La autoridad competente llevará a cabo controles documentales en fábricas fotográficas autorizadas indicadas en el anexo XIV, capítulo II, sección 11, punto 1, cuadro 3, en la cadena de transmisión, desde los puestos fronterizos de inspección de primera entrada hasta la fábrica fotográfica autorizada con el fin de cuadrar las cantidades de productos importados, utilizados y eliminados.
La autoridad competente llevará a cabo controles documentales en establecimientos o plantas registrados que reciban grasas extraídas importadas de conformidad con lo dispuesto en el anexo XIV, capítulo II, sección 9, en la cadena de transmisión, desde los puestos fronterizos de inspección de primera entrada hasta el establecimiento o planta registrados con el fin de cuadrar las cantidades de productos importados, utilizados y eliminados.
Los explotadores presentarán solicitudes para la autorización del envío de subproductos animales indicados en el artículo 48, apartado 1, del Reglamento (CE) nº 1069/2009 de conformidad con el siguiente modelo:


Agencia Estatal Boletín Oficial del Estado
Avda. de Manoteras, 54 - 28050 Madrid