Content not available in English
 Este texto consolidado es de carácter informativo y no tiene valor jurídico.
Este texto consolidado es de carácter informativo y no tiene valor jurídico.[Bloque 1: #pr]
Las Ordenes de 31 de enero de 1977 («Boletín Oficial del Estado» de 14 al 17 de julio); 31 de julio de 1979 («Boletín Oficial del Estado» de 29 y 30 de agosto); 17 de septiembre de 1981 («Boletín Oficial del Estado» de 14 de octubre); 1 de diciembre de 1981 («Boletín Oficial del Estado» de 20 de enero de 1982), y 26 de enero de 1989 («Boletín Oficial del Estado» de 4 de febrero), establecieron diversos métodos oficiales de análisis de leche y productos lácteos, siendo necesario complementarlos con otros nuevos que atiendan al control de las mezclas de leches citadas anteriormente.
Las normas relativas a los métodos oficiales de análisis de leche y productos lácteos deben tener en cuenta, principalmente, la protección de la salud humana, por lo que el presente Real Decreto se dicta al amparo del artículo 149.1.16. de la Constitución Española, y de acuerdo con lo dispuesto en el artículo 40.2 de la Ley 14/1986, de 25 de abril, General de Sanidad.
En su virtud, a propuesta de los Ministros de Sanidad y Consumo; de Agricultura, Pesca y Alimentación; de Industria y Energía, y de Comercio y Turismo, oídos los sectores afectados, previo informe de la Comisión interministerial para la Ordenación Alimentaria, de acuerdo con el Consejo de Estado y previa deliberación del Consejo de Ministros en su reunión del día 19 de noviembre de 1993,
DISPONGO:
[Bloque 2: #au]
Se aprueba como oficial el Método de Análisis de Leche y Productos Lácteos que se determina en el anexo del presente Real Decreto.
[Bloque 3: #da]
Lo dispuesto en el presente Real Decreto y el Método Oficial de Análisis que aprueba se dictan al amparo de lo establecido en el artículo 149.1.16. de la Constitución Española y en virtud de lo dispuesto en el artículo 40.2 de la Ley 14/1986, de 25 de abril, General de Sanidad.
[Bloque 4: #dd]
Quedan derogadas las disposiciones de igual o inferior rango que se opongan a lo establecido en el presente Real Decreto.
[Bloque 5: #fi]
Dado en Madrid a 19 de noviembre de 1993.
JUAN CARLOS R.
El Ministro de la Presidencia,
ALFREDO PEREZ RUBALCABA
[Bloque 6: #an]
[Bloque 7: #A1]
El método permite poner de manifiesto la presencia de suero de quesería mediante la determinación de glicomacropéptidos por CLAE, previa eliminación de grasas y proteínas con ácido tricloroacético.
El método es aplicable a leches líquidas UHT y esterilizadas en el plazo de siete días a partir de la fecha de envasado y a leches pasteurizadas y en polvo dentro del plazo de vida comercial del producto establecido de acuerdo con las disposiciones vigentes en la materia.
[Bloque 8: #A2]
1. Material de uso corriente en laboratorio.
2. Equipo de cromatografía líquida de alta eficacia, que comprenda:
a) Dos columnas en serie de permeación de gel TSK 2000 SW (30 cm de longitud, diámetro interior de 0,75 cm) o de eficacia equivalente. Alternativamente puede utilizarse una de estas columnas con precolumna previa (3 cm × 0,3 cm) rellena de I 125 o material de eficacia equivalente.
b) Horno de columna con termostato regulado a 35 ºC. ± 1 ºC. Se puede trabajar con columnas, mantenidas a temperatura ambiente, pero su poder de resolución es ligeramente menor. En este caso, las variaciones de temperatura durante una misma serie de análisis deberán ser inferiores a ± 5 C.
c) Detector ultravioleta que permita efectuar lecturas a 205 nm.
d) Integrador que pueda integrar de valle a valle.
[Bloque 9: #A3]
1. Solución de ácido tricloroacético.
Disolver 240 g de ácido tricloroacético en agua destilada hasta 1.000 ml.
2. Solución eluyente pH 6,0.
Disolver 1,74 g de fosfato dipotásico, 12,37 g de fosfato monopotásico y 21,41 g de sulfato de sodio en 700 ml de agua aproximadamente.
Ajustar, si es necesario, a pH 6,0 con ayuda de una solución de ácido fosfórico o de hidróxido potásico. Completar hasta 1.000 ml con agua y homogeneizar.
En caso de utilizar una columna diferente a la TSK 2000 SW emplear una solución eluyente adecuada.
Esta solución se debe filtrar antes de su utilización a través de una membrana filtrante de 0,45 µm de diámetro de poro.
3. Solución de lavado y de conservación de columnas.
Mezclar un volumen de acetonitrilo en nueve volúmenes de agua.
Filtrar la mezcla, antes de su utilización, a través de una membrana filtrante de 0,45 µm de diámetro de poro.
Puede utilizarse cualquier otra solución de lavado que tenga efecto bactericida y que no altere la eficacia de resolución de las columnas.
4. Muestras patrón.
a) Leche desnatada en polvo que responda a las exigencias del Reglamento CEE número 625/78, exenta de suero de quesería.
b) La misma leche anterior adicionada con un 5 por 100 m/m de suero de quesería de composición media.
[Bloque 10: #A4]
1. Preparación de la muestra.
a) Leche en polvo.
Trasvasar la leche en polvo a un recipiente de capacidad aproximadamente doble del volumen de ésta, provisto de cierre hermético. Cerrar el recipiente inmediatamente y mezclar bien.
Pesar 2,000 g ± 0,001 g y añadir 20,0 g de agua a 50 ºC. Disolver agitando durante cinco minutos con ayuda de un agitador. Llevar a temperatura de 25 ºC. Añadir en dos minutos 10,0 ml de la solución de ácido tricloroacético (3.1) bajo agitación magnética.
Mantener a 25 ºC durante sesenta minutos. Centrifugar a 2.200 ges durante diez minutos o filtrar sobre papel desechando los cinco primeros ml de filtrado.
b) Leche líquida.
Tomar 20 ml de leche y continuar el proceso de igual forma a la que figura a partir del segundo punto y seguido del párrafo segundo del apartado a).
c) Patrones.
Aplicar exactamente a la leche en polvo (3.4.a) y a la leche en polvo adicionada con el 5 por 100 de suero de quesería (3.4.b) el procedimiento descrito en el apartado 4.1.a.
2. Análisis cromatográfico.
a) Inyectar de 15 a 30 µl medidos exactamente de sobrenadante o de filtrado obtenido según el apartado 4.1 en el aparato de cromatografía líquida de alta eficacia con un flujo de 1,0 ml/min de la solución eluyente (3.2).
En cada interrupción lavar las columnas con agua y en toda interrupción superior a veinticuatro horas, después del lavado con agua, se les debe pasar solución de lavado (3.3) por lo menos tres horas a un flujo de 0,2 ml por minuto o seguir las instrucciones del fabricante.
b) Antes de proceder al análisis cromatográfico de las muestras, inyectar el patrón de leche en polvo adicionada con el 5 por 100 de suero de quesería (3.4.b) preparado según el apartado 4.1.c) las veces que sean necesarias hasta que la superficie y el tiempo de retención del pico correspondiente a los GMP sea constante.
[Bloque 11: #A5]
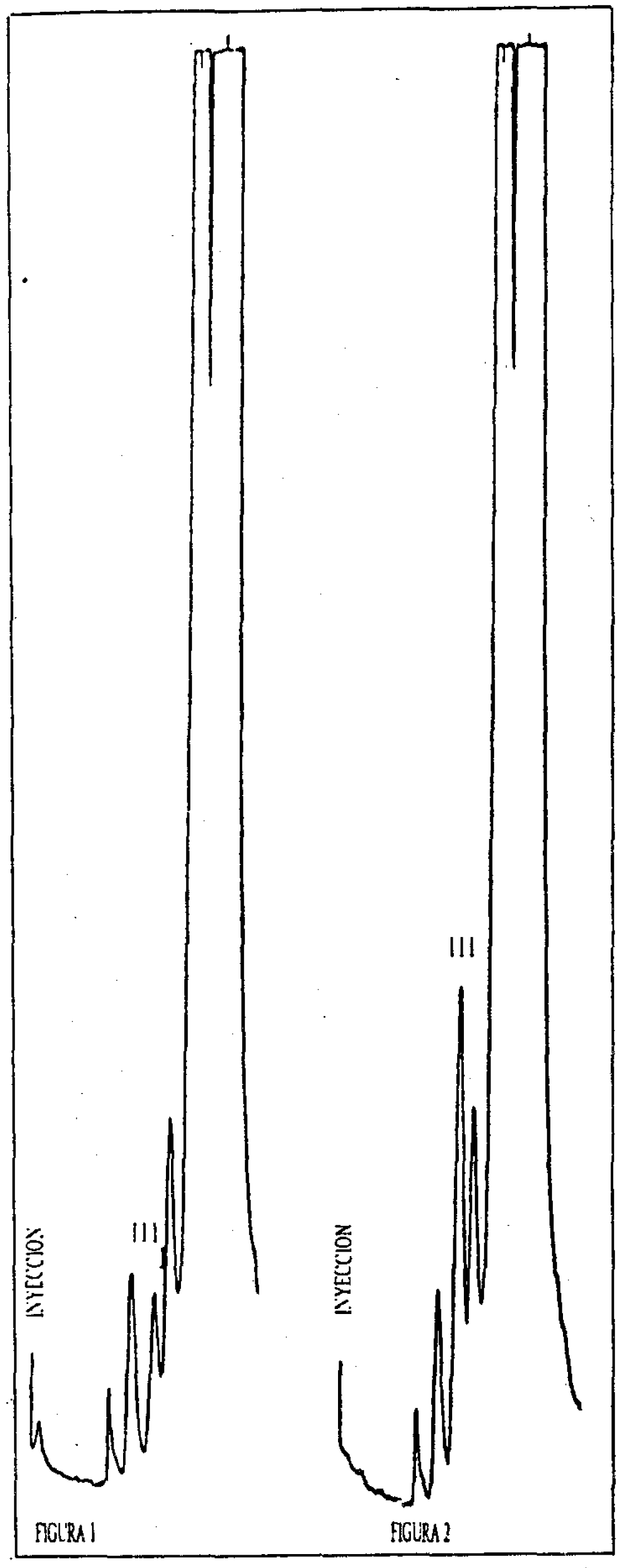
1. En las figuras 1 y 2 se representan los cromatogramas de una leche en polvo exenta de suero de quesería (3.4.a) y de la misma leche en polvo adicionada con el 5 por 100 (m/m) de suero de quesería (3.4.b), respectivamente. El pico III es el correspondiente a los GMP.
Con el fin de detectar cualquier anomalía, ya sea debida al mal funcionamiento del cromatógrafo o de las columnas, ya sea debido a la muestra a analizar, es necesario observar el aspecto de cada cromatograma antes de efectuar cualquier interpretación cuantitativa.
2. Cálculo del coeficiente de respuesta:
donde:
R: es el coeficiente de respuesta.
A(5): es el área del pico III obtenido en el análisis cromatográfico del patrón de leche en polvo adicionada con 5 por 100 (m/m) de suero de quesería (3.4.b).
A(0): es el área del pico III, obtenido en el análisis cromatográfico del patrón de leche en polvo exenta de suero de quesería (3.4.a).
P: es el porcentaje de suero de quesería presente en el patrón (3.4.b), en este caso 5.
3. Cálculo del área relativa del pico III obtenido en el análisis cromatográfico de la muestra (E).
S(E) = R × A(E)
donde:
S(E): área relativa del pico III en la muestra (E).
A(E): área correspondiente al pico III obtenida en el análisis cromatográfico de la muestra.
R: Coeficiente de respuesta calculado según (5.2).
4. Cálculo del área relativa del pico III obtenido en el análisis cromatográfico del patrón de leche en polvo exento de suero de quesería (3.4.a).
S(O) = R × A(O)
donde:
S(0): área relativa del pico III en el patrón de leche en polvo exenta de suero de quesería (3.4.a).
A(0): área correspondiente al pico III obtenido en el análisis cromatográfico del patrón de leche en polvo exenta de suero de quesería (3.4.a).
R: coeficiente de respuesta calculado según (5.2).
5. Cálculo del tiempo de retención relativo del pico III en la muestra (E).
donde:
TRR(E): tiempo de retención relativo del pico III de la muestra (E).
TR(E): tiempo de retención del pico III obtenido en el análisis cromatográfico de la muestra (E).
TR(5): tiempo de retención del pico III obtenido en el análisis cromatográfico del patrón de leche en polvo adicionada con 5 por 100 (m/m) de suero de quesería (3.4.b).
6. Por la experimentación, está demostrado que existe una relación lineal entre el tiempo relativo del pico III en la muestra y el porcentaje de suero de quesería en polvo añadido hasta el 10 por 100:
– Con un contenido < 5 por 100, el TRR(E) es > 1,000.
– Con un contenido ≥ = 5 por 100, el TRR(E) es ≤ 1,000.
– La incertidumbre admitida para los valores del TRR(E) es de ± 0,002.
7. Cálculo de porcentaje de suero de quesería en polvo presente en la muestra.
W = S(E) - [1,3 + (S(O) -0,9)]
donde:
W: porcentaje m/m de suero de quesería presente en la muestra (E).
S(E): área relativa del pico III para la muestra obtenida según (5.3).
1,3 +: media experimental del área relativa del pico III expresada en gramos de suero de quesería en 100 g de leche en polvo no adulterada.
S(0): área relativa del pico III para el patrón de leche en polvo exenta de suero de quesería (3.4.a) obtenida según (5.4).
(S(0) – 0,9): corrección que hay que efectuar en el área relativa media 1,3 cuando el valor S(0) no es igual a 0,9.
8. Repetibilidad.
La diferencia entre los resultados de dos determinaciones efectuadas simultáneamente o en un corto intervalo de tiempo por el mismo analista que utilice los mismos aparatos, con la misma toma de muestra, no debe sobrepasar el 0,2 por 100 m/m.
9. Reproducibilidad.
La diferencia entre dos resultados individuales e independientes obtenidos en dos laboratorios diferentes, con la misma toma de muestras no debe sobrepasar el 0,4 por 100 m/m.
10. Límite de detección.
Se considerará que una muestra contiene suero de quesería añadido cuando el porcentaje cuantificado sea superior a cinco en el caso de leches UHT y superior a tres en leches pasteurizadas, esterilizadas y en polvo.
[Bloque 12: #A6]
1. «Olieman (et al) 1983. A sensitive HPLC method of detecting and stimating rennet whey total soolids in skim milk powder; Neth Milk Dairy J. 37 27-36)».
2. Reglamento CEE número 3711/1986, de la Comisión, de 4 de diciembre de 1986.
Este documento es de carácter informativo y no tiene valor jurídico.
Ayúdenos a mejorar: puede dirigir sus comentarios y sugerencias a nuestro Servicio de atención al ciudadano
State Agency Official State Gazette
Avda. de Manoteras, 54 - 28050 Madrid